��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ij��ѧ��ȤС����ֻ������������ͭ�Ĺ�ҵ������ȡ�������Ȼ�����Һ���̷�����(FeSO4��7H2O)�͵������壬��̽����ҵ���ϵ������á���ʵ�鷽�����£�
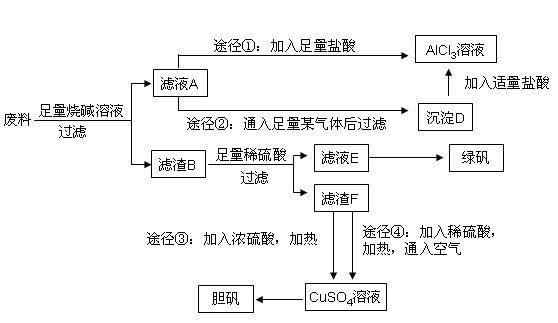
��1��д���Ͻ����ռ���Һ��Ӧ�����ӷ���ʽ��?��
��2������ҺA��AlCl3��Һ��;���Тٺ͢����֣�;������ͨ���ij���壨��̬ʱ�������˹����꣩��д��������ĵ���ʽ?������Ϊ�Ϻ�����;����?����ٻ�ڣ��������ǣ�?��
��3����ҺE�������ڿ�����һ��ʱ�����Һ�е������ӳ���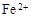 ��
��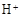 �⣬�����ܴ���?�������ӷ��ű�ʾ�����������ӵķ�����?��
�⣬�����ܴ���?�������ӷ��ű�ʾ�����������ӵķ�����?��
��4��������Fͨ������;����ȡ��������;������ȣ�;�������Ծ��е������ŵ��ǣ�?��?��
��5��;���ܷ����ķ�Ӧ�Ļ�ѧ����ʽΪ��?��
��6��ʵ���Ҵ�CuSO4��Һ��ȡ��������������������Ũ������ȴ�ᾧ��?����Ȼ���
�ο��𰸣�
��1��2Al +2OH�D + 2H2O = 2AlO2�D +3H2�� (2��)
��2��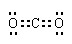 ? (1��)?��? (1��)?;������ȡ��AlCl3��Һ�л���NaCl����(1��)
? (1��)?��? (1��)?;������ȡ��AlCl3��Һ�л���NaCl����(1��)
��3��Fe3��?(1��) ȡ�����μ�KSCN������Ѫ��ɫ������Fe3�� ��(1��)
��4���ɱ��� (1�֣��������֣���ͬ) ���������ж����� (1��)
��5��2Cu +2H2SO4 +O2�� 2CuSO4 +2H2O ?(2��)
��6������ϴ�� (1��)
���������
��1����������ֻͭ�������ռ���Һ��Ӧ��
��2����NaAlO2��Ӧ����Al(OH)3����̬ʱ�������˹����꣬������CO2 ��NaAlO2 +4HCl=AlCl3+NaCl+2H2O ����AlCl3��Һ�л���NaCl���ʡ�
��3��Fe2��������������Fe3����Fe3����KSCN��Ӧ����Ѫ��ɫ��Fe2�����ܡ�
��4��;����Cu+2H2SO4= CuSO4+ SO2��+2H2O
;���� 2Cu +2H2SO4 +O2 = 2CuSO4 +2H2O;������ϡH2SO4�ɱ��ͣ��������ж�����
�����Ѷȣ�����
2�������
(1)д��Cu��ȡCuSO4(ϡH2SO4������)�ķ���ʽ________________��
(2)Cu��ŨH2SO4����Ҳ����ȡCuSO4���䷴Ӧ����ʽΪ��________________������������ȡ����________________�ߺ�(�ǰ����)��ԭ����________________��
�ο��𰸣�(1)2H2SO4��O2��2Cu 2CuSO4��2H2O
2CuSO4��2H2O
(2)2H2SO4(Ũ)��Cu CuSO4��SO2����2H2O?ǰ?��ʡ��������������Ⱦ���ŷ�
CuSO4��SO2����2H2O?ǰ?��ʡ��������������Ⱦ���ŷ�
����������ڼ��������£�Cu��O2����ת��ΪCuO��CuO������ϡH2SO4����CuSO4��H2O��
�����Ѷȣ���
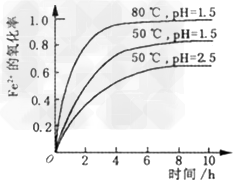
3��ѡ���� ������Һ�У�Fe2+�ᱻ������������ΪFe3+����ͬ�����£�һ��Ũ�ȵ�Fe2+����������ʱ��仯��ϵ��ͼ��ʾ�������й�˵����ȷ����
[? ]
A�����������̵����ӷ���ʽΪ��Fe2++O2+4H+==Fe3++2H2O
B��pH=1.5ʱFe2+��������һ����pH=2.5�Ĵ�
C��Fe2+�������ʽ�����Һ��pH���¶��й�
D������������ͬʱ��80��ʱFe2+�������ʱ�50��Ĵ�
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4��ѡ���� �����������Ź㷺��Ӧ�á�����˵��������ǣ�?��
A������������ǿ��ԭ�ԣ����Կ���ͨ�����ȷ�Ӧұ��ijЩ���۵����
B����������������������������ʱ������������
C������������ϡ���ᣬ��Ӧ�����ӷ���Ϊ��Fe��4H����NO3-=Fe3����NO����2H2O
D������Fe������Cu�Ļ�ѧ���Զ���ԭ����ǿ�����߶��������ᷴӦ��������
�ο��𰸣�D
�������������Cu����ڿ�״ͭ��˵��ֻ��״̬�ı䣬����ѧ���ʲ��䣬�䲻�������ᷴӦ����������
�����Ѷȣ���
5��ѡ���� ֤����Һ���Ƿ���Fe2�����������ȷ��˳����
�ټ������ữ��KMnO4��Һ���ڼ�������ˮ���۵μ�����KSCN��Һ
A���٢�
B���ڢ�
C���٢ڢ�
D���ۢ�
�ο��𰸣�D
����������ȵμ�����KSCN��Һ�������Ա仯�������������ˮ��������Ѫ��ɫ������֤��ԭ��Һ�к���Fe2����һ�㲻�ʺ�ѡKMnO4��Һ��ΪKMnO4��Һ��������ɫ����ֹ���š�2������
����������Fe2������,��ʹ�ữ��KMnO4��Һ��ɫֻ��˵���л�ԭ�ԣ�����ȷ�����Ƕ������Ĵ��ڡ�
�����Ѷȣ�һ��