微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 某化学小组采用下图装置模拟电解饱和食盐水制备氢气,通过氢气还原氧化铜测定Cu的相对原子质量,同时检验氯气的氧化性(图中夹持和加热仪器已经略去).

(1)写出装置甲中反应的离子方程式______.为完成上述实验,正确的连按方式为a连接______,b连接______(填字母).
(2)①装置乙烧杯中液体的作用是______.A瓶内盛装的溶液最好是______(填字母).
a.I2-淀粉溶液b.NaOH溶液 c.FeCl2与KSCN混合溶液d.Na2SO3溶液
②加热装置丙中的氧化铜粉末之前,除了要检查该装置的气密性还需进行的必要操作是______.
(3)利用装置丙测定Cu的相对原子质量,现有两种方案:①测得反应前后洗气瓶B及其中液体质量差m1,②测得反应前后U形管及其中固体质量差m2.你认为合理的方案为______(填“①”或“②”).若采用测得反应后硬质玻璃管中剩余固体的质量m3的方案,已知O的相对原子质量为16,实验中氧化铜样品质量为m,则测定Cu的相对原子质量的表达式为______,该方案在反应后硬质玻璃管冷却过程中没有一直通氢气,会导致测定Cu韵相对原子质量______(填“偏大”、“偏小”或“无影响”),理由是______.
参考答案:(1)电解饱和食盐水时,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,溶液中同时生成氢氧根离子,所以电解反应离子方程式为2Cl-+2H2O电解.2OH-+H2↑+Cl2↑,要检验氯气的氧化性,则氯气连接强还原性的物质且反应现象要明显,故选c,用氢气还原氧化铜来检验氢气,因为电解得到的氢气中含有水蒸气,所以在实验前要除去水蒸气,故选e,
故答案为:2Cl-+2H2O电解.2OH-+H2↑+Cl2↑;e;c;
(2)①氯气有毒,不能直接排空,氯气和水反应生成酸,所以氯气可以用碱性物质来处理,所以装置乙烧杯中液体的作用是吸收多余的氯气,防止环境污染;
氯气具有强氧化性,能氧化强还原性的物质,要检验氯气,必须选用强还原性的物质且反应现象明显,
a.氯气能氧化碘而使溶液褪色,氯气和水反应生成的次氯酸也能使溶液褪色,所以无法证明氯气的氧化性,故不选;
b.氯气和氢氧化钠溶液反应生成氯化钠和次氯酸钠,反应现象不明显,故不选;
c.氯气能把亚铁离子氧化成三价铁离子,铁离子和硫氰化钾溶液反应生成血红色溶液,反应现象明显,且能检验氯气的氧化性,故选;
d.氯气能氧化亚硫酸钠生成硫酸钠,但反应前后溶液颜色不变,反应现象不明显,故不选;
故答案为:吸收多余的氯气,防止环境污染;c;
②氢气是可燃性气体,与氧气混合,加热容易发生爆炸危险,加热氧化铜之前要通入氢气排尽装置内空气,故答案为:通入氢气排尽装置内空气;
(3)①中质量的差量是氢气还原氧化铜得到的物质,与铜有关,所以能计算铜的相对原子质量,②中质量的差量是氢气中原来的水蒸气,与铜无关,所以不能计算铜的相对原子质量,故选①;
硬质玻璃管中的质量差是氧元素的质量=m-m3,
设铜的相对原子质量为x,
CuO------O
1 16
mx+16 m-m3
x=16m3m-m3,
反应生成的铜被空气的氧气氧化使m3数据增大,则16m3m-m3偏大,所以导致测定结果偏大,
故答案为:①;16m3m-m3;偏大;反应生成的铜被空气的氧气氧化使m3数据增大,导致测定结果偏大.
本题解析:
本题难度:简单
2、选择题 下列关于工业生产说法不正确的是( )
A.电解精炼铜时,用粗铜做阴极,纯铜做阳极
B.在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率
C.在炼铁工业,需要的原料有铁矿石、焦炭、空气、石灰石等
D.在侯氏制碱工业中,向饱和氯化钠溶液中先通氨气,后通二氧化碳
参考答案:A
本题解析:
本题难度:简单
3、选择题 我国第五套人民币中的一元硬币材料为钢芯镀镍,依据你所掌握的电镀原理,你认为在硬币制作时,钢芯应作?
[? ]
A.阴极
B.阳极
C.正极
D.负极
参考答案:A
本题解析:
本题难度:简单
4、简答题 钢铁的生产与使用是人类文明和生活进步的一个重要标志.
(1)工业铝热法炼铁的主要化学反应方程式______.
(2)炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑.
试回答:①铁锅的腐蚀主要是由______腐蚀造成的.
②铁锅锈蚀的负极反应式为______.
(3)通常使用钢铁是铁和______的合金;当马口铁(表层镀锡)镀层被损坏后,这时被腐蚀速度比普通铁______(填“快”或“慢”).为防止轮船的船体在海水中腐蚀,一般在船身连接______(填“锌块”或“铜块”)
参考答案:(1)铝热法冶炼金属铁的原理方程式为:2Al+Fe2O3高温.2Fe+Al2O3,故答案为:2Al+Fe2O3高温.2Fe+Al2O3;
(2)①在弱酸或中性条件下,铁发生吸氧腐蚀,故答案为:吸氧;
②铁、碳和电解质溶液构成原电池,铁作负极,发生失电子的氧化反应,即Fe=Fe2++2e-,故答案为:Fe=Fe2++2e-;
(3)钢铁是铁和碳的合金,当马口铁(表层镀锡)镀层被损坏后,金属铁、锡以及电解质形成原电池,金属铁为负极,这时被腐蚀速度比普通铁快,要保护金属铁,可以连接一种比金属铁活泼的金属,如金属锌,故答案为:碳;快;锌块.
本题解析:
本题难度:简单
5、选择题 下列实验操作或装置符合实验要求的是
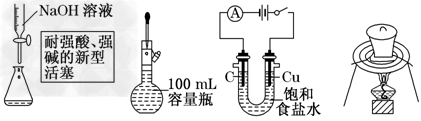
[? ]
A.量取15.00?mL?NaOH溶液
B.定容
C.电解制Cl2和H2
D.高温煅烧石灰石
参考答案:A
本题解析:
本题难度:一般