��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
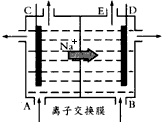
1��ѡ���� ��ͼΪ�����ӽ���Ĥ����ⱥ��ʳ��ˮԭ��ʾ��ͼ������˵������ȷ����
[? ]
A����E���ݳ���������H2
B����B�ڼ��뺬����NaOH��ˮ��Һ����ǿ������
C����״����ÿ����22. 4 L Cl2��ͬʱ����2 mol NaOH
D������ˮ�к�Ca2+��Mg2+��Fe3+��SO42-�����ӣ�����ʱ�ȼ�Na2CO3��Һ
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2��ѡ���� ��ѧ�ν��ܵ�Ӧ�õ�ⷨ�Ʊ���������Ҫ�����֣�һ�����Ĺ�ҵ�Ʊ������ǵ�ⱥ��NaCl��Һ�Ʊ��ռ ���ǽ����Ƶ��Ʊ������й�����������ҵ��������������ȷ����
[? ]
A����ⷨ����ʱһ����������̬�����������е�⣬��Ҳ��������Ӧ����������̬��AlCl3
B����ⷨ������ʱ��ÿת��3mol���ӵ�ʱ����������1mol����
C���ڵ�ⱥ��NaCl��Һ�У������е�������������H2��NaOH��������������
D����ⱥ��NaCl��Һ�ͽ����Ƶ�ұ�����õ���NaCl�����ʱ��������Cl-ʧ����
�ο��𰸣�B
���������
�����Ѷȣ�һ��
3������� [��ѧ--ѡ��ѧ�뼼��]
�غ��������ŷḻ�ĺ�ˮ��Դ����ˮռ�����ܴ�ˮ����97.4%����ˮ�����౦�����Ȼ��Դ�����Ѻ�ˮ�����ͻ�����������������ȿ��Խ����ˮ��Դȱ�������⣬�ֿ��Գ�����ú�ˮ��Դ���Ӻ�ˮ�п�����ȡ���ֻ���ԭ�ϣ���ͼ��ij�����Ժ�ˮ��Դ�ۺ����õ�ʾ��ͼ��

��1�����оٺ�ˮ���������ַ���______��______��
��2��ʹ�����ӽ�����֬��ˮ�е����ӽ��н���Ҳ�dz��õ�ˮ�����������۱�ϩ������һ�����ӽ�����֬��д���۱�ϩ���Ƶ���Ľṹ��ʽ______��
��3����������ѻ��Br2����������ֽ�Br2��ԭΪBr?-����Ŀ���ǣ�______��
�������SO2ˮ��Һ����Br2�������ʿɴ�95%���йط�Ӧ�����ӷ���ʽ______
��4������ȡ��ˮ�Ȼ�þʱ��Ҫ�ڸ����HCl�����м���MgCl2��6H2O��ԭ��______��
��5�������ˮ�Ȼ�þ���õ�þ�������ض��Ļ�������ȴ��Ϊ����þ�����������п�������þ��������ȴ������______
A��H2?B��CO2?C������?D��O2?E��ˮ����
��6����±����ˮ�����ᾧ�����ʳ�κ��ĸҺ���к��н϶��NaCl��MgCl2��KCl��MgSO4�����ʣ��ó������ⶨ��±��MgCl2�ĺ�����g/L�����ⶨ������Ӧ��ȡ��������______��
�ο��𰸣���1����ˮ���������ú�ˮ����������ˮ�Ĺ��̣������ķ����У�����Ĥ�����䶳�������ӽ������ȣ��ʴ�Ϊ����������������
��2���۱�ϩ�����DZ�ϩ���ƼӾ۷�Ӧ�IJ�����ݾۺ����ҵ���ķ���������Ϊ��ϩ���ƣ��ṹ��ʽΪ��CH2=CHCOONa���ʴ�Ϊ��CH2=CHCOONa��
��3����������ѻ��Br2����������ֽ�Br2��ԭΪBr-����Ϊ�˸�����Ԫ�أ���SO2ˮ��Һ����Br2��ԭ������ʽΪ��
Br2+SO2+2H2O=4H++SO42-+2Br-���ʴ�Ϊ��������Ԫ�أ�Br2+SO2+2H2O�T4H++SO2-4+2Br-��
��4���Ȼ�þ�е�þ������ˮ�⣬�ڸ����HCl�����У�������MgCl2ˮ�⣬�Ҵ���MgCl2?6H2O���Ȳ�����ˮ�������ܵõ���ˮMgCl2��
�ʴ�Ϊ���ڸ����HCl�����У�������MgCl2ˮ�⣬�Ҵ���MgCl2��6H2O���Ȳ�����ˮ�������ܵõ���ˮMgCl2��
��5���ܺͽ���þ������Ӧ�����壺������������������̼��ˮ�����Կ�����������þ��������ȴ������ѡA��
��6����±�к���MgCl2��MgSO4���ֺ�þ���ӵ��Σ��ⶨ��±��MgCl2�ĺ������뽫����þ�е�þ����ȥ����������������BaCl2��Һ������������ӣ������������ӵ������������MgSO4������Ȼ��������NaOH��Һ����Mg2+������ܵ�Mg2+����ȥMgSO4�е�Mg2+�õ�MgCl2������
�ʴ�Ϊ����±��Ʒ���������NaOH��Һ������Mg��OH��2������������BaCl2��Һ������BaSO4��������
���������
�����Ѷȣ�һ��
4��ѡ���� ���������У�����������ʵ�ʵ���
[? ]
A���ϳɰ���ҵ�У�N2��H2��������ӦΪ���ʵ���֮��1��3
B����ⷨ������ͭ���ô�ͭ������
C����ҵ�ϵ�ⱥ��ʳ��ˮ���ռ�����ӽ���Ĥ��ֹOH-��������
D���ڶƼ��ϵ��п��п������
�ο��𰸣�A
���������
�����Ѷȣ���
5������� ����Լռ����������71%����ˮ��ѧ��Դ�����þ��зdz�������ǰ����þ����Ͻ���һ����;�ܹ�Ľ������ϣ�Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ģ�����Ҫ�������£�
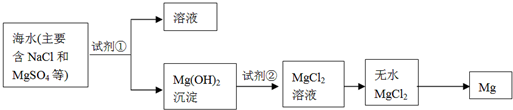
��Ϊ��ʹMgSO4ת��ΪMg��OH��2���Լ��ٿ���ѡ��______��
���Լ��ڿ���ѡ��______��
���Դӽ�Լ��Դ����߽���þ�Ĵ��ȷ������������˵�ұþ������______��
A��Mg��OH��2
MgOMg
B��Mg��OH��2MgOMg
C��Mg��OH��2MgCl2Mg
D��Mg��OH��2MgCl2Mg
��д������Ʊ�þ�Ļ�ѧ����ʽ______��
�ο��𰸣���ʹMgSO4ת��ΪMg��OH��2��Ӧѡ����ת���в������µ����ӣ����Լ���ѡ��NaOH���ʴ�Ϊ��NaOH��
��Mg��OH��2ת��ΪMgCl2ʱ�������ܽ�������������ӿ�֪���Լ��ڿ���ѡ�����ᣬ�ʴ�Ϊ�����
��MgO���۵�ߣ��������õ���ԭ�����Ʊ�þ����ABD�������˵�ұþ������C���ʴ�Ϊ��C��
���Ʊ�þһ�����õ�����ڵ�MgCl2����ⷴӦΪMgCl2�����ڣ�?���?.?Mg+Cl2����
�ʴ�Ϊ��MgCl2�����ڣ�?���?.?Mg+Cl2����
���������
�����Ѷȣ�һ��