微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对于可逆反应:A2(g)+3B2(g) 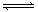 2AB3(g)?△H<0,下列图像正确的是(?)
2AB3(g)?△H<0,下列图像正确的是(?)
(友情提示:V-速率;? W(AB3)-AB3的质量分数)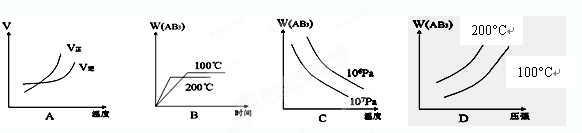
参考答案:B
本题解析:正反应是放热反应,升高温度,正、逆反应速率均加快,平衡向逆反应方向移动,W(AB3)减小,A错误、B正确、D错误;增大压强,平衡向正反应方向移动,W(AB3)增大,C错误。
点评:解图像题要看清图像中横坐标、纵坐标的涵义及图像中曲线的走向和位置高低。
本题难度:简单
2、填空题 某温度时在密闭容器中A、B、C三种气态物质的物质的量随时间变化的曲线如图所示。请回答下列问题:
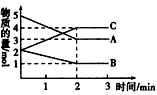
(1)该反应的反应物是_______,生成物是_______。
(2)该反应的化学方程式为________________。
(3)反应开始至2 min时,____(填“能”或“不能”)用物质C表示该反应的反应速率,若能,其反应速率为 _______,若不能,其原因是_________。
(4)2 min后,A、B、C的物质的量不再随时间的变化而变化,说明在这个条件下,该反应__________。
参考答案:(1)A、B;C
(2)2A+B=2C
(3)不能;容器体积未知,无法求出物质C的浓度变化量?
(4)已达化学平衡状态(或达到最大限度)
本题解析:
本题难度:一般
3、选择题 下列物质溶于水时会破坏水的电离平衡,且属于电解质的是(?)
A.氯气
B.二氧化碳
C.碘化钾
D.醋酸钠
参考答案:D
本题解析:略
本题难度:简单
4、填空题 温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g) PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据如图:
PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据如图:
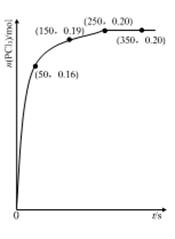
下列说法正确的是
A.反应在前50 s 的平均速率v(PCl3)=0.0032 mol・L-1・s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol・L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入2.0 mol PCl3和2.0mol Cl2,达到平衡时,PCl3的转化率小于80%
D.相同温度下,起始时向容器中充入1.0 mol PCl5、0.20mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
参考答案:D
本题解析:A、反应在前50 s 的平均速率v(PCl3)=0.16÷2÷50="0.0016" mol・L-1・s-1,错误;B、平衡时c(PCl3)=0.20÷2=0.10mol・L-1,升高温度其浓度增大,平衡正向移动,反应吸热,错误;C、相同温度下,起始时向容器中充入1.0 mol PCl3和1.0 mol Cl2时与元平衡为等效平衡, PCl3的转化率小于80% ,充入2.0 mol PCl3和2.0 mol Cl2,压强增大平衡向生成PCl5方向移动,PCl3的转化率增大,错误;
PCl5(g) PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
始量? 1? 0? 0
转化量? 0.2? 0.2? 0.2
平衡量? 0.8? 0.2? 0.2
k=(0.2/2×0.2/2)÷0.8/2=0.025
此时浓度熵Q=(0.2/2×0.2/2)÷1.0/2=0.02<0.025,平衡正向移动,v(正)>v(逆),正确。
本题难度:一般
5、选择题 将4molA气体和2molB气体在2L的容器中混合,并在一定条件下发生如下反应2A(g)+B(g)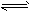 2C(g),若2s后测得C的浓度为0.6mol/L,现有下列几种说法,其中正确的是
2C(g),若2s后测得C的浓度为0.6mol/L,现有下列几种说法,其中正确的是
[? ]
①用物质A表示的平均反应速率为0.3mol/(L・s)
②用物质B表示的平均反应速率为0.6mol/(L・s)
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7mol/L
A.①③
B.①④
C.②③
D.③④
参考答案:B
本题解析:
本题难度:简单