微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列事实中,不能用勒沙特列原理解释的是
A.开启啤酒瓶后,瓶中立刻泛起大量泡沫
B.工业合成氨时选择铁做催化剂能极大加快反应速率
C.向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低
D.工业生产硫酸的过程中使用过量的空气以提高SO2的利用率
参考答案:BC
本题解析:勒夏特列原理是改变影响化学平衡移动的一个因素,平衡朝减弱这种改变的方向移动。B、催化剂不影响平衡移动,C、盐酸为强酸,稀释过程,没有平衡移动。
本题难度:一般
2、选择题 下列事实不能用勒夏特列原理解释的是
A.温度控制在500℃有利于合成氨反应
B.实验室中常用排饱和食盐水的方法收集Cl2
C.将相同体积、相同pH盐酸与醋酸分别稀释相同倍数,后者的pH变化值小于前者
D.打开碳酸饮料会有大量气泡冒出
参考答案:A
本题解析:如果改变影响平衡的1个条件,则平衡就向能够减弱这种改变的方向移动,这就是勒夏特列原理。合成氨是放热反应,所以高温是不利于平衡向正反应方向移动的,因此选项A不能用勒夏特列原理解释,其余选项都可以用勒夏特列原理解释。所以答案选A。
本题难度:一般
3、选择题 现有容积为1 L的甲乙两个恒温恒容密闭容器,向甲中加入2 mol A气体和2 mol B气体后发生如下反应:A(g)+B(g) C(g) △H=" -a" kJ・mol-1,反应达到平衡状态时生成1 mol C气体,放出热量Q1kJ;乙中加入1molC气体,反应达到平衡时,吸收热量Q2kJ,则Q1 与Q2的相互关系正确的是(?)
C(g) △H=" -a" kJ・mol-1,反应达到平衡状态时生成1 mol C气体,放出热量Q1kJ;乙中加入1molC气体,反应达到平衡时,吸收热量Q2kJ,则Q1 与Q2的相互关系正确的是(?)
A.Q1 + Q2 = a
B.Q1 + 2Q2 < 2a
C.Q1 + 2Q2 > 2a
D.Q1 + Q2 < a
参考答案:C
本题解析:在乙中若加入2molC气体,反应达到平衡时,吸收热量Q3kJ,那么依题意有:Q1 + Q3= a。但现在加的是1molC气体,如果这1molC气体与原来的2molC气体是等效平衡的话,则有:Q1 + 2Q2= 2a,我们可以理解为是在2molC达到平衡以后再取走其中的一半,此时相当于压强减小,平衡向着体积增大的左方移动,使得吸收的热量增加,因此有:Q1 + 2Q2 > 2a,选C。
本题难度:一般
4、选择题 一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20.0%,与反应前的体积相比,反应后体积缩小的百分率是
A.80.0%
B.20.0%
C.16.7%
D.83.3%
参考答案:C
本题解析:解:由合成氨的化学反应达到平衡时,测得混合气体中氨气的体积分数为20.0%,
设平衡时气体总体积为100L,则氨气为100L×20%=20L,
气体缩小的体积为x,则
N2+3H2?2NH3?△V
1? 3? 2? 2
20L? x
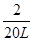 =
=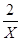 ,
,
解得x=20L,
原混合气体的体积为100L+20L=120L,
反应后体积缩小的百分率为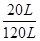 ×100%=16.7%,
×100%=16.7%,
故选:C
本题难度:一般
5、填空题 (9分)(1)在容积为3L的密闭容器中,由I2(g)和H2(g)合成HI(g),在其他条件不变的情况下,研究温度对反应的影响,HI的物质的量的变化情况如下图所示。
①温度为T1时,在0~tAmin内,H2的消耗速率
v (H2)=________________
②分析右图所示图像,下列说法正确的是_________(填序号)
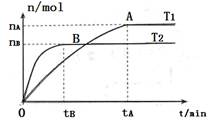
a.温度为T2,容器内气体密度不变时,反应到达B点所示状态
b.平衡状态从A点移动到B点,n(HI)/n(H2)增大
c.该反应为放热反应
(2) 加水稀释0.1mol・L-1的HF溶液,下列各量中增大的是________(填序号)
a.c(H+)? b. Ka(HF)? c. c(F-)/c(H+)? d. c(H+) / c(HF)
(3) 在0.1mol・L-1HCl溶液中加入过量AgNO3溶液,产生白色沉淀,再滴加KI溶液,出现黄色沉淀,试写出有关的离子方程式?、?。
参考答案:(1)nA/6tA mol・L-1・min-1(2分)? c?(2分)
(2)d? (2分)
(3)Ag++Cl-=AgCl↓(1分)? AgCl(s)+I-(aq)=AgI(s)+Cl-(aq) (2分)
本题解析:①根据图像可知在在0~tAmin内,生成的碘化氢是nAmol,则消耗氢气是0.5 nAmol,所以反应速率是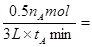 nA/6tAmol/(L・min)。
nA/6tAmol/(L・min)。
②因为反应前后体积不变,所以混合气的密度始终是不变的。B点最先达到平衡状态,所以B点对应的温度高。由A点到B点碘化氢的物质的量减少,平衡向逆反应方向移动,所以n(HI)/n(H2)减小。升高温度,平衡向逆反应方向移动,所以正反应是放热反应。
(2)HF属于弱电解质,存在电离平衡HF F-+H+。稀释有利于电离,即在稀释过程中氢离子和氟离子的物质的量是增加的,但其浓度是减小的,所以OH-的浓度是增大的。HF的物质的量是减小的,浓度也是减小的。电离常数和温度有关,与浓度无关,因此正确的答案是d。
F-+H+。稀释有利于电离,即在稀释过程中氢离子和氟离子的物质的量是增加的,但其浓度是减小的,所以OH-的浓度是增大的。HF的物质的量是减小的,浓度也是减小的。电离常数和温度有关,与浓度无关,因此正确的答案是d。
(3)本题主要考查了溶解平衡的相关内容。由于AgI的Ksp小,所以AgCl可转化为AgI。
本题难度:一般