微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 液氨与水性质颇为相似,其电离方程式可表示为:2NH3 NH4++NH2-。某温度下其离子积常数为1×10-30(mol・L-1)2。液氨中的pNH4与水中的pH类似,向1L液氨中加入2.3gNa此时上述平衡____________移动(填“向正方向”“向逆方向”或“不”),完全反应后溶液的pNH4=__________。
NH4++NH2-。某温度下其离子积常数为1×10-30(mol・L-1)2。液氨中的pNH4与水中的pH类似,向1L液氨中加入2.3gNa此时上述平衡____________移动(填“向正方向”“向逆方向”或“不”),完全反应后溶液的pNH4=__________。
参考答案:(1)向正方向
(2)29
本题解析:2.3gNa加入液氨后发生反应2Na+2NH4+=2Na++2NH3+H2↑, c(NH4+)减小,平衡向正反应方向移动,2.3gNa的物质的量为0.1mol,所以生成NH2-的物质的量为0.1mol,c(NH4+)=1×10-30(mol・L-1)/ 0.1mol・L-1= 1×10-29mol・L-1,pNH4+=29
本题难度:简单
2、选择题 MOH和ROH两种碱的溶液分别加水稀释时,pH变化如图所示。下列叙述中正确的是(?)
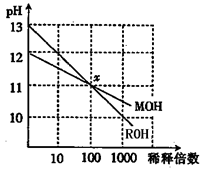
A.MOH是一种强碱
B.在x点,MOH完全电离
C.在x点,c(M+)==c(R+)
D.稀释前,c(ROH)==10c(MOH)
参考答案:C
本题解析:A.ROH是一种强碱,MOH为弱碱;
B.在x点,MOH和ROH溶液pH值相同;
D.稀释前,c(ROH中的OH-)==10c(MOH中的OH-);
本题难度:一般
3、实验题 (10分)用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2 g含有少量中性易溶杂质(不与盐酸反应)的样品,配成500 mL待测溶液。称量时,样品可放在??(填编号字母)称量。
A.小烧杯中? B.洁净纸片上? C.托盘上
(2)滴定时,用0.2000 mol・L-1的盐酸来滴定待测溶液,不可选用??(填编号字母)作指示剂。
A.甲基橙? B.石蕊? C.酚酞? D.甲基红
(3)滴定过程中,眼睛应注视?;
在铁架台上垫一张白纸,其目的是?。
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是?mol・L-1,烧碱样品的纯度是?。
滴定次数
| 待测溶液体积(mL)
| 标准酸体积
|
滴定前的刻度(mL)
| 滴定后的刻度(mL)
|
第一次
| 10.00
| 0.40
| 20.50
|
第二次
| 10.00
| 4.10
| 24.00
|
(5)下列实验操作对滴定结果产生什么影响(填“偏高”、“偏低”或“无影响”)?
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果________。
②若将锥形瓶用待测液润洗,然后再加入10.00 mL待测液,则滴定结果________。
参考答案:(1)A(1分)? (2)B(1分) (3)锥形瓶内溶液颜色的变化(1分)
便于观察锥形瓶内液体颜色的变化,减小滴定误差(1分)
(4)0.4000(2分)? 97.56%(2分)? (5)①偏高(1分)?②偏高(1分)
本题解析:(1)由于氢氧化钠具有吸水性和腐蚀性,所以秤量时应该放在烧杯中,答案选A。
(2)由于石蕊试液的颜色变化不明显,所以一般不用石蕊试液作酸碱指示剂,答案选B。
(3)滴定的关键是准确判断滴定终点,因此在滴定过程中眼睛要注视锥形瓶内溶液颜色的变化。白纸其对照作用,便于观察锥形瓶内液体颜色的变化,减小滴定误差。
(4)两次滴定所消耗的盐酸体积是20.10ml和19.90ml,其平均值是20.00ml。所以氢氧化钠溶液的是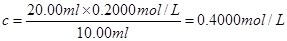 。
。
(5)①滴定管俯视读数则读数偏小,所以开始俯视,滴定终点平视,则消耗盐酸的体积偏大,滴定结果偏高。
②若将锥形瓶用待测液润洗,则消耗盐酸的体积偏大,滴定结果偏高。
本题难度:一般
4、选择题 室温下,在pH=12的某溶液中,由水电离的c(OH-)为(?)
①1.0×10-7 mol・L-1?②1.0×10-6 mol・L-1?③1.0×10-2 mol・L-1?④1.0×10-12 mol・L-1?
A.③
B.④
C.①③
D.③④
参考答案:D
本题解析:当水的电离受抑制时,由水电离的c(OH-)为1.0×10-12 mol・L-1 ;当促进水的电离时,由水电离的c(OH-)为1.0×10-2 mol・L-1
本题难度:一般
5、选择题 下列溶液,加热后颜色变浅的是
A.稀氨水和酚酞溶液
B.滴有酚酞的Na2CO3溶液
C.溶有氯气的品红溶液
D.溶有SO2的品红溶液
参考答案:A
本题解析:略
本题难度:简单