| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《物质的量》高频试题巩固(2017年最新版)(八)
参考答案:A 本题解析:该题利用溶液A中阴阳离子所带电荷数相等这一规律,即可轻松解答。若A溶液中Na+、Cl-、Br-的物质的量之比为3∶1∶4,不能保持溶液呈电中性,故A肯定不正确;B、C、D均可满足题意,故正确。 本题难度:一般 2、填空题 (8分)明矾的化学式为KAl(SO4)2 ?12H2O,相对分子质量为474。它是一种常用净水剂。 参考答案:(每空2分) 本题解析:(1)明矾是强电解质,在水中完全电离产生钾离子、铝离子、硫酸根离子,电离方程式为KAl(SO4)2=K++Al3++2SO42-; 本题难度:一般 3、填空题 Ⅰ。(每空1分,共4分)⑴通常状况下,甲同学取1 mol H2O加热到100℃时,液态水会汽化为水蒸气(如图所示),该过程属于??变化。 |
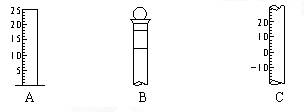
 ?③刻度线?④浓度?⑤容积
?③刻度线?④浓度?⑤容积参考答案:
本题解析:略
本题难度:一般
4、选择题 废水中CrO42-浓度降至5.0×10-7 mol・L-1以下才能排放。含CrO42-的废水可用沉淀法处理:加入可溶性钡盐生成BaCrO4沉淀,再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于(已知:Ksp(BaCrO4)=1.2×10-10)
A.1.2×10-5 mol・L-1
B.2.4×10-4 mol・L-1
C.3.6×10-4 mol・L-1
D.4.8×10-4 mo l・L-1
l・L-1
参考答案:B
本题解析:略
本题难度:简单
5、填空题 有一种氯化钠与氯化钾的混合物,它所含钾与钠的物质的量之比为3∶1,求:
(1)混合物中氯化钾的质 量分数。
(2)含1 mol Cl-的混合物的质量。
参考答案:(1)79.3%(2)70.5 g
本题解析:(1)则设混合物中有1mol的氯化钠,则氯化钾有3mol,混合物的总质量=1*58.5+3*74.5=282g,所以氯化钾的质量分数=(74.5*3/282)*100%=79.3%
(2)总的氯离子为1mol,所以氯化钾为0.75mol,氯化钠为0.25mol,所以混合物的质量="0.75*74.5+0.25*58.5=70.5" g
点评:本题抓住在氯化钾中,氯离子的物质的量等于钾离子的物质的量等于氯化钾的物质的量,而且计算过程中需要对物质的量与质量间的换算非常熟练。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点讲解《酯》高频考.. | |