��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��10�֣�ij��ѧ��ѧʵ��С��Ϊ��֤���ͱȽ�SO2����ˮ��Ư���ԣ����������װ�ã�
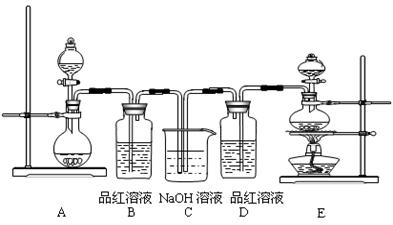
��1��ʵ���ҳ���װ��E�Ʊ�Cl2��ָ���÷�Ӧ��Ũ���������ֳ�������______��_______��?
��2����Ӧ��ʼ����B��D�����Թ��е�Ʒ����Һ����ɫ��ֹͣͨ����B��D�����Թܼ��ȣ������Թ��е�����ֱ�Ϊ��B ?�� D_________________��
��3��װ��C��������________________________________��
��4����ʵ��С��ļס�����λͬѧ��������������װ�ð���ͼװ�ü�������ʵ�飺
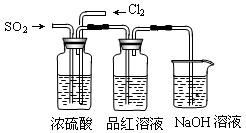
ͨ��һ��ʱ���ͬѧʵ�������Ʒ����Һ��������ɫ������ͬѧ��ʵ��������Ʒ����Һ��ʱ������Ʊ��Խ��Խdz��
�Ը��ݸ�ʵ��װ�ú�����ͬѧ��ʵ�����ش����⡣
���Է�����ͬѧʵ������У�Ʒ����Һ����ɫ��ԭ���ǣ�?
?��
������Ϊ��ͬѧ������������Ʒ����Һ���Խ��Խdz�ģ�
?
�ο��𰸣���10�֣���1�����ԣ�1�֣�����ԭ�ԣ�1�֣���
��2��B��Һ�ָ���ɫ��1�֣���? D��Һ����ɫ��1�֣�
��3�����ն����SO2��Cl2����ֹ��Ⱦ������2�֣�
��4���ٿ���SO2��Cl2�����ʵ���֮��1�U1���������߷�����Ӧ��������Ư���Ե�H2SO4��HCl��SO2 + Cl2 + 2H2O =SO42��+ 2Cl��+ 4H+ ��2�֣�
�ڿ���SO2��Cl2���������ʵ���,ʹ֮����ȣ�2�֣�
�����������
�����Ѷȣ�һ��
2��ʵ���� �ں�����ߺ�DZˮͧ�п����ù���������Ϊ��������ij��ѧ̽��ѧϰС��ѡ���ʵ��Ļ�ѧ�Լ���ʵ����Ʒ������ͼ��ʵ��װ�ã�����ʵ����֤���������ƿ��������������У�A��ʵ������ȡCO2��װ�ã�D��װ�й������ƹ��塣

��1��д��Aװ���з�����Ӧ�����ӷ���ʽ��?��
��2����д���пո�
����
| �����Լ�
| ������Լ���Ŀ��
|
B
| ����NaHCO3��Һ
| ?
|
C
| ?
| ��ȥCO2�е�ˮ����
|
E
| ?
| ?
|
��3������Cװ�ã���ʵ�ָ�ʵ��Ŀ���Ƿ���Ӱ��?����ǡ�����
ԭ��????��
��4���Թ�F���ռ������岢��ˮ��ȡ������һ��ʵ�����Ϊ��?��
�ο��𰸣���1��CaCO3+2H+��Ca2++H2O+CO2��?��2�֣�
��2����ÿ��1�֣�
����
�����Լ�
������Լ���Ŀ��
B
?
��ȥCO2�е�HCl
C
Ũ����
?
E
NaOH��Һ
��ȥO2�е�CO2
��3����1�֣���2Na2O2+2H2O=4NaOH+O2?��2�֣�
��4�������Ѵ����ǵ�ľ�������Թܿ��ڣ�ľ����ȼ��֤���Թ����ռ���������������?��2�֣�
�����������1��A��ʵ������ȡCO2��װ�ã����Է�����Ӧ�����ӷ���ʽ��CaCO3+2H+��Ca2++H2O+CO2����
��2���������ɵ�CO2�к���ˮ�������Ȼ������壬�����ٺ������Ʒ�Ӧ֮ǰ����Ҫ���ӡ�B�б���̼��������Һ��ȥ���������Ȼ��⣻C�е��Լ�ԭ������CO2����ѡ�����Ũ����������ɵ������к���δ��Ӧ��CO2�����Ϊ�˷�ֹCO2�������ռ��ĸ��ţ���Ҫ�ȳ�ȥCO2����E������������Һ�����þ��dz�ȥ�����е�CO2���塣
��4������ˮ����Ҳ�ܺ������Ʒ�Ӧ�������������Ҳ����֤���������ƿ�������������������Cװ�ã���ʵ�ָ�ʵ��Ŀ����Ӱ�졣
��4���Թ�F���ռ������岢��ˮ��ȡ������һ��ʵ�����Ӧ���Ǽ����ռ��������Ƿ�����������ȷ�������������Ѵ����ǵ�ľ�������Թܿ��ڣ�ľ����ȼ��֤���Թ����ռ���������������2���Ʊ������ӣ��������������������й��жϡ������ļ���
�������������е��Ѷȵ����⣬����ע�ػ���������ʵ��������������ѵ��������������ѧ���Ͻ���ʵ����ƺͶ��ֲ������������ѧ�����ۺ�ʵ��������������Ҫ����ʵ���������Ϊ���ģ�ͨ����ʲô��Ϊʲô���������ص㿼��ʵ����������Ĺ淶�Ժ�ȷ�Լ��������֪ʶ���ʵ�������������
�����Ѷȣ�һ��
3��ʵ���� ij��ѧʵ����ȤС���ڡ�̽����ˮ���廯������Һ��Ӧ����ʵ���з��֣������������廯������Һ�У�����1��2����ˮ������Һ�ʻ�ɫ����
�����ϡ�
| ��ˮ���嵥�ʵ�ˮ��Һ���������嵥�ʶ��ʻ�ɫ��
|
�������л�ѧ֪ʶ�����ϣ�����������������γ�ԭ��ķ�����̽����
��1�����������룺
��Һ�ʻ�ɫ���������ӷ�Ӧ��?�������ӷ���ʽ�����¡�
��Һ�ʻ�ɫ���������ӷ�Ӧ��?�������ӷ���ʽ�����¡�
��2�����ʵ�鲢��֤
Ϊ��֤����������ĸ�ԭ��������Һ���ɫ����Ʋ�����������ʵ�顣��������������Լ������к���ѡ�ã����ʵ�鷽��1�ͷ���2��
�Լ�
| ��̪��Һ��CCl4����ˮ�ƾ���KSCN��Һ
|
����
| ��������
| ʵ������
| ����
|
1
| ȡ������ɫ��Һ���Թ��У��μ�?����
| ��Һ���ɫ
| ��Ӧ?����
|
2
| ȡ������ɫ��Һ���Թ��У��μ�?����
| ________
________
|
��3��ʵ����ۣ�����ʵ�鲻����֤����Һ��Ƶ���ʵԭ��ͬʱ֤����Fe2+�Ļ�ԭ�Ա�Br��?���ǿ������������
��4��ʵ�鷴˼
I. ��������ʵ���Ʋ⣬�����廯������Һ�е���������ˮ���ټ���CCl4�������ֹ��������������?��
��. ��100 mLFeBr2��Һ��ͨ��2.24 L Cl2����״��������Һ����1/2��Br���������ɵ���Br2����ԭFeBr2��Һ��FeBr2�����ʵ���Ũ��Ϊ?��
�ο��𰸣���1��2Fe2+��Cl2=2Fe3+��2Cl����2Br����Cl2=Br2��2Cl��
��2��
����
��������
ʵ������
����
1
KSCN��Һ
?
��
2
CCl4
��Һ���������㣬�ϲ�Ϊ��ɫ���²�Ϊ��ɫ
�����������1����Ϊ�����������������Һ�о��Ի�ɫ�������������������������������ӣ������������������ɵ����塣���Է�Ӧ�����ӷ���ʽ�ֱ�Ϊ2Fe2+��Cl2=2Fe3+��2Cl����2Br����Cl2=Br2��2Cl����
��2�������Ӧ�����������ӣ������KSCN��Һ����ҺӦ���Ժ�ɫ��������ɵ��ǵ����壬�����������ȡ������֤��
��3���������ӵĻ�ԭ��ǿ�������ӵģ����������������������������ӡ�
��4�������ˮ��������������Ҳ���������ɵ����塣�������CCl4�������ֹ����ҺӦ���������㣬�ϲ�Ϊ��ɫ���²�Ϊ�Ⱥ�ɫ�����FeBr2�����ʵ�����xmol������ݵ�ʧ�����غ��֪x��1+2x��1/2��1��0.1��2�����x��0.1������Ũ����1mol/L��
�����Ѷȣ�һ��
4��ʵ���� Fe2O3��Cu2O���Ǻ�ɫ��ĩ�����������ϡ�ijУ��ѧʵ��С��ͨ��ʵ����̽��һ��ɫ��ĩ��Fe2O3��Cu2O�������̽���������£�
�������ϣ�Cu2O����ϡ��������Cu��CuSO4���ڿ����м�������CuO��
������裺?
����1����ɫ��ĩ��Fe2O3?
����2����ɫ��ĩ��Cu2O
��1������3��?
���̽��ʵ�飺
ȡ������ĩ��������ϡ�����У���������Һ���ٵμ� KSCN ��Һ��
��2��������1��������ʵ��������?��
��3�����μ� KSCN �Լ�����Һ�����ɫ����֤��ԭ�����ĩ��һ����������������������Ϊ����˵��������?��
�����������?��
��4���������ĩ��ȫ�ܽ�������� , �μ� KSCN �Լ�ʱ��Һ�����ɫ , ��֤��ԭ�����ĩ��?��д��������Ӧ�����ӷ���ʽ?��?��?��
̽�����죺��ʵ�������ȷ����ɫ��ĩΪFe2O3��Cu2O�Ļ���
��5�� ʵ��С�����ü��ȷ��ⶨCu2O������������ȡa g�����ĩ�ڿ����г�ּ��ȣ����������ٱ仯ʱ����������Ϊbg��b > a������������Cu2O����������Ϊ?��
�ο��𰸣���1������3����ɫ��ĩ��Fe2O3��Cu2O�Ļ���1�֣�
��2����Һ��ΪѪ��ɫ��1�֣�
��3��������? Cu�ܽ�Fe3+��ԭΪFe2+��2�֣�
��4��Fe2O3��Cu2O�Ļ����?
Fe2O3+6H+ = 2Fe3++3H2O? Cu2O+2H+ =" Cu" + Cu2+ + H2O
2 Fe3+ + Cu =" 2" Fe2+ + Cu2+��ÿ��1�֣���4�֣�
��5��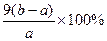 ��1�֣�
��1�֣�
�����������
�����Ѷȣ�һ��
5��ѡ���� ��1������ͼ��ʾ������������ͨ��ʢ�и�����ɫ�����Ĺ��ƿ��ʢ�г�ʪ��ɫ�����Ĺ��ƿ���ɹ۲쵽��������________________��
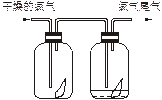
��2��Ϊ��ֹ����β����Ⱦ������������ˮ�����Ե����ʣ�����_____________��Һ���ն����������ԭ���ǣ��û�ѧ����ʽ��ʾ��__________________________��
������һԭ������ҵ�ϳ������۵�ʯ�������չ�ҵ����β���Ƶ�Ư�ۣ�Ư�۵���Ч�ɷ���___________���ѧʽ��������¶���ڿ����е�Ư�ۣ���ϡ����������������___________������ĸ�������
A��O2? B��Cl2? C��CO2? D��HClO
��3���ݡ���������������2004��4��15����16�գ�λ�������н���������ԭ�����ܳ���̷�������й©�ͱ�ը�¹ʡ��������߷���ʱ������9�����¹���ʧ��������3�����ˣ�15���˱�������ɢ�����������뱬ը�ֳ�ʱ�������ý���һ��Ũ�ȵ�ij�����ʵ�ˮ��Һ��ë����ס���ӣ������˲��õĸ�������_______��
A��NaOH? B��NaCl? C��KBr? D��Na2CO3
�ο��𰸣���1����ʪ����ɫ������ɫ��������ɫ��������ɫ?��2���������ƣ�NaOH��? 2NaOH+Cl2====NaClO+NaCl+H2O? Ca(ClO)2? C?��3��D
�����������
�����Ѷȣ�һ��