��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ƻ��֭������ϲ�������ϣ��������к����������ӣ���եȡ���������Ϊ�ػ�ɫ�������ϳ������м���ά����C�Է�ֹ���ɫ������������ά����C�� ��?��
A��������
B����ԭ��
C������
D������
2������� �ڵ��ʡ�������ᡢ�����ѡȡԭ����ȡFe��NO3��2��д���������з�Ӧ�Ļ�ѧ����ʽ����Ҫ�ظ�ͬһ��Ӧ���ͣ���
��1��______����2��______����3��______��
3������� ��15�֣���֪�������ӵĻ�ԭ����ǿ��˳��ΪI��>Fe2��>Br��������200 mL�����Һ�к�FeI2��FeBr2��0.10 mol����������ε�����ˮ(�ٶ�Cl2����ֻ���������ӷ�Ӧ��������������Ӧ)
��1������ˮ����0.15 mol Cl2����ԭ����������Һ�к��е���������Ҫ��________��ʣ��Fe2�������ʵ���Ϊ________��
��2����ԭ��Һ��Br����һ�뱻������������Cl2�����ʵ���Ϊ________��������������ҺΪ400 mL��������Ҫ�����Ӽ������ʵ���Ũ��Ϊ________��
��3��ͨ����������Ӧ�ķ��������ж�Cl2��I2��Fe3����Br2����������������������ǿ������˳����________________________��
��4��������Ӧ��ԭ��Һ����������ȫ�����������ٵ���������ˮ����I2ȫ����Cl2������HIO3(ǿ��)����д���˷�Ӧ�����ӷ���ʽ��_________________���������з�Ӧ������Cl2________mol��
4������� ����[CO(NH2)2]��һ�ַdz���Ҫ�ĸߵ�����,����Ȼ������H2S)Ϊԭ�Ϻϳ����ص���Ҫ��������ͼ��ʾ��ͼ��ijЩת������δ�г�����
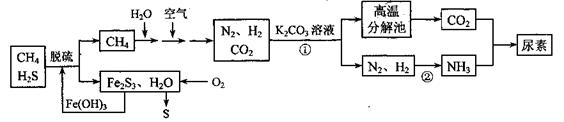
��ش��������⣺
��1����Ӧ�ٵ����ӷ���ʽ��______________
��2����Ȼ������������Fe2S3��H2O��02��Ӧ�Ļ�ѧ����ʽ��_______��
��3����Ӧ���Ƿ��ȷ�Ӧ���¶����ߣ��÷�Ӧ��ƽ�ⳣ��_______ (�� ����������С�� ���䡱)��H2NCOONH4(��������泥��Ǻϳ����ص��м��壬����̼ԭ�ӵ��ӻ����������_______�ӻ���
��4����������������������ɫ��ѧ���գ�������120t������������Ҫ?CH4___m3 (��״������
��5����ѧ�������о����ض���ȼ�ϵ�أ���ҺҲ�ܷ��磡�����ֵ��ֱ��ȥ�����з�ˮ�е����أ����ܲ���������ˮ���ܷ��硣����ȼ�ϵ�ؽṹ��ͼ��ʾ������ʱ�����ĵ缫��ӦʽΪ__________
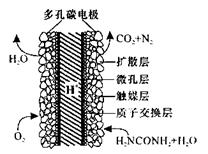
5��ѡ���� ���з�Ӧ�б�����뻹ԭ�����ܽ��е���
A��Fe2O3�� Fe
B��H2 �� H2O
C��HCl��FeCl2
D��Na ��NaOH