微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 1986年,人们成功的用如下反应制得了氟:
①2KMnO4+2KF+10HF+3H2O2=2K2MnF6+8H2O+3O2?
②K2MnF6+2SbF5=2KSbF6+MnF4?③2MnF4=2MnF3+F2↑。下列说法中正确的是
A.反应①、②、③都是氧化还原反应
B.反应①H2O2既是还原剂又是氧化剂
C.氧化性:KMnO4>O2
D.每生成1mol F2,上述反应共转移2mol电子
参考答案:C
本题解析:②中没有化合价变化,A错;①H2O2是还原剂,B错;D中每生成1mol F2,上述反应共转移8mol电子。
本题难度:一般
2、选择题 Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2和NO的体积相等时,实际参加反应的Cu2S与HNO3的物质的量之比为?(? )
A.1∶7
B.1∶5
C.1∶9
D.2∶9
参考答案:A
本题解析:根据NO2和NO的体积相等时,其方程式中的系数相等,根据得失电子守恒,可推出该反应的方程式为2Cu2S+14HNO3 = 2Cu(NO3)2+2CuSO4+5NO2↑+5NO↑+7H2O,所以实际参加反应的Cu2S与HNO3的物质的量之比为1∶7,故选A。
点评:本题考查氧化还原反应的内容,有一定难度,解答本题的关键是结合题意,根据反应中各个元素的化合价升降,推断得失电子情况,根据电子守恒,原子守恒,进一步推断出反应的方程式。
本题难度:一般
3、简答题 铝热反应不仅用于焊接钢轨,而且还常用于冶炼熔点较高的金属如钒、铬、锰等。
请配平下列用铝热反应冶炼金属钒和钴的化学方程式,指出哪些物质是还原剂、哪些物质是氧化剂,并计算生成1 mol各种金属分别需要纯铝的质量。
V2O5+Al――Al2O3+V? Co3O4+Al――Al2O3+Co
参考答案:3V2O5+10Al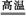 5Al2O3+6V 还原剂:Al 氧化剂:V2O5 生成1 mol V需要纯铝45 g
5Al2O3+6V 还原剂:Al 氧化剂:V2O5 生成1 mol V需要纯铝45 g
3Co3O4+8Al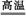 4Al2O3+9Co 还原剂:Al 氧化剂:Co3O4 生成1 mol Co需要纯铝24 g
4Al2O3+9Co 还原剂:Al 氧化剂:Co3O4 生成1 mol Co需要纯铝24 g
本题解析:根据原子守恒配平化学方程式,两个反应均为氧化还原反应,根据“所含元素化合价升高的物质是还原剂,所含元素化合价降低的物质是氧化剂”进行判断:
3V2O5+10Al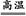 5Al2O3+6V
5Al2O3+6V
氧化剂 还原剂
3Co3O4+8Al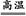 4Al2O3+9Co
4Al2O3+9Co
氧化剂 还原剂
根据化学方程式找到纯铝与生成金属之间的物质的量的关系:
10Al ~ 6V 8Al ~ 9Co
270 g 6 mol 216 g 9 mol
x 1 mol y 1 mol
列出比例式,解得x="45" g,y="24" g
即生成1 mol钒需要45 g纯铝,生成1 mol钴需要24 g纯铝。
本题难度:一般
4、计算题 验室常用浓盐酸与二氧化锰反应来制取氯气,反应的化学方程式4HCl+MnO2="=" MnCl2+2H2O+Cl2↑现用密度为1.1 9g/cm3、质量分数为36.5%的浓盐酸与二氧化锰反应,生成的氯气在标准状况下的体积为5.6L。计算:
(1)浓盐酸中HCl的物质的量浓度。
(2)需要消耗二氧化锰多少克?
(3)被氧化的HCl的物质的量是多少?
参考答案:(1)11.9 mol/L?(2)21.75g?(3)0.5 mol
本题解析:略
本题难度:简单
5、填空题 (17分)
I.(1)亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:
??Na2SO3+?KIO3+?H2SO4――?Na2SO4+?K2SO4+? I2+?H2O
①配平上面的氧化还原反应方程式,将计量数填在方框内。
②其中氧化剂是?,若反应中有5 mol电子转移,则生成的碘是?mol。
(2)0.3 mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ热量,乙硼烷燃烧热的热化学方程式为?。
II.含氰化物(有CN-)的废水危害大,CN-的含量为0.01mol/L~0.04mol/L就能毒 杀鱼类。其处理方法是用氧化法使其转化为低毒的氰酸钾(KCNO),氧化剂常用次氯酸盐;而生成的CNO-可进一步降解为能直接排放到空气中的无毒气体。近期研究将把某些导体的小粒悬浮在溶液中,在光的作用下,在小粒和溶液界面发生氧化还原反应。但小粒的质量和性质不发生变化,如二氧化钛(TiO2)小粒表面就可以破坏氰化物等有毒废物。
杀鱼类。其处理方法是用氧化法使其转化为低毒的氰酸钾(KCNO),氧化剂常用次氯酸盐;而生成的CNO-可进一步降解为能直接排放到空气中的无毒气体。近期研究将把某些导体的小粒悬浮在溶液中,在光的作用下,在小粒和溶液界面发生氧化还原反应。但小粒的质量和性质不发生变化,如二氧化钛(TiO2)小粒表面就可以破坏氰化物等有毒废物。
(1)二氧化钛在上述反应中的作用是?。
(2)CNO-经进一步处理后产生的两种无毒气体应该是?和?。
(3)若用NaClO溶液处理NaCN的废液,产生另外两种盐,其化学方程式为?。
参考答案:(共17分,(2)中热化学方程式3分,共余每空2分)
Ⅰ(1)①5? 2? 1? 5? 1? 1? 1
②KIO3? 0.5mol
(2)B2H6(g)+3O2(g)===B2O3(s)+3H2O(l);△H=-2165kJ/mol(3分)
Ⅱ(1)催化剂或催化作用
(2)CO2;N2
(3)NaClO+NaCN====NaCl+NaCNO
本题解析:略
本题难度:简单