微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合右图。则甲和X(要求甲和X能互换)不可能是
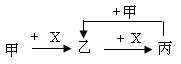
A.C和O2
B.SO2 和NaOH溶液
C.Cl2和Fe
D.CO2和石灰水
参考答案:C
本题解析: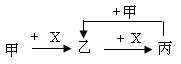
A.C和O2 ? 乙是CO2?丙是CO
?B.SO2 和NaOH溶液?乙是NaHSO3?丙是Na2SO3
C.Cl2和Fe 乙是FeCl3?,乙转化到丙时甲和X不能互换
D.CO2和石灰水?乙是CaCO3?丙是CaHCO3。故选C。
点评:本题考查的是物之间的转化,学生只要熟悉物质间的转化,此类问题应该就没有问题的。
本题难度:简单
2、填空题 (15分)A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,甲、乙、丙为常见化合物。它们之间有如下转化关系。请回答:
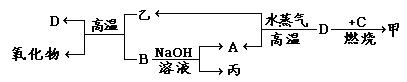
(1)工业上冶炼B的常用方法为______________(填字母)
a.电解法? b.热还原法? c.热分解法?
(2)丙的水溶液显?性(填酸或碱),原因是(用离子方程式表示)
? ??。
(3)D与甲溶液反应的化学方程式? ??。
(4)将C单质通入KI的碱性溶液中,可生成碘盐中的一种添加剂,试写出其反应的离子方程式:__________________________________________________。
(5)一定条件下,2molB与3molD的氧化物W恰好反应,则W的化学式??。
参考答案:
(1)a(2分)
(2)碱(2分); AlO2-+2H2O 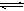 Al(OH)3+OH-(2分)
Al(OH)3+OH-(2分)
(3)Fe+2FeCl3=3FeCl2(3分)
(4)I-+6OH-+3 Cl2?=IO3-+6Cl-+3H2O(3分)
(5)FeO (2分)
本题解析:略
本题难度:一般
3、简答题 工业上生产高氯酸(沸点:90°C)时还同时生产了亚氯酸钠,其工艺流程如下:
(1)冷却过滤的目的______
(2)通入反应器2的SO2作用是______反应器2中发生反应的离子方程式为______
(3)循环使用的物质是______
(4)可以通过蒸馏滤液的方法得到高氯酸的原因可能是______
(5)通过电解NaClO3水溶液的方法也可以制备NaClO4,进而可以制备HClO4,写出阳极的电极反应式______.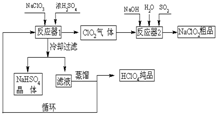
参考答案:(1)在反应器1中,硫酸钠和硫酸反应获得的硫酸氢钠的溶解度随着温度的降低而减小,这样冷却过滤,可以降低NaHSO4的溶解度并分离出NaHSO4晶体,故答案为:降低NaHSO4的溶解度并分离出NaHSO4晶体;
(2)在反应器2中,可以实现二氧化氯向NaClO2的转化,二氧化硫可以作为还原剂把ClO2还原为NaClO2,
即2ClO2+SO2+4OH-=2ClO2-+SO42-+2H2O,
故答案为:二氧化硫作为还原剂把ClO2还原为NaClO2;2ClO2+SO2+4OH-=2ClO2-+SO42-+2H2O;
(3)根据循环图可以发现硫酸作为反应物进入反应器1中,又作为生成物在反应器2中生成,可以循环使用,
故答案为:H2SO4;?
(4)根据题意高氯酸的沸点:90°C,可以采用蒸馏滤液的方法得到高氯酸,
故答案为:高氯酸的沸点比较低,容易从溶液中逸出;
(5)电解NaClO3水溶液的电解池中,阳极是ClO3-失电子发生氧化反应的过程,
即电极反应式为:H2O+ClO3--2e-=ClO4-+2H+,
故答案为:H2O+ClO3--2e-=ClO4-+2H+.
本题解析:
本题难度:一般
4、填空题 (8分)A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示。若A、B、C的焰色反应均呈黄色,水溶液均为碱性;将C加到盐酸中,有无色无味的气体X产生。

(1)写出A的电子式_____________。
(2)将X通入水玻璃溶液中,写出反应的离子方程式___________。
(3)自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100mL溶液,测得溶液中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为__________ g。
(4)写出区分B、C溶液的一种实验方案?
参考答案:(1)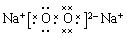 (2分)
(2分)
(2)2H2O+2CO2+SiO32--=H2SiO3↓+2HCO3-;或H2O+CO2+SiO32--=H2SiO3↓+CO32-(2分)
(3)2.65 g?(2分)
(4)合理即可?(2分)
本题解析:根据物质的性质可知,A是氢氧化钠,B是碳酸钠,C是碳酸氢钠,X是CO2。
(1)氢氧化钠中还原离子键和极性键,电子式为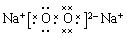 。
。
(2)碳酸的酸性强于硅酸的,所以方程式为2H2O+2CO2+SiO32--=H2SiO3↓+2HCO3-;或H2O+CO2+SiO32--=H2SiO3↓+CO32-。
(3)碳酸氢钠加热分解生成碳酸钠,根据钠原子守恒可知,最终碳酸钠的质量是0.1L×0.5mol/L÷2×106g/mol=2.65g。
(3)碳酸钠能和氯化钙反应生成碳酸钙沉淀,而碳酸氢钠不能,据此可以鉴别。
本题难度:一般
5、填空题 现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
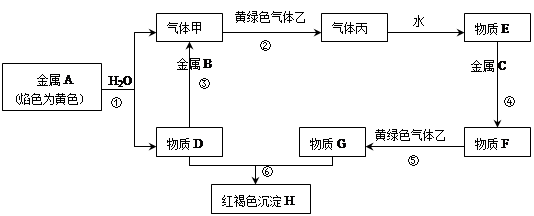
请回答下列问题:
(1)写出下列物质的化学式:B?、丙?、乙?。
(2)写出下列反应的化学方程式:
反应①?;
反应⑤?;
反应⑥??。
参考答案:(1) Al? HCl? Cl2[
(2) ① 2Na+2H2O=2NaOH+H2↑
⑤2FeCl2+Cl2=2FeCl3?
⑥3NaOH+FeCl3=Fe(OH)3↓+3NaCl
本题解析:由金属A焰色反应为黄色知A为钠,则甲为氢气,D为氢氧化钠,B为铝,乙为黄绿色气体,则乙为氯气,丙为氯化氢,E为稀盐酸,H为黄褐色沉淀氢氧化铁,所以C为铁,F为氯化亚铁,G为氯化铁。所以,(1)B:Al、乙:Cl2、丙:HCl;
(2)反应①的方程式:2Na+2H2O=2NaOH+H2↑
反应⑤方程式:2FeCl2+Cl2=2FeCl3
反应⑥方程式:3NaOH+FeCl3=Fe(OH)3↓+3NaCl
本题难度:一般