微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组离子中,在溶液中能够大量共存的一组是( )
A.A1O2-、SO42-、OH-、K+
B.Al3+、Na+、OH-、Cl-
C.Fe3+、NH4+、SO42-、SCN-
D.OH-、C1-、Na+、HCO3-
参考答案:A.该组离子之间不反应,能共存,故A正确;
B.因Al3+、OH-能结合生成沉淀,则不能共存,故B错误;
C.因Fe3+、SCN-能结合生成络离子,则不能共存,故C错误;
D.因OH-、HCO3-能结合生成水和碳酸根离子,则不能共存,故D错误;
故选A.
本题解析:
本题难度:一般
2、选择题 下列叙述正确的是?
A.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,
溶质浓度大小关系是:c[(NH4)2Fe(SO4)2] < c[(NH4)2SO4] < c(NH4Cl)
B.向AgCl悬浊液中滴入KI溶液,有AgI沉淀生成,说明AgCl的溶解度小于AgI
的溶解度
C.0.2 mol?L-1盐酸与等体积0.05 mol?L-1Ba(OH)2溶液混合后,溶液的pH=1
D.0.2 mol?L-1的NaHCO3溶液中c(H+)+c(H2CO3)=2c(CO32-)+c(OH-)
参考答案:A
本题解析:A、(NH4)2Fe(SO4)2溶液,铵根离子和亚铁离子水解相互抑制,且电离出两个铵根,故浓度最小。
B、沉淀始终朝着溶解度小的方向进行;
C、中和后,c(H+)=0.05mol/L;
D、电荷守恒:c(H+)+c(Na+)=2c(CO32-)+c(OH-)+ c(HCO3-)
物料守恒:c(Na+)=c(CO32-)+c(H2CO3)+ c(HCO3-);二者相减
c(H+)+c(H2CO3)=c(CO32-)+c(OH-)
本题难度:简单
3、选择题 在下述条件下,一定能大量共存的离子组是
[? ]
A.强酸性溶液中:K+ 、Ba2+、I-、MnO4-
B.含有大量NO3-的水溶液中:NH4+、Fe2+、SO42-、H+
C.c(HCO3-)=0.1mol・L-1的溶液中:Na+、K+、CO32-、Br-
D.强碱性溶液中:[Al(OH)4]-、HCO3-、Na+、Ca2+
参考答案:C
本题解析:
本题难度:一般
4、填空题 最近雾霾天气肆虐我国大部分地区。其中SO2是造成空气的污染的主要原因,利用钠碱循环法可除去SO2。
(1)钠碱循环法中,吸收液为Na2SO3溶液,该反应的离子方程式是________。
(2)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7;H2CO3的电离常数为K1=4.30×10-7,K2=5.60×10-11,则下列微粒可以大量共存的是______(填序号)。
A.CO32- HSO3-? B. HCO3-? HSO3-? C. SO32-? HCO3-? D. H2SO3? HCO3-
(3)吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
n(SO32-):n(HSO3-)
| 91:9
| 1:1
| 1:91
|
pH
| 8.2
| 7.2
| 6.2
|
?
①根据上表判断NaHSO3溶液显_______性,试解释原因__________________________;
②在NaHSO3溶液中离子浓度关系不正确的是_______(填序号)。
A.c(Na+)=2c(SO32-)+c(HSO3-)
B.c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
C.c(H2SO3)+ c(H+)=c(SO32-)+c(OH-)
D.c(Na+)+ c(H+)=2c(SO32-)+ c(HSO3-)+ c(OH-)
(4)当吸收液的pH降至约为6时,需送至电解槽处理,直至得到pH>8的吸收液再循环利用,电解示意图如下:
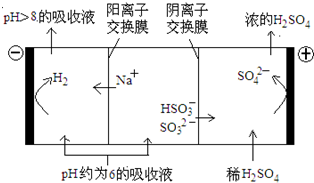
①写出阳极上发生的电极反应式____________;
②当电极上有1mol电子转移时阴极产物的质量为__________。
参考答案:(1)SO32-+SO2+H2O=2HSO3-(1分)
(2)BC(2分,全对得2分,有错不得分,选不全得1分)
(3)①酸(1分);在亚硫酸氢钠溶液中HSO3-存在电离平衡:HSO3- SO32-+H+和水解平衡HSO3-+H2O
SO32-+H+和水解平衡HSO3-+H2O H2SO3+OH-,HSO3-的电离程度强于水解程度,故溶液呈酸性(2分)②A(1分)
H2SO3+OH-,HSO3-的电离程度强于水解程度,故溶液呈酸性(2分)②A(1分)
(4)①HSO3-+H2O-2e-=SO42-+3H+(2分)②1g(1分)
本题解析:(1)亚硫酸是二元弱酸,其正盐能吸收SO2转化为酸式盐,所以钠碱循环法中,吸收液为Na2SO3溶液时反应的离子方程式为SO32-+SO2+H2O=2HSO3-。
(2)弱酸的电离常数越大,酸性越强,则根据H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7和H2CO3的电离常数为K1=4.30×10-7,K2=5.60×10-11可知,酸性强弱顺序是H2SO3>H2CO3>HSO3->HCO3-。根据较强的酸制备减弱的酸可知,CO32-与HSO3-反应生成HCO3-和SO32-,不能大量共存;H2SO3与HCO3-反应生成CO2和HSO3-,不能大量共存。而HCO3-与HSO3-、SO32-与HCO3-均可以大量共存,答案选BC。
(3)①由于SO32-只能水解,溶液显碱性,所以根据n(SO32-):n(HSO3-)=1:91时溶液显酸性可知,NaHSO3溶液显酸性。这是由于在亚硫酸氢钠溶液中HSO3-存在电离平衡:HSO3- SO32-+H+和水解平衡HSO3-+H2O
SO32-+H+和水解平衡HSO3-+H2O H2SO3+OH-,HSO3-的电离程度强于水解程度,故溶液呈酸性。
H2SO3+OH-,HSO3-的电离程度强于水解程度,故溶液呈酸性。
②根据物料守恒可知,c(Na+)=c(SO32-)+c(HSO3-)+ c(H2SO3),A不正确;B、由于HSO3-的电离程度强于水解程度,且均是很弱的,所以溶液中c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-),B正确;C、根据电荷守恒可知c(Na+)+ c(H+)=2c(SO32-)+ c(HSO3-)+ c(OH-)和物料守恒可知c(Na+)=c(SO32-)+c(HSO3-)+ c(H2SO3),溶液中c(H2SO3)+ c(H+)=c(SO32-)+c(OH-),C正确;D、符合电荷守恒c(Na+)+ c(H+)=2c(SO32-)+ c(HSO3-)+ c(OH-),D正确,答案选A。
(4)①电解池中阳极与电源的正极相连,失去电子,发生氧化反应。根据装置可知阳极有硫酸生成,由于溶液的pH=6,溶液中主要是以HSO3-存在,所以阳极主要是HSO3-放电,因此阳极上发生的电极反应式为HSO3-+H2O-2e-=SO42-+3H+。
②电解池中阴极得到电阻,则根据装置可判断阴极是溶液中的氢离子放电生成氢气,电极反应式为2H++2e-=H2↑。当电极上有1mol电子转移时阴极得到0.5mol氢气,所以阴极产物的质量为0.5mol×2g/mol=1g。
本题难度:困难
5、选择题 常温下,下列各组离子在指定溶液中一定能大量共存的是
A.1.0mol・L-1的KNO3溶液:Cl-、SO42-、H+、Fe2+
B.c(H+)=1.0×10-12mol・L-1的溶液:K+、Na+、CH3COO-、Br-
C.甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl-
D.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、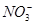
参考答案:B
本题解析:Fe2+在酸性条件下被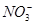 氧化而不能共存;甲基橙呈红色的溶液显酸性,则
氧化而不能共存;甲基橙呈红色的溶液显酸性,则 不能存在;与铝粉反应产生氢气的溶液可以是酸溶液,
不能存在;与铝粉反应产生氢气的溶液可以是酸溶液,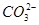 不能存在或碱溶液,因此选B。
不能存在或碱溶液,因此选B。
本题难度:一般