��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ�������£������ܱ������н��еĿ��淴ӦA��g��+3B��g��?

2C��g��������˵���У���˵����һ��Ӧ�Ѿ��ﵽ��ѧƽ��״̬���ǣ�������
A����λʱ������nmolA��ͬʱ����3nmolB
B��A��B��C��Ũ�����
C������C��������C�ֽ���������
D��A��B��C�ķ�����֮��Ϊ1��3��2
�ο��𰸣�A�����۷�Ӧ�Ƿ�ﵽƽ��״̬���淴Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�����˵���ﵽƽ��״̬����A����
B�������ڸ����ʵ�Ũ�Ȳ���ʱ��仯����˵���ﵽƽ��״̬����A��B��C��Ũ�Ȳ�һ����ȣ���B����
C������C��������C�ֽ��������ȣ�˵����Ӧv��=v�棬�ﵽƽ��״̬����C��ȷ��
D����Ӧ�ﵽƽ��ʱ��Ũ���뷴Ӧ�ij�ʼ���ʵ����Լ���Ӧ��ת���̶��йأ�����ȷ���Ƿ�ﵽƽ�⣬��D����
��ѡC��
���������
�����Ѷȣ���
2��ѡ���� ��֪N2��g��+3H2��g�� 2NH3��g��������һ�ܱ������г���1molN2��3molH2���ڸ��¡���ѹ�ʹ������������·�����Ӧ�������й�˵����ȷ���ǣ�������
2NH3��g��������һ�ܱ������г���1molN2��3molH2���ڸ��¡���ѹ�ʹ������������·�����Ӧ�������й�˵����ȷ���ǣ�������
A�����տ�������2molNH3
B���ﵽ��ѧƽ��״̬ʱ������Ӧ���淴Ӧ�����ʶ�Ϊ0
C���ﵽ��ѧƽ��״̬ʱ��������N2��H2��NH3�����ʵ���֮��Ϊ1��3��2
D���ﵽ��ѧƽ��״̬ʱ��N2��H2��NH3�����ʵ���Ũ�Ȳ��ٱ仯
�ο��𰸣�A����ӦΪ���淴Ӧ����Ӧ�ﲻ����ȫת������A����
B���ﵽ��ѧƽ��״̬ʱ������Ӧ���淴Ӧ��ȵ���Ϊ0����B����
C����Ӧ�����������ȷ������Ӧ���ת���ʲ�ȷ��������ȷ��ƽ��ʱ�����ʵ����ʵ�����ϵ����C����
D�����ﵽ��ѧƽ��״̬ʱ�������ʵ�Ũ�Ȳ��ٸı䣬��D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
3������� ��8�֣����ܱ������У�ʹ2molN2��6molH2��Ϸ������з�Ӧ��
N2��g��+3H2��g��===2NH3��g��������ӦΪ���ȷ�Ӧ��
��1������Ӧ�ﵽƽ��ʱ��N2��H2��Ũ�ȱ���_______��N2��H2��ת���ʱ���_________��
��2������ƽ����ϵ���¶ȣ�����������䣩����������ƽ����Է�������_______���ܶ�________������������С�����䡱 ��
��3�����ﵽƽ��ʱ����C��N2����C��H2����C��NH3��ͬʱ��Сһ����ƽ�⽫��______�ƶ���
��4�����ﵽƽ��ʱ�����������������ѹǿ���䣬ƽ�⽫��_________�ƶ���
��5�����������ݣ����ȡ�����ʹ�������¶�Ѹ������ԭ����2����ƽ�⽫_______
��������ƶ����������ƶ������ƶ��������ﵽ��ƽ����������¶�_______������ڡ���С�ڡ����ڡ���ԭ����2����
�ο��𰸣���1��1 : 3 ;? 1 : 1
��2����������
��3���淴Ӧ����
��4���淴Ӧ����
��5�������ƶ���С��
�����������
�����Ѷȣ���
4��ѡ���� ��һ�������µĺ����ܱ������з�����Ӧ��CO2(g)��3H2(g)  CH3OH(g)��H2O(g)��ͼ1��ʾ��Ӧ�����������ı仯��ͼ2��ʾ��Ӧ����������Ũ�ȵı仯�������й�˵����ȷ����
CH3OH(g)��H2O(g)��ͼ1��ʾ��Ӧ�����������ı仯��ͼ2��ʾ��Ӧ����������Ũ�ȵı仯�������й�˵����ȷ����

A���÷�Ӧ���ʱ���ر䣺��H��0����S��0
B���¶Ƚ��ͣ��÷�Ӧ��ƽ�ⳣ��K����
C�������¶ȣ�n(CH3OH)/n(CO2)����
D���ӷ�Ӧ��ʼ��ƽ�⣬��������ʾ��ƽ����Ӧ����Ϊ2.25 mol/(L��min)
�ο��𰸣�B
����������÷�Ӧ�Ƿ��ȷ�Ӧ����H��0����������ʵ������٣���S��0��A�����¶Ƚ��ͣ�ƽ�������ƶ���ƽ�ⳣ������B��ȷ�������¶ȣ�ƽ�������ƶ���n(CH3OH)/n(CO2)��С��C�����ӷ�Ӧ��ʼ��ƽ�⣬v(CO2)�� ��0.075 mol/(L��min)��v(H2)��3v(CO2)��0.225 mol/(L��min)��D����
��0.075 mol/(L��min)��v(H2)��3v(CO2)��0.225 mol/(L��min)��D����
�����Ѷȣ�һ��
5������� ��������̼��̼�Ļ���������������ʵ����Ӧ�ù㷺��
(1)��2�����ܱ������У�����2mol CO��4mol ˮ�������ڴ��������½������»�ѧ��Ӧ��CO(g)+H2O(g) CO2(g)+H2(g)��CO��ת���ʺ��¶�t�Ĺ�ϵ���±���
CO2(g)+H2(g)��CO��ת���ʺ��¶�t�Ĺ�ϵ���±���
t(��)
| 750
| 850
| 1000
|
CO%
| 0.7
| 2/3
| 0.5
|
?
1000��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ___________________��850��ʱ���������������ͨ��1mol CO��1.5mol H2O��0.5mol CO2��2molH2����ʱ��Ӧ___________(����ҽ��С�����������С�����ƽ��״̬��)��
(2)��֪��C(s)��O2 (g) ===CO2(g) ��H1=��393.5kJ��mol��1
2H2(g)��O2(g)===?2H2O(g) ��H2=��483.6kJ��mol��1
C(s)��H2O(g)===?CO(g)��H2(g) ��H3=+131.3kJ��mol��1
��CO��H2O����CO2��H2���Ȼ�ѧ����ʽΪ_______________________________��
(3) Ŀǰ��ҵ�Ͽ���CO2������ȼ�ϼ״����йط�ӦΪ��
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ��H��-49.0 kJ��mol��1���������Ϊ1 L���ܱ������У�����
CH3OH(g)+H2O(g) ��H��-49.0 kJ��mol��1���������Ϊ1 L���ܱ������У�����
1mol CO2��3mol H2����Ӧ�����в��CO2��CH3OH(g)��Ũ����ʱ��ı仯��ͼ��ʾ��
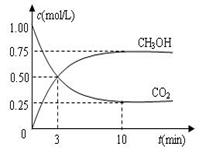
�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)��_____________��
�����ı�����ʹƽ��������Ӧ�����ƶ�����ƽ�ⳣ��______________(�����)
a�����ܲ���?b�����ܼ�С ?c���������� ?d�����䡢��С��������п���
(4)NaHCO3��ˮ��Һ�ʼ��ԣ���ԭ����(����������)_______________________�������£���100mL
0.2mol/LNaHCO3��Һ�еμ�amol/L�Ĵ�����Һ�����μӵ���Һ������ʱ������ȥ�Ĵ�������պ�Ҳ
Ϊ100mL����ʱ����ĵ��볣��Ϊb�� �ú�b�Ĵ���ʽ��ʾ�����Ũ��a=_____________________��
�ο��𰸣�(14�֣�ÿ��2��) (1)1/3�����ҽ���? (2)CO(g)+H2O(g)��CO2(g)+H2(g)?��H����41.2 kJ/mol
(3)��0.225mol��L��1��min��1(��λ����ֵ��1��)?��ac(��һ����1�֣���һ������1��)
(4)HCO3��ˮ��̶ȴ��������̶ȡ�
a��0.2(10��7+b)/b��a��(10��7��b)/5b(������ʾ��ʽ��ֻҪ��ȷ������)
�����������1��? CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
��ʼŨ�ȣ�mol/L��? 1? 2? 0? 0
ת��Ũ�ȣ�mol/L��? 0.5? 0.5? 0.5? 0.5
ƽ��Ũ�ȣ�mol/L��? 0.5? 1.5? 0.5? 0.5
��Ϊ��ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ�Ӧ�Ļ�ѧ����ʽ��֪���÷�Ӧ��ƽ�ⳣ��K��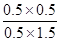 ��
��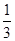 �����ݱ������ݿ�֪�������¶ȣ�CO��ת���ʽ��͡���˵�������¶�ƽ�����淴Ӧ�����ƶ������ƽ�ⳣ����С������850��ʱ��ƽ�ⳣ������
�����ݱ������ݿ�֪�������¶ȣ�CO��ת���ʽ��͡���˵�������¶�ƽ�����淴Ӧ�����ƶ������ƽ�ⳣ����С������850��ʱ��ƽ�ⳣ������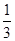 ��850��ʱ���������������ͨ��1mol CO��1.5mol H2O��0.5mol CO2��2molH2����ʱQ��
��850��ʱ���������������ͨ��1mol CO��1.5mol H2O��0.5mol CO2��2molH2����ʱQ��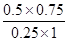 ��
�� �����Է�Ӧ���ҽ��С�
�����Է�Ӧ���ҽ��С�
��2�������Ȼ�ѧ����ʽ��C(s)��O2 (g) ===CO2(g) ��H1=��393.5kJ��mol��1����2H2(g)��O2(g)===?2H2O(g) ��H2=��483.6kJ��mol��1����C(s)��H2O(g)===?CO(g)��H2(g) ��H3=+131.3kJ��mol��1�����ݸ�˹���ɿ�֪�٣��ڣ��ۼ��õ�CO(g)+H2O(g)=CO2(g)+H2(g)����÷�Ӧ�ķ�Ӧ�ȡ�H����393.5kJ/mol��483.6kJ/mol��131.3kJ/mol����41.2 kJ/mol��
��3���ٸ���ͼ���֪����Ӧ���е�10minʱ����Ӧ�ﵽƽ��״̬����ʱ���ɼ״���Ũ����0.75mol/L������ݷ���ʽ��֪������������Ũ����0.75mol/L��3��2.25mol/L�����������ķ�Ӧ����v(H2)��2.25mol/L��10min��0.225mol��L��1��min��1��
������¶Ȳ��䣬�ı�����ʹƽ��������Ӧ�����ƶ�����ƽ�ⳣ�����䣻��������Ӧ�Ƿ��ȷ�Ӧ����˽����¶�ƽ��������Ӧ������У�ƽ�ⳣ�����������ȷ�Ĵ�ѡac��
��4������HCO3����ˮ��̶ȴ���HCO3���ĵ���̶ȣ�����̼��������Һ�Լ��ԡ����������ǿ��̼�����Ƶģ���˷�Ӧ����CO2�������ɡ����ݵ���غ��֪c(Na��)��c(H��)��c(OH��)��c(CH3COO��)����Һ�����ԣ���c(H��)��c(OH��)��10��7mol/L������c(CH3COO��)��c(Na��)��0.2mol/L��2��0.1mol/L��������Һ��c(CH3COOH)��0.5amol/L��c(CH3COO��)��0.5amol/L��0.1mol/L�����Ը��ݵ���ƽ�ⳣ������ʽ��֪b��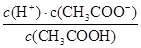 ����b��
����b�� �����a��
�����a��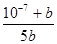 ��
��
�����Ѷȣ�һ��