微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 为确定HCl、H2CO3、H2SiO3的酸性强弱,某同学设计了如图所示的装置,一次实验即可达到目的(不必选其他酸性物质)。请据此回答
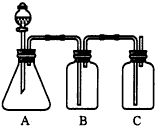
(1)锥形瓶中装某可溶性正盐溶液,分液漏斗所盛试剂应为_______________。
(2)装置B所盛的试剂是___________,其作用是________________。
(3)装置C所盛试剂是____________,C中反应的离子方程式是___________________。
2、填空题 (15分)某矿样含有大量的CuS、少量铁的氧化物及少量其它不溶于酸的杂质。某化学课外小组设计以下流程,取该矿样为原料生产CuC12・2H2O 晶体。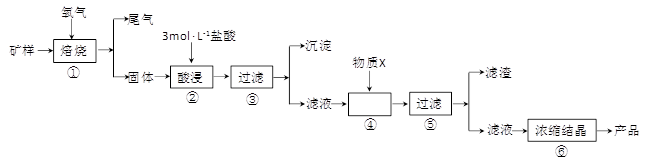
已知:常温下,金属离子开始沉淀和沉淀完全时的pH 见下表。
金属离子
| 氢氧化物开始沉淀的pH
| 氢氧化物沉淀完全的pH
|
Fe2+
| 7.0
| 9.0
|
Fe3+
| 1.9
| 3.2
|
Cu2+
| 4.7
| 6.7
|
回答下列问题:
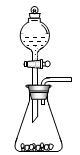
(l)步骤①的焙烧过程中需要通入氧气。在实验室中,可使用常见化学物质利用上图所示装置制取氧气,试写出熟悉的符合上述条件的两个化学方程式:______________________、______________________。
(2)焙烧产生的尾气中含有的一种气体是形成酸雨的污染物,若将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:____________________、__________________。
(3)步骤②酸浸过程中,需要用到3 mol ・ L-1的盐酸100 mL,配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有_______________________________________。
(4)步骤④加入物质X的目的是_________________________________________,物质X 可以选用下列物质中的______________________。
(A)氢氧化钠?(B)稀盐酸?(C)氨水?(D)氧化铜
(5)当溶液中金属离子浓度低于1×10-5 mol ・ L-1时,认为该金属离子沉淀完全,则Ksp[Fe(OH)2]=_____。
3、实验题 已知某混合金属粉末中,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上。请设计合理实验,探究该混合金属粉末中铁、铜元素的存在。
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1 mol/L硫酸、2 mol/L硝酸、2 mol/LNaOH溶液、 20%KSCN溶液。
完成以下实验探究过程:
(1)提出假设
假设1该混合金属粉末中除铝外还含有____________元素。
假设2该混合金属粉末中除铝外还含有_______________元素。
假设3该混合金属粉末中除铝外还含有Fe、Cu元素。
设计实验方案
基于假设3,设计出实验方案。
(2)实验过程
根据上述的实验方案,叙述实验操作、预期现象和结论。
4、实验题 实验室利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
4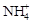 ?+ 6HCHO = 3H++ 6H2O + (CH2)6N4H+
?+ 6HCHO = 3H++ 6H2O + (CH2)6N4H+
然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行如下实验:
[滴定时,1 mol (CH2)6N4H+与1 mol H+相当]
步骤Ⅰ:称取样品1.500 g
步骤Ⅱ:将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀
步骤Ⅲ:移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1-2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次
步骤Ⅳ:实验数据记录
<若NaOH标准溶液的浓度为0.1010 mol/L>
滴定次数
| 待测液的体积(mL)
| 标准溶液的体积
|
滴定前刻度(mL)
| 滴定后刻度(mL)
|
1
| 25.00
| 1.02
| 21.03
|
2
| 25.00
| 2.00
| 21.99
|
3
| 25.00
| 0.20
| 20.20
|
根据上述实验步骤填空:
(1)滴定操作时,眼睛应观察?
(2)滴定终点的判断方法是?
(3)锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积?(填“偏大”、“偏小”或“无影响”)
(4)碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数?(填“偏大”、“偏小”或“无影响”)
(5)配制样品溶液及滴定实验中所需的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒、滴定管外,还有?(填仪器名称)
该样品中氮的质量分数为?
5、填空题 碘是人体必需的微量元素之一,有“智力元素”之称.食用加碘食盐可预防碘缺乏病.查阅资料知:①在酸性条件下,I-能被NO3-离子氧化成IO3-离子,被H2O2或O2等氧化成I2;②IO3-离子能被HSO3-离子还原成I2.
请你利用实验室常用仪器和下列限选试剂,依次研究某食盐样品中所加碘的存在形式是I2、I-、IO3-中的哪一种.
限选试剂如下:1.0mol?L-1HNO3溶液、1.0mol?L-1?H2SO4溶液、1.0mol?L-1NaHSO3溶液、3%?H2O2溶液、1%淀粉溶液、蒸馏水
Ⅰ.提出假设
假设1:该食盐样品中含I2;?假设2:该食盐样品中含I-
假设3:______.
Ⅱ.设计方案与实验探究
将适量食盐样品溶于蒸馏水制成溶液,请按要求填写下表
| 实验步骤 | 预期现象与结论
步骤1:取少量上述溶液注入试管中,滴入几滴淀粉溶液振荡.
若溶液显______,则假设1成立;否则,假设1不成立,再进行步骤2
步骤2:______
______
______
若溶液显蓝色,则假设2成立,反应的离子方程式为______;否则,假设2不成立,再进行步骤3
步骤3:______
______
______
______
______
|
Ⅲ.问题与思考
纯的KIO3或KI都可以作为食用加碘盐中碘的来源.从化学角度来看,试验中添加______(填“KIO3”或“KI”)更好;理由是______.