��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��100��ʱ����0.200 mol�������������������2L��յ��ܱ������У�ÿ��һ��ʱ��Ը����������ʵ�Ũ�ȣ�mol/L�����з������õ����±���
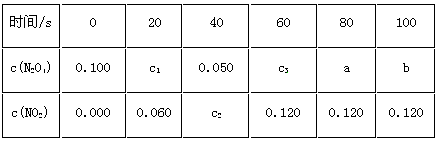
����գ�
��1���÷�Ӧ�Ļ�ѧ����ʽΪ_____________���ﵽƽ��ʱ������������ת����Ϊ______%��
��2��20sʱ������������Ũ��c1=________mol��L-1����0��20sʱ����ڣ�������������ƽ����Ӧ����Ϊ________mol��L-1��s-1��
��3��������ͬ���������������г�����Ƕ����������壬Ҫ�ﵽ����ͬ����ƽ��״̬�����������ij�ʼŨ��Ϊ________mol��L-1��
�ο��𰸣���1��N2O4 2NO2��60
2NO2��60
��2��0.070��0.0015
��3��0.2
���������
�����Ѷȣ�һ��
2������� ��֪���淴Ӧ:A(g)��B(g) C(g)��D(g)?��H��0����ش���������:
C(g)��D(g)?��H��0����ش���������:
(1)��ij�¶��£���Ӧ�����ʼŨ�ȷֱ�Ϊ:c(A)="1" mol/L��c(B)="2.4" mol/L���ﵽƽ��ʱ��A��ת����Ϊ60%����ʱB��ת����Ϊ?��
(2)����Ӧ�¶Ƚ��ͣ���B��ת���ʽ�?(���������С�����䡱)��
(3)����Ӧ�¶Ȳ��䣬��Ӧ�����ʼŨ�ȷֱ�Ϊc(A)="4" mol��L-1��c(B)=" a" mol��L-1���ﵽƽ���c(C)="2" mol��L-1����a=?��
(4)����Ӧ�¶Ȳ���,��Ӧ�����ʼŨ�ȷֱ�Ϊc(A)="c(B)=b" mol/L���ﵽƽ���c(D)=?��(������λ��Ч����)
�ο��𰸣�(1)25%? (2)����? (3)6? (4)0.41b mol/L
���������(1)����A��ת���ʿ�֪��ת��A��Ũ��Ϊ0.6 mol��L-1��ת��B��Ũ��ҲΪ0.6 mol��L-1��B��ת����Ϊ0.6 mol��L-1/2.4 mol��L-1��100%=25%��
(2)��Ϊ����ӦΪ���ȷ�Ӧ�����Խ����¶ȣ�ƽ��������Ӧ�����ƶ���B��ת��������
(3)����ƽ��ʱC��Ũ�ȿ�֪���ﵽƽ��ʱA��B��C��D�����ʵ�Ũ�ȷֱ�Ϊ2 mol��L-1��(a��2) mol��L-1��2 mol��L-1��2 mol��L-1������(1)��֪���¶��µ�ƽ�ⳣ��ΪK=(0.6��0.6)/(0.4��1.8)=0.5������2��2/��2��(a��2)��=0.5�����a=6��
(4)��ﵽƽ���c(D)=x,
��? A(g)+B(g) C(g)+D(g)
C(g)+D(g)
��ʼmol/L? b? b? 0? 0
ƽ��mol/L? b-x b-x? x? x
��K=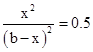
���x��0.41b mol/L
�����Ѷȣ�һ��
3��ѡ���� һ���¶��£���2L�����ܱ������з�����Ӧ��2N2O5(g)  4NO2(g)+ O2(g)����H��0.��Ӧ��Ͳ�������������ʵ����淴Ӧʱ��仯��������ͼ��ʾ������˵����ȷ����
4NO2(g)+ O2(g)����H��0.��Ӧ��Ͳ�������������ʵ����淴Ӧʱ��仯��������ͼ��ʾ������˵����ȷ����

A��10minʱ����Ӧ�ﵽƽ��
B�����¶��·�Ӧ��ƽ�ⳣ��Ϊ8
C��0~20min��ƽ����Ӧ����v(N2O5)=0.05mol?L-1?min-1
D������a��ʾNO2�����ʵ����淴Ӧʱ��ı仯
�ο��𰸣�CD
���������A�����������ʾ��20minʱ����Ӧ�ﵽƽ�⣬�ʴ���B����¶��·�Ӧ��ƽ�ⳣ��Ӧ��Ϊ32/9���ʴ�����ѡCD��
���������⿼�黯ѧƽ��ͼ�����⣬��Ŀ�ѶȽϴ���ע�����ͼ�����ʵ����ı仯�������״�������ʱע��˼����
�����Ѷȣ�һ��
4��ѡ���� ��һ���¶��£���a L�ܱ������м���1mol X�����2 mol Y���壬�������·�Ӧ��
X��g����2Y��g�� 2Z��g�����˷�Ӧ�ﵽƽ��ı�־�� (? )
2Z��g�����˷�Ӧ�ﵽƽ��ı�־�� (? )
A������������ƽ��Ħ����������
B�������ڸ����ʵ�Ũ�����
C��������X��Y��Z��Ũ��֮��Ϊ1�U2�U2
D����λʱ������0.1mol Xͬʱ����0.2mol Z
�ο��𰸣�A
������������ڷ�ӦX��g����2Y��g�� 2Z��g����Ӧǰ��ƽ��Ħ�����������ı䣬�����жϴ�ƽ�⣬A����ȷ�������÷�Ӧ�и����ʵ�Ũ�ȹ�ϵ���ж�ƽ�⣬B��C�����λʱ��������0.1molXͬʱ����0.2molZ��ֻ������Ӧ����û���淴Ӧ���ʣ������ж�ƽ�⣬D�����ѡA��
2Z��g����Ӧǰ��ƽ��Ħ�����������ı䣬�����жϴ�ƽ�⣬A����ȷ�������÷�Ӧ�и����ʵ�Ũ�ȹ�ϵ���ж�ƽ�⣬B��C�����λʱ��������0.1molXͬʱ����0.2molZ��ֻ������Ӧ����û���淴Ӧ���ʣ������ж�ƽ�⣬D�����ѡA��
�������жϻ�ѧ��Ӧ��ƽ�������ֱ�ӱ�־��v(��)=v(��)�������Ũ�Ȳ��ٷ����ı����ж��⣬�������ü�ӱ�־������Ӧǰ��ı仯�����ٷ����ı����жϡ�
�����Ѷȣ���
5��ѡ���� �����ͬ�ļס��������������ֱ��е����ʵ�����SO2��O2������ͬ�¶��·�����Ӧ��
2SO2��g��+O2��g�� 2SO3��g�������ﵽƽ�⣬�ù����У�����������������䣬����������ѹǿ���䣬����������SO2��ת����ΪP��������������SO2��ת����
2SO3��g�������ﵽƽ�⣬�ù����У�����������������䣬����������ѹǿ���䣬����������SO2��ת����ΪP��������������SO2��ת����
[? ]
A������P��
B������P��
C����P%
D�����ж�
�ο��𰸣�B
���������
�����Ѷȣ�һ��