微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 (6分)铜是生命必需的元素,也是人类最早使用的金属之一,铜的生产和使用对国计民生各个方面产生了深远的影响。在化学反应中,铜元素可表现为0价、+1价、+2价。
(1)在西汉古籍中曾有记载:曾青得铁则化为铜〔即:曾青(CuSO4)跟铁反应生成铜〕,试写出该反应的离子方程式:____________________________________。
(2)尽管铜比铁较为稳定,但铜器表面经常会生成铜锈〔即:铜绿,化学式Cu2(OH)2CO3〕,其中生成铜绿的反应物除铜外还有O2、CO2和H2O。试写出保护铜制品的方法:________________________________________。
(3)铜钱在历史上曾经是一种广泛流通的货币。试从物理性质和化学性质的角度分析为什么铜常用于制造货币。(铜的熔点是1 183.4 ℃,铁的熔点是1 534.8 ℃)
参考答案:(1)Fe+Cu2+====Fe2++Cu
(2)在干燥空气中保存
(3)铜的化学性质比较稳定,不易被腐蚀,铜的熔点比较低,容易冶炼铸造成型
本题解析:湿法冶金我们在初中学过,防止铜器的生锈由防止铁生锈类比得出,根据铜的一些性质可以回答出第(3)问。
本题难度:简单
2、填空题 (15分)现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。F的水溶液为浅绿色。物质D的焰色为黄色
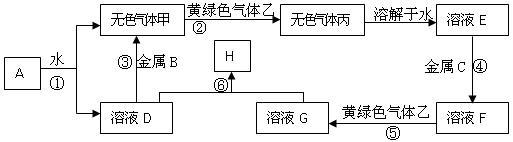
回答下列问题:
(1)写出下列物质的化学式:A?、丙?
(2)写出下列反应离子方程式:
反应③?
反应⑤?
(3)写出G溶液与金属 C反应的离子方程式?。
若该方程式是一套原电池装置的总反应式,则该原电池负极反应式为?,正极反应式为:?。
(4)描述F溶液中滴加D溶液后的现象?,写出最后生成H的化学方程式?。
参考答案:

本题解析:略
本题难度:简单
3、计算题 (4分)常温下,要将质量分数为10%的氯化钠溶液100g变为质量分数为20%的氯化钠,常用的方法有加入溶质和蒸发溶剂。请通过计算回答:
⑴需要加入氯化钠晶体?g。?
⑵需要蒸发掉?g水。
参考答案:⑴12.5g。?⑵50g
本题解析:(1)设需要加入氯化钠的质量是m,则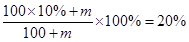 ,解得m=12.5g。
,解得m=12.5g。
(2)设需要蒸发的溶剂质量是n,则根据蒸发过程中溶质不变可知,100×10%=(100-n)×20%,解得n=50g。
本题难度:简单
4、填空题 100毫升含HNO3、H2SO4的稀溶液中,加入9.6克铜充分反应,铜全溶,产生2.24升NO(标准状况)。同体积的混合酸恰好与250毫升2mol/L的NaOH完全中和。
计算原混合酸中HNO3的物质的量浓度的取值范围_________________________
H2SO4的物质的量浓度的取值范围_______________________。
参考答案:1 mol/L≤C(HNO3)<5 mol/L,? 0<C(H2SO4)≤2 mol/L
本题解析:本题用极限法考虑,铜与混酸反应的离子方程式为3Cu+2NO3-+8H+="3" Cu 2++2NO↑+4 H2O,2.24L标准状况下的NO的物质的量是0.1mol,若硝酸全部被还原为NO,则硝酸的物质的量最小是0.1mol,浓度是1mol/L;同体积的混合酸恰好与250毫升2mol/L的NaOH完全中和,说明混酸中的氢离子的物质的量为0.5mol,若全部是硝酸提供,则硝酸的物质的量最大是0.5mol,浓度是5mol/L,所以硝酸的物质的量浓度的范围是1 mol/L≤C(HNO3)<5 mol/L;当硝酸的物质的量最小时,硫酸的物质的量最大是0.2mol,所以浓度的最大值是2mol/L,硝酸物质的量最大时,硫酸的物质的量最小为0,实际是硝酸和硫酸的混合酸,所以硫酸的浓度的取值范围是? 0<C(H2SO4)≤2 mol/L。
本题难度:一般
5、选择题 下列反应的产物中,一定不含有+ 2价铁元素的是
A.铁与盐酸
B.铁与氯气
C.铁与氯化铁溶液
D.铁与稀硝酸
参考答案:B
本题解析:A、无论谁过量,铁与盐酸反应均能生成FeCl2、H2,错误;B、无论谁过量,铁与氯气反应均生成FeCl3,正确;C、无论谁过量,铁与FeCl3溶液反应均能生成FeCl2,错误;D、铁过量时,铁与稀硝酸反应均能生成Fe(NO3)2、NO、H2O,错误。
本题难度:一般