微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某学生利用如图所示的装置制备某种干燥纯净的气体,其中A中盛放一种密度比B中密度小的液体,符合题意的选项是( )
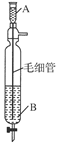
A.A为浓盐酸,B为浓硫酸,制得HCl气体
B.A为浓氨水,B为浓氢氧化钠溶液,制得NH3
C.A为浓醋酸,B为浓硫酸,制得CH3COOH
D.A为浓HI溶液,B为浓硫酸,制得HI气体
参考答案:A
本题解析:此题在于装置上的创新,利用浓H2SO4吸水放热使挥发性物质逸出。因浓H2SO4有吸水性,A可得到干燥的HCl气体,B能得到NH3但不干燥。C得到CH3COOH是液体,D中HI被浓H2SO4氧化得不到气体。所以选A。
本题难度:简单
2、填空题 (10分)农村还有些家庭直接用河水或池塘水或井水龙头作为生活饮用水,一般是把水担回家倒入水缸,加明矾使水澄清,加漂白粉进行消毒,煮沸消除暂时硬度,明矾的化学式为?,写出它溶于水后生成胶体的离子方程式:?。漂白粉的成分是?,它在自然条件下能产生次氯酸,次氯酸的氧化性很强,能杀死病菌。写出漂白粉在空气中生成次氯酸的化学方程式:?。煮沸时形成水垢的成份是?(填化学式)
参考答案:KAl(SO4)2・12H2O? Al3++3H2O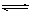 Al(OH)3(胶体)+3H+?
Al(OH)3(胶体)+3H+?
CaCl2、Ca(C1O)2? Ca(C1O)2+CO2+2H2O=CaCO3↓+2HClO
CaCO3、Mg(OH)2
本题解析:明矾的化学式为KAl(SO4)2・12H2O 。明矾溶于后,铝离子水解水生成氢氧化铝胶体,方程式为Al3++3H2O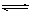 Al(OH)3(胶体)+3H+。漂白粉是混合物,含有CaCl2、Ca(C1O)2。次氯酸钙能吸收空气中的水和CO2,生成次氯酸,方程式为Ca(C1O)2+CO2+2H2O=CaCO3↓+2HClO。水垢的成份是碳酸钙和氢氧化镁。
Al(OH)3(胶体)+3H+。漂白粉是混合物,含有CaCl2、Ca(C1O)2。次氯酸钙能吸收空气中的水和CO2,生成次氯酸,方程式为Ca(C1O)2+CO2+2H2O=CaCO3↓+2HClO。水垢的成份是碳酸钙和氢氧化镁。
本题难度:一般
3、选择题 用已知浓度的盐酸滴定未知浓度的NaOH溶液,选用酚酞作指示剂,下列操作会导致测定结果偏低的是?(?)
A.酸式滴定管用蒸馏水洗后未用标准液润洗就装标准液滴定
B.锥形瓶未用待测液润洗
C.读取标准液读数时,滴前仰视,滴定到终点后俯视
D.滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失
参考答案:C
本题解析:A中酸式滴定管用蒸馏水洗后未用标准液润洗就装标准液滴定,则盐酸的浓度被稀释,消耗盐酸的体积增加,所以测定结果偏高;B中锥形瓶未用待测液润洗,属于正确的操作要求,不会影响结果;C中读取标准液读数时,滴前仰视,读数偏大。滴定到终点后俯视,读数偏小,所以消耗的盐酸的体积减少,测定结果偏低。D中滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失,说明消耗盐酸的体积增加,所以测定结果偏高,答案选C。
点评:该题是高考中的常见题型和重要考点,属于中等难度试题的考查。试题综合性强,在注重对学生基础知识巩固和训练的同时,侧重对学生解题能力的培养和方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力。该类试题需要注意的是误差分析的总依据为:由C测==C标V标/V测 由于C标、V待均为定植,所以C测的大小取决于V标的大小,即V标:偏大或偏小,则C测偏大或偏小。
本题难度:简单
4、填空题 (14分)高纯六水氯化锶(SrCl2・6H2O)可用于制造高档磁性材料、电解金属钠的助熔剂、高档颜料和液晶玻璃等,具有很高的经济价值。高纯六水氯化锶的制备过程如下:
Ⅰ.将纯水加入烧杯内,搅拌下加入适量工业碳酸锶粉末(含少量Ba、Fe的化合物),制成浆料。
Ⅱ.缓慢加入工业盐酸进行酸化,将固体物质溶解。
Ⅲ.然后喷淋加入适量的硫酸,再加入质量分数为30%的双氧水少许。
Ⅳ.调节pH至8~10, 加热至60~70℃, ,搅拌1h,过滤,除去残渣。
Ⅴ.滤液加热至沸,继续浓缩至氯化锶质量浓度(溶质质量与溶液体积之比)为 x g/L。
请回答:
(1)用电子式表示HCl的形成过程?。
(2)已知Sr为第五周期第ⅡA族元素,则不符合Sr>Ca的是?(填序号)。
①原子半径?②最外层电子数
③金属性?④最高价氧化物对应的水化物的碱性
(3)写出步骤Ⅱ中加入盐酸时发生反应的离子方程式:?。
(4)加入硫酸后会先生成硫酸锶沉淀,进而转化为硫酸钡沉淀,试分析原理?。
(5)步骤Ⅲ中在酸性环境下加入双氧水是为将亚铁离子氧化成铁离子,写出该反应的离子方程式:?。
(6)步骤Ⅳ中调节pH至8~10,最好选用的试剂为?。
(7)已知某次实验得到浓缩后的氯化锶溶液中溶质为818g,溶剂为1000 g,经测定该溶液的密度为1.5 g/mL,则该溶液溶质的质量浓度x为??g/L(计算结果保留整数)。
参考答案:(14分)
(1) (2分)
(2分)
(2)②(2分)
(3)SrCO3+2H+=Sr2++H2O+CO2↑(2分)
(4)溶液中大部分是氯化锶,所以加入硫酸后会先生成硫酸锶,由于硫酸钡的溶解度小于硫酸锶,所以会进一步转化为硫酸钡沉淀(2分)
(5)2Fe2+ + H2O2 + 2H +=2Fe3+ + 2H2O (2分)
(6)Sr(OH)2(2分)
(7)675(2分)
本题解析:略
本题难度:一般
5、实验题 (14分)某学校探究性学习小组对消毒液次氯酸钠(NaClO)的制备与性质等进行了探究。
甲同学:为制备消毒液,探究并制作了一种家用环保型消毒液(NaClO溶液)发生器,设计了如图所示的装置,用石墨作电极电解饱和氯化钠溶液。
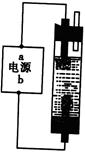
请完成下列问题:若通电时,为使生成的Cl2被完全吸收,制得有较强杀菌能力的消毒液,则电源的a电极名称为?极(填“正”、“负”、“阴”或“阳”);装置溶液中反应生成NaClO的离子方程式为:?。
乙同学:从某超市中查询到某品牌消毒液包装说明的部分内容,摘录如下:
主要有效成份为次氯酸钠,有效氯含量8000-10000mg/L。可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用。切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品。本品须密封,置阴凉暗处保存。
请完成以下实验探究过程:
I.阅读材料,根据学过的知识判断问题?
(1)室温条件下,该消毒液(NaClO)的不显中性的原因是(用离子方程式表示)
_____________________。
(2)该消毒液还具有的化学性质是_________(填序号)。
A.强氧化性? B.强还原性? C.不稳定性? D.漂白性? E.弱酸性
(3)从该消毒液的保存要求分析,导致其失效的主要原因是(用化学方程式表示)
_?。
II.确定要研究的问题
该消毒液对碳钢制品的腐蚀原理。
III.设计方案,实施探究
(1)用烧杯取少量样品,将一颗光亮的普通碳钢钉放入烧杯,浸泡一段时间。
预期的实验现象是_________________________________。
(2)为了进一步探究铁钉在该漂白剂(NaClO)溶液中的腐蚀原理,丁同学设计了如下图实验装置,写出碳(C)极上发生的电极反应式:?。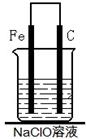
参考答案:甲:负(1分)Cl2+2OH-===Cl-+ClO-+H2O(2分)
乙:I.(1)ClO-+H2O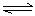 HClO+OH- (2分)
HClO+OH- (2分)
(2)A、D(2分)2NaClO+CO2+H2O=Na2CO3+2HClO(2分)? 2HClO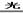 2HCl+O2↑(2分)
2HCl+O2↑(2分)
III.(1)钢钉表面有红褐色物质生成(2分)
(2)ClO-+2e-+H2O=Cl-+2OH-(2分)
本题解析:电解NaCl溶液生成氢氧化钠、氢气和氯气,氯气与氢氧化钠反应生成次氯酸钠,次氯酸钠因为水解显碱性。次氯酸钠具有强氧化性和漂白性。如果接触到空气中CO2,就会生成HClO,HClO分解就会使消毒液失效。将碳钢铁钉浸在次氯酸钠中,会发生电化学腐蚀。其中铁为负极,碳为正极。铁失电子,因为次氯酸根离子的强氧化性,次氯酸根离子得电子生成Cl―。
本题难度:简单