微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下述对乙烯和聚乙烯的描述不正确的是
A.乙烯性质比聚乙烯活泼
B.乙烯是纯净物,常温下为气态,聚乙烯为固态,是混合物
C.取等物质的量的乙烯和聚乙烯,完全燃烧,生成的CO2和H2O的物质的量分别相等
D.取等质量乙烯和聚乙烯,完全燃烧后,生成的CO2和H2O的质量分别相等
参考答案:C
本题解析:乙烯中含有碳碳双键,聚乙烯中不含双键,所以乙烯性质活泼;聚乙烯的聚合度不确定,是一种混合物;乙烯和聚乙烯的组成相同,所以取等质量乙烯和聚乙烯,完全燃烧后,生成的CO2和H2O的质量分别相等;但是等物质的量的乙烯和聚乙烯,完全燃烧,生成的CO2和H2O不相同,聚乙烯因为乙烯的n倍(n为聚乙烯的聚合度).
本题难度:困难
2、选择题 将5.6克Fe在一定量稀硝酸中恰好完全溶解后,往溶液中滴加KOH溶液立即产生沉淀,滴加至沉淀量最大时,再将所得溶液和沉淀一起加热蒸干,并在空气中灼烧至恒重,所得固体成分和可能的质量为
A.Fe2O3:8gKNO2:12.7g
B.Fe2O3:8gKNO2:20.4g
C.Fe2O3:8gKNO2:31.5g
D.FeO:7.2gKNO3:16.4g
参考答案:B
本题解析:分析:根据5.6gFe与稀硝酸反应可能生成硝酸亚铁或硝酸铁两种情况计算,5.6gFe的物质的量为0.1mol,加入氢氧化钾后蒸干,滴加至沉淀量最大时,溶液为硝酸钾溶液,得到0.1mol铁的氢氧化物(氢氧化亚铁会被空气氧化)和0.2mol硝酸钾或硝酸钾0.3mol,蒸干并在空气中灼烧至恒重,最后得 到0.05mol氧化铁和0.2mol硝酸钾或0.3mol亚硝酸钾,可分别计算出亚硝酸钾的质量范围.
解答:5.6gFe的物质的量为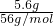 =0.1mol,
=0.1mol,
若铁全部恰好生成硝酸亚铁,根据铁元素守恒n[Fe(NO3)2]=n(Fe)=0.1mol,
加入氢氧化钾后,加热蒸干,并在空气中灼烧至恒重,固体为氧化铁与硝酸钾.
根据硝酸根子守恒可得n(KNO3)=2n[Fe(NO3)2]=2×0.1mol=0.2mol,
根据铁元素守恒可得n(Fe2O3)= n(Fe)=
n(Fe)= ×0.1mol=0.05mol,
×0.1mol=0.05mol,
所以固体质量是:氧化铁0.05mol×160g/mol=8g,亚硝酸钾0.2mol×69g/mol=13.8g
若铁全部恰好生成硝酸铁,根据铁元素守恒n[Fe(NO3)3]=n(Fe)=0.1mol,
根据硝酸根子守恒可得n(KNO3)=3n[Fe(NO3)2]=3×0.1mol=0.3mol,
加入氢氧化钾后,加热蒸干,并在空气中灼烧至恒重,固体为氧化铁与硝酸钾.
根据铁元素守恒可得n(Fe2O3)= n(Fe)=
n(Fe)= ×0.1mol=0.05mol,
×0.1mol=0.05mol,
所以固体质量是:氧化铁0.05mol×160g/mol=8g,亚硝酸钾0.3mol×69g/mol=20.7g
所以氧化铁质量是8g,亚硝酸钾质量在13.8g~20.7g之间.
故选:B.
点评:本题考查混合物的计算,题目难度较大,注意本题考虑5.6gFe与稀硝酸反应可能生成硝酸亚铁或硝酸铁两种情况计算,利用端值法求解.
本题难度:困难
3、选择题 在下列反应中,水既不作氧化剂,也不作还原剂的氧化还原反应是
A.Na2O2+H2O
B.Na2O+H2O
C.Na+H2O
D.CO2+H2O
参考答案:A
本题解析:分析以上四个反应,B、D不是氧化还原反应,C中水是氧化剂,符合题意的只有过氧化钠与水的反应。
本题难度:困难
4、选择题 根据某种共性,可将CO2、SO2归为同类氧化物。下列物质中,也属于这类氧化物的是:
A.SO3
B.CaO
C.NO
D.NO2
参考答案:A
本题解析:由性质分析可知CO2、SO2均能与碱反应且产物只有盐和水,即为酸性氧化物,A也是酸性氧化物,B为碱性氧化物,而C与碱溶液不反应D与碱溶液发生氧化还原反应。答案选A。
本题难度:一般
5、选择题 已知HX为一元弱酸.某混合溶液中含有4mol?NaX、2mol?Na2CO3和1mol?NaHCO3.往溶液中通入3mol?CO2气体,充分反应后,气体全部被吸收,所得溶液中钠盐的量可能为
A.A
B.B
C.C
D.D
参考答案:A
本题解析:分析:HX为一元弱酸,混合溶液中含NaX、Na2CO3和NaHCO3,故酸性HX>HCO3-,若酸性HX>H2CO3,则CO2与Na2CO3反应,若酸性
HX<H2CO3,CO2先与Na2CO3反应先,Na2CO3反应完毕,若CO2有剩余,再与NaX反应,故溶液中首先发生反应:Na2CO3+CO2+H2O=2NaHCO3,由方程式可知2molNa2CO3消耗2molCO2,故剩余1molCO2,由气体全部被吸收,故酸性HX<H2CO3,还发生反应NaX+CO2+H2O=HX+NaHCO3,据此计算结合进行判断.
解答:溶液中首先发生反应:Na2CO3+CO2+H2O=2NaHCO3,由方程式可知2molNa2CO3消耗2molCO2,故剩余1molCO2,故溶液中n(Na2CO3)=0mol,生成NaHCO3为2mol;
由气体全部被吸收,故酸性HX<H2CO3,还发生反应NaX+CO2+H2O=HX+NaHCO3,则:
? NaX+CO2+H2O=HX+NaHCO3,
1mol? 1mol? 1mol
故1mol反应消耗1molNaX,生成1molNaHCO3,
所以溶液中n(NaX)=4mol-1mol=3mol,n(NaHCO3)=1mol+2mol+1mol=5mol,
故选A.
点评:考查混合物的计算,难度较大,为易错题,根据离子共存与二氧化碳没有剩余判断发生的反应是解题的关键.
本题难度:一般