| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点归纳《化学平衡的移动和应用》考点强化练习(2017年押题版)(六)
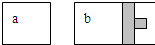 参考答案:充入SO3(g)后发生反应2SO3(g)?2SO2(g)+O2(g),气体的物质的量增大,a容器内压强比b容器内高,a容器相当于在b容器的基础上增大压强,平衡逆向移动,SO3的转化率降低,故a<b, 本题解析: 本题难度:简单 3、填空题 一定条件下,在体积为3L的密闭容器中化学反应 CO(g)+2H2(g) (1)该反应的平衡常数表示K=______________根据上图降低温度K将__________(填“增大”、 参考答案:(1) 本题解析: 本题难度:一般 4、填空题 一种“人工固氮”的新方法是在常温、常压、光照条件下,N2在催化剂表面与水发生反应生成NH3: 参考答案:(1)2.5×10-8 本题解析: 本题难度:一般 5、选择题 一定条件下,将X和Y两种气体按不同比例放入固定容积的密闭容器中,反应达平衡后,测得X、Y的转化率与起始时物质的量之比 参考答案:A 本题解析: 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《物质的组成.. | |