微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一定条件下存在下列平衡:2A(g)?B(g);△H<O在测定A的相对分子质量时,下列条件中测定结果误差最小的是( )
A.温度150℃、压强5.05×104Pa
B.温度150℃、压强4.04×105Pa
C.温度25℃、压强1.01×105Pa
D.温度0℃、压强5.05×104Pa
参考答案:由于存在平衡2A(g)?B(g),B的存在会影响A的相对分子质量测定,故应采取措施使平衡向左移动,减小B的含量,该反应正反应是体积减小的放热反应,减小压强平衡向逆反应移动,升高温度平衡向逆反应移动,故应采取高温低压,平衡逆向进行,测定结果误差最小,
故选A.
本题解析:
本题难度:一般
2、填空题 有两个起始体积相同的密闭容器A和B,A容器有一个可移动的活塞,能使容器内保持恒压;B容器为固定体积。起始时这两个容器分别充入等量的体积比为2∶1的SO2和O2的混合气,并使A、B容器中气体体积相等,并保持在400℃条件下发生反应2SO2+O2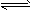 2SO3,并达到平衡。
2SO3,并达到平衡。

(1)达到平衡所需时间,A容器比B容器_______,两容器中SO2的转化率A比B______。
(2)达到⑴所述平衡后,若向两容器中分别通入数量不多的等量Ar气体,A容器的化学平衡向________移动,B容器的化学平衡________移动。
(3)达到⑴所述平衡后,若向容器中通入等量的原混合气体,重新达到平衡后,A容器中SO3的体积分数________,B容器中SO3的体积分数__________(填变大、变小、不变)。
参考答案:(1)短;大
(2)逆反应方向;不
(3)不变;变大
本题解析:
本题难度:一般
3、选择题 某温度下,在容积固定不变的密闭容器中进行如下可逆反应:X(g)+Y(g)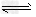 Z(g)+W(s) ΔH>0 一段时间后,达到化学平衡状态.下列叙述正确的是
Z(g)+W(s) ΔH>0 一段时间后,达到化学平衡状态.下列叙述正确的是
[? ]
A.通入稀有气体,平衡向正反应方向移动
B.加入少量W,逆反应速率增大
C.升高温度,正反应速率增大,逆反应速率减小
D.降低温度,平衡向逆反应方向移动
参考答案:D
本题解析:
本题难度:一般
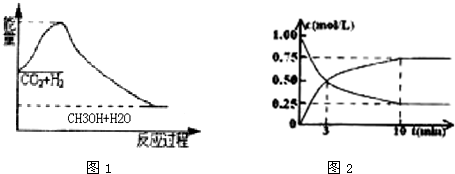
4、简答题 2009年12月7日~18日在丹麦首都哥本哈根召开了世界气候大会,商讨《京都议定书》一期承诺到期后的后续方案,即2012年至2020年的全球减排协议,大会倡导“节能减排”和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.过渡排放CO2会造成“温室效应”,科学家正在研究如何将CO2转化为可利用的资源.目前工业上有一种方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),图1表示该反应过程中能量(单位为kJ?mol-1)的变化:
(1)关于该反应的下列说法中,正确的是______(填字母).
A.△H>0,△S>0
B.△H>0,△S<0
C.△H<0,△S<O
D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在1L固定体积的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),经测得CO2和CH3OH(g)的浓度随时间变化如图2所示.
①从反应开始到平衡,CO2的平均反应速率v(CO2)=______.
②该反应的平衡常数表达式K=______.
③下列措施中能使化学平衡向正反应方向移动的是______.(填字母)
A.升高温度
B.将CH3OH(g)及时液化抽出
C.选择高效催化剂
D.再充入1molCO2和3molH2
(3)25℃,1.01×105Pa时,16g液态甲醇完全燃烧,当恢复到原状态时,放出362.9kJ的热量,写出该反应的热化学方程式为______.
参考答案:(1)依据反应和图象分析判断:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),气体的物质的量减少,反应是熵减少的反应△S<0;反应物能量高于生成物的能量,判断反应是放热反应,△H<0,
故答案为:C;
(2)二氧化碳是反应物随反应进行浓度减小,甲醇是生成物,随反应进行浓度增大;10nim内达到平衡,生成甲醇浓度为0.75mol/L,二氧化碳浓度变化了0.75mol/L,则:
①v(CO2)=0.75mol/L10min=0.075mol/(L?min);
故答案为:0.075mol/(L?min);
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)的平衡常数表达式K=c(H2O)c(CH3OH)c(CO2)c3(H2),
故答案为:c(H2O)c(CH3OH)c(CO2)c3(H2);
③措施中能使化学平衡向正反应方向移动的是:
A、反应是放热反应,升温平衡逆向进行;故A错误;
B、将CH3OH(g)及时液化抽出,减小生成物的量,平衡正向进行,故B正确;
C、选择高效催化剂只能改变速率,不改变化学平衡,故C错误;
D、再充入l molCO2和4molH2,增大压强平衡正向进行,故D正确;
故选:BD;
(3)25℃,1.01×105Pa时,16g液态甲醇完全燃烧,当恢复到原状态时,放出362.9kJ的热量,则1mol甲醇完全燃烧恢复到原状态时,放出热量
=362.9kJ×1mol×32g/mol16g=725.8kJ,故甲醇燃烧热的热化学方程式为:CH3OH(l)+32O2(g)=CO2(g)+2H2O(l)△H=-725.8 kJ?mol-1;
故答案为:CH3OH(l)+32O2(g)=CO2(g)+2H2O(l)△H=-725.8 kJ?mol-1.
本题解析:
本题难度:一般
5、选择题 在密闭容器中,反应N2(g)+3H2(g)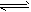 2NH3(g);ΔH<0, 达到甲平衡。在仅改变某一条件后,达到乙平衡,改变的这一条件是
2NH3(g);ΔH<0, 达到甲平衡。在仅改变某一条件后,达到乙平衡,改变的这一条件是
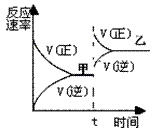
[? ]
A.增大压强
B.升高温度
C.增大N2的浓度
D.加入适当催化剂
参考答案:A
本题解析:
本题难度:一般
|