微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在氯水中存在着如下反应:Cl2+H2O=HCl+HClO,因此氯水中存在多种分子和离子。在下列实验现象中与相应离子或分子性质关系正确的是(? )
A.氯水有刺激性气味说明氯水中有HCl
B.氯水中滴入品红溶液,溶液为无色说明氯水中有Cl2
C.向氯水中通入SO2气体,氯水黄绿色褪去说明Cl2发生了反应
D.向氯水中加入CaCO3有气泡产生,说明有HCl和HClO
参考答案:C
本题解析:氯水中的HCl不会挥发,有刺激性气味的是Cl2分子,A错误。氯水的漂白性是HClO,而不是Cl2,B错误。SO2与Cl2反应黄绿色褪去,C正确。HClO不会与CaCO3反应产生CO2,D错误。
本题难度:简单
2、填空题 (8分)右图为实验室某浓盐酸试剂瓶标签上的有关数据,根据有关数据回答下列问题:
盐酸
分子式:HCl
相对分子质量:36.5
密度:1.19g/m3
质量分数:36.5%
|
(1)该浓盐酸中HCl的物质的量浓度为?mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少?而变化的是?。
A、溶液中HCl的质量? B、溶液的p H
C、溶液中H+的数目? D、溶液的密度
(3)欲配制上述浓盐酸,需要在1L水中通入标态下?L
HCl气体(保留1位小数)
(4)现有1L1mol/L的稀盐酸,欲使其浓度增大1倍,采取的措施合理的是?。
A、通入标况下HCl气体22.4L? B、将溶液加热浓缩至0.5L?
C、加入5mol/L的盐酸0.6L,再稀释至2L。? D、加入1L 3mol/L的盐酸混合均匀。
参考答案:(1)11.9mol/L(2分)?(2)BD(2分)
(3)352.7(2分)?(4)C?(2分)
本题解析:略
本题难度:简单
3、选择题 “绿色化学实验”进课堂。某化学教师为“氯气与钠反应”设计了如下装置与操作以替代课本相关实验。实验操作如下图:
将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大的金属钠(已擦净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔化成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是
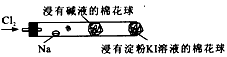
[? ]
A.反应生成的大量白烟是氯化钠晶体
B.玻璃管尾部塞一团浸有NaOH溶液的棉花球是用于吸收过量的氯气,以免其污染空气
C.钠燃烧产生苍白色火焰
D.若在棉球外沿滴一滴淀粉碘化钾溶液,可据其颜色变化判断氯气是否被碱液完全吸收
参考答案:C
本题解析:
本题难度:一般
4、选择题 对下列事实的解释错误的是( )
A.氨溶于水的喷泉实验,说明氨气极易溶于水
B.常温下,浓硝酸可用铝罐来贮存,说明浓硝酸具有强氧化性
C.氯气可使湿润的红色布条褪色,说明次氯酸具有漂白性
D.向蔗糖中加入浓硫酸后出现发黑现象,说明浓H2SO4具有吸水性
参考答案:A.如果盛放氨气的烧瓶内外不产生压强差,则不能形成喷泉,实际上,氨气能形成喷泉实验,则说明氨气极易溶于水,而使烧瓶内外产生压强差而形成喷泉,故A正确;
B.常温下,浓硝酸和铝反应生成一层致密的氧化物薄膜而阻止进一步反应,浓硝酸体现了强氧化性,故B正确;
C.氯气和水反应生成次氯酸,氯气、盐酸都不能使干燥的有色布条褪色,湿润的氯气能使有色布条褪色,则说明次氯酸有漂白性,故C正确;
D.浓硫酸具有脱水性,可使蔗糖脱水、碳化生成炭黑和水而导致蔗糖变黑,故D错误;
故选D.
本题解析:
本题难度:一般
5、填空题 Ⅰ.玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流等等。下列有关实验过程中,肯定不需要使用玻璃棒进行操作的是 (可以多选)?
A.用pH试纸测定Na2CO3溶液的pH
B.从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl
C.实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
D.配制一定物质的量浓度的氯化钠溶液
E.取某溶液做焰色反应实验,说明该溶液中含有钠元素
F.用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
G.促使过饱和的硝酸钾溶液析出晶体
Ⅱ.二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。ClO2是一种黄绿色的气体,易溶于水,有刺激性气味,对人的呼吸系统有损伤,可与碱发生作用。实验室以NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
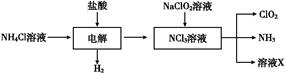
(1)写出电解时发生反应的化学方程式 ?;
(2)除去ClO2中的NH3可选用的试剂是 (填序号);
A.饱和食盐水? B.碱石灰? C.浓硫酸? D.水
(3)测定ClO2(如图)的过程如下:在锥形瓶中加入足量的碘化钾,用100 mL水溶解后,再加3 mL足量硫酸溶液;在玻璃液封管中加入水;将生成的ClO2气体通过导管在锥形瓶中被吸收(假设吸收完全);将玻璃封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用c mol/L硫代硫酸钠标准溶液滴定(I2+2S2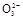
 2I-+S4
2I-+S4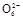 ),共用去V mL硫代硫酸钠溶液。
),共用去V mL硫代硫酸钠溶液。
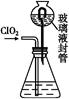
①装置中玻璃液封管的作用是 ;
②请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式?;
③测得ClO2的质量m(ClO2)= 。(用含c、V的代数式表示)。
参考答案:Ⅰ.CE
Ⅱ.(1)NH4Cl+2HCl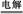 3H2↑+NCl3
3H2↑+NCl3
(2)C
(3)①吸收残余的二氧化氯气体,并使锥形瓶内外压强相等
②2ClO2+10I-+8H+ 4H2O+5I2+2Cl-
4H2O+5I2+2Cl-
③1.35 cV×10-2 g
本题解析:Ⅰ.A需要用玻璃棒蘸取溶液,B中需要对残留固体进行溶解、过滤、蒸发结晶,需要用玻璃棒搅拌、引流。C中用不到玻璃棒。D中配制溶液时要用玻璃棒搅拌、引流。E实验需要用铂丝,用不到玻璃棒。F用玻璃棒搅拌。G用玻璃棒摩擦烧杯壁来引发结晶。用不到玻璃棒的是C、E。
Ⅱ.(1)从流程图中可以看出电解过程中生成了H2、NCl3溶液,所以阴极上是H+得电子生成H2,阳极上是N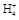 失去电子被氧化为NCl3,电解反应方程式:NH4Cl+2HCl
失去电子被氧化为NCl3,电解反应方程式:NH4Cl+2HCl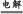 3H2↑+NCl3。(2)ClO2对人体有伤害作用,所以需用试剂吸收,又因ClO2及NH3都易溶于水,都能与碱作用,所以A、B、D不用选,只能用浓H2SO4吸收其中的NH3。
3H2↑+NCl3。(2)ClO2对人体有伤害作用,所以需用试剂吸收,又因ClO2及NH3都易溶于水,都能与碱作用,所以A、B、D不用选,只能用浓H2SO4吸收其中的NH3。
(3)①ClO2气体逸出会危害环境,玻璃密封管可以把逸出的少量气体吸收,同时通过水封与大气相通,保证锥形瓶内压强与大气压强相等。
②ClO2气体把还原性的I-氧化成I2。
③根据:I2+2S2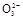
 2I-+S4
2I-+S4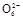 和2ClO2+10I-+8H+
和2ClO2+10I-+8H+ 4H2O+5I2+2Cl-,可以得出关系式:
4H2O+5I2+2Cl-,可以得出关系式:
2ClO2~5I2~10S2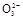 ,n(S2
,n(S2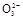 )=cV×10-3 mol,
)=cV×10-3 mol,
n(ClO2)=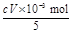 ,m(ClO2)="1.35" cV×10-2 g。
,m(ClO2)="1.35" cV×10-2 g。
本题难度:一般