��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �Ȼ�����ˮ�д����ܽ�ƽ�⣺AgCl?Ag++Cl-������ͬ�¶��£��������Ȼ����ֱ������ͬ�����������Һ�У�Ag+��Ũ����С���ǣ�������
A��0.1mol/L?HCl
B������ˮ
C��0.1mol/LAlCl3
D��0.1mol/LMgCl2
�ο��𰸣��������Ȼ����ֱ������ͬ�����������Һ�У�Ag+��Ũ����С����Cl-Ũ��Ӧ�������C��Cl-Ũ�����
��ѡC��
���������
�����Ѷȣ���
2������� (4��)��֪AgClΪ������ˮ����İ�ɫ���壬Ag2SΪ������ˮ����ĺ�ɫ���塣��
AgCI��ˮ������Һ�м���������Na2S��Һ���������ɫ������ȫת��Ϊ��ɫ���壺
(1)д����ɫ����ת���ɺ�ɫ����Ļ�ѧ����ʽ��? ��?��
(2)��ɫ����ת���ɺ�ɫ�����ԭ���ǣ�? ��?��
�ο��𰸣�

�����������
�����Ѷȣ���
3��ѡ���� ����˵������ȷ����
[? ]
A�����ʵ��ܽ���Ϊ���ܣ�������ʲ�����ˮ
B��������ˮ�������ܽ��Ϊ0
C��ij���ӱ�������ȫ��ָ����������Һ�е�Ũ��Ϊ0
D�����Բ��ܽ�������Dz����ڵ�
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4��ѡ���� ����˵���������
[? ]
A.Ǧ�����ڷŵ�����У������������ռ�С������������������
B.���ȷ�Ӧ��һ�����Է�����
C.һ�������£�ʹ�ô����ܼӿ췴Ӧ���ʣ���������߷�Ӧ���ƽ��ת����
D.�¶�һ��������Һ��Ag����Cl��Ũ�ɵij˻�����Kspʱ����ҺΪAgCl�ı�����Һ
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5������� ���û�ѧ��Ӧԭ���о��⡢�����ȡ���ȵ��ʼ��仯����ķ�Ӧ����Ҫ����
��1����֪��25��ʱKSP��AgCl��=1.6��l0��10?KSP��AgI��=1.5��l0��16
��ˮ�к��д�����Ԫ�أ�����Ԫ�����ȣ���Ԫ����⣬���ں�ˮ�о��Ի���̬���ڡ���25���£���0.1L0.002mol��L��l��NaCl��Һ�м���0.1L0.002mol��L��l��������Һ���а�ɫ�������ɣ�����������ԭ���ǣ�ͨ������ش�?����Ӧ��Ļ���Һ�м�������0.1L0.002mol��L��1��NaI��Һ��������������?�������������ԭ���ǣ������ӷ���ʽ��ʾ��?��
��2������������Ʊ������ܶ࣬���з�����ԭ����������ߵ���?������ţ���
A��BaO2 + H2SO4�� BaSO4 �� + H2O2 ?
B��2NH4HSO4 (NH4)2S2O8 + H2��
(NH4)2S2O8 + H2��
(NH4)2S2O8 + 2H2O �� 2NH4HSO4 + H2O2
C��CH3CHOHCH3 + O2�� CH3COCH3 + H2O2
D���һ�����������ͼ
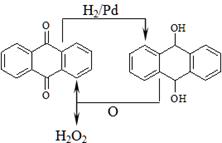
��3��ij���ױ����˲�ͬ�������Ӽ���Ũ�ȶ�˫��ˮ�������⺣��������Һ��Ӧ���ʵ�Ӱ�죬ʵ������ͼ1��ͼ2��ʾ��
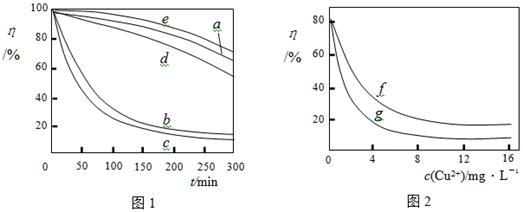
ע������ʵ������¶�Ϊ20�桢w(H2O2)��0.25%��pH��7.12������������ҺŨ��Ϊ8mg��L�D1�������½��С�ͼ1������a��H2O2��b��H2O2+Cu2+��c��H2O2+Fe2+��d��H2O2+Zn2+��e��H2O2+Mn2+��ͼ2������f����Ӧʱ��Ϊ1h��g����Ӧʱ��Ϊ2h����ͼ�е��������������������Һ��ճ�ȣ���������Ũ������Һճ������أ���
��������Ϣ��֪�����������������?������ţ���
A����������ʹ�ý��ⷴӦ���ʼ���?
B���������ӶԸý��ⷴӦ�Ĵ�Ч�ʱ�ͭ���ӵ�
C������������Һճ�ȵı仯�����ɷ�ӳ���併�ⷴӦ���ʵĿ���
D��һ�������£�ͭ����Ũ��һ��ʱ����Ӧʱ��Խ��������������ҺŨ��ԽС
�ο��𰸣���10�֣�
��1��Q (AgCl)= c(Ag+)��c (Cl��)= 1��l0��6��Ksp(AgCl)?��2�֣�
��ɫ����ת��Ϊ��ɫ���� ��2�֣�
AgCl(s) + I����aq�� ==? AgI(s) + Cl��(aq)? (2�֣�����s��1�֣�����aq���۷�)
��2��D��2�֣�
��3��B��2�֣�
�����������1��Q (AgCl)= c(Ag+)��c (Cl��)= 1��l0��6��Ksp(AgCl)��KSP��AgI��=1.5��l0��16>Q (AgCl),�ʰ�ɫ����ת��Ϊ��ɫ���������ӷ���ʽ�ǣ�AgCl(s) + I����aq�� ==? AgI(s) + Cl��(aq)��
��2��ԭ����������ߵ��Ƿ�Ӧ�ﶼת��Ϊ���������Щ��Ӧ�������±�Ϊ�������ٷ�Ӧ���ʴ�D��
��3��B�H2O2���������Զ�Fe2+���л�ԭ�ԣ�֮�䷢����������ԭ��Ӧ�����������ӶԸý��ⷴӦ�Ĵ�Ч�ʱ�ͭ���ӵ�˵���Ǵ���ġ���ѡB��
���������⿼�黯ѧƽ�⡢�Ȼ�ѧ����ʽ������ת������ͼ�������Ѷ��еȣ�ѧ��ע��Ի���֪ʶ��ѧϰ��Ӧ�á�
�����Ѷȣ�һ��