微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 抗氧剂亚硫酸钠可利用硫酸工业的炉气和尾气与纯碱反应来制取,生产流程如图1:
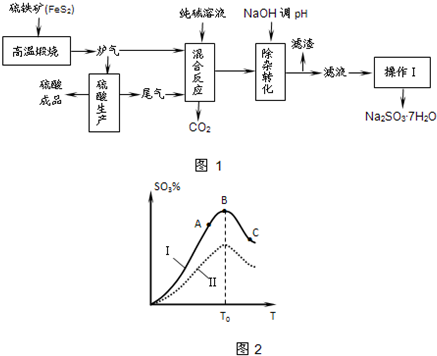
已知:①炉气、尾气中含有SO2;②混合反应中还溶解有少量Fe2O3、MgO等矿尘.
(1)煅烧1molFeS2放出热量为853kJ,则FeS2燃烧的热化学方程式为______.
(2)“混合反应”中纯碱(Na2CO3)参与反应的化学方程式为______(任写一个).
(3)用NaOH“除杂”时,主要的离子方程式为______(任写一个).
(4)通过“操作Ⅰ”可以得到亚硫酸钠晶体,写出主要操作步骤的名称:______
(5)硫酸生产中炉气转化反应为:2SO2(g)+O2(g)?2SO3(g).研究发现,SO3的体积分数(SO3%)随温度(T)的变化如图2曲线Ⅰ所示.下列判断正确的是______
A.该反应的正反应为放热反应
B.曲线Ⅰ上A、C两点反应速率的关系是:vA>vC
C.反应达到B点时,2v正(O2)=v逆(SO3)
D.已知V2O5的催化效果比Fe2O3好,
若Ⅰ表示用V2O5催化剂的曲线,则Ⅱ是Fe2O3作催化剂的曲线.
参考答案:(1)FeS2燃烧生成二氧化硫与氧化铁,1molFeS2放出热量为853kJ,则FeS2燃烧的热化学方程式为4FeS2(S)+11O2(g)=8SO2(g)+2Fe2O3(s),△H=-3412?kJ?mol?-1.
故答案为:4FeS2(S)+11O2(g)=8SO2(g)+2Fe2O3(s),△H=-3412?kJ?mol?-1.
(2)SO2与纯碱(Na2CO3)溶液反应的方程式为SO2+Na2CO3=Na2SO3+CO2↑或2?SO2+Na2CO3+H2O=NaHSO3+CO2↑.
故答案为:SO2+Na2CO3=Na2SO3+CO2↑或2?SO2+Na2CO3+H2O=NaHSO3+CO2↑.
(3)合反应后的溶液中含有少量的Fe2+、Mg2+、HSO3-等.Fe2+、Mg2+、HSO3-等都与OH-发生反应.发生反应离子方程式为
Fe2++2OH-=Fe(OH)2↓或Mg2++2OH-=Mg(OH)2↓或HSO3-+OH-=SO32-+H2O.
故答案为:Fe2++2OH-=Fe(OH)2↓或Mg2++2OH-=Mg(OH)2↓或HSO3-+OH-=SO32-+H2O.
(4)从溶液中获得固体物质应加热蒸发、冷却结晶、过滤、洗涤干燥.
故答案为:加热蒸发、冷却结晶、过滤、洗涤干燥.
(5)由图象可知T0前反应未达平衡,T0时处于平衡状态,T0后升高温度平衡向逆反应移动.
A、T0后升高温度平衡向逆反应移动,升高温度平衡向吸热反应移动,故正反应为放热反应,故A正确;
B、A未达平衡,B处于平衡状态,反应速率比A点高,T0后温度升高反应速率加快,平衡向逆反应移动,但比B点的速率高,所以:vA<vC,故B错误;
C、不同物质表示的正逆反应速率之比等于化学计量数之比,反应到达平衡状态,反应达到B点时,到达平衡状态,所以2v正(O2)=v逆(SO3),故C正确;
D、使用催化剂,加快反应速率,缩短到达平衡时间,但平衡不移动,用V2O5催化剂与Fe2O3作催化剂,到达平衡时三氧化硫的含量相同,故D错误.
故选:AC.
本题解析:
本题难度:一般
2、选择题 在密闭容器中发生下列反应aA(g)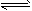 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
[? ]
A.A的转化率变大
B.平衡向正反应方向移动
C.D的体积分数变大
D.a <c+d
参考答案:D
本题解析:
本题难度:一般
3、选择题 某温度下,在一容积固定的容器中,反应aA(g)+bB(g)?hH(g)达到平衡后,A、B、H的物质的量分别为amol、bmol和hmol.已知a+b=h,若保持温度不变,将三者的物质的量增大一倍,则下列判断正确的是( )
A.气体的平均相对分子质量变大
B.平衡不移动
C.B的体积分数减少
D.混合气体的密度不变
参考答案:A、将三者的物质的量增大一倍,混合气体的质量和气体的物质的量同等程度的增大,所以气体的平均相对分子质量保持不变,故A错误;
B、a+b=h,说明反应前后气体体积不变,将三者的物质的量增大一倍,相当于增大压强,平衡不移动,故B正确;
C、将三者的物质的量增大一倍,相当于增大压强,平衡不移动,B的体积分数不变,故C错误;
D、混合气体的质量是增大的,容积固定,所以混合气体的密度增大,故D错误.
故选B.
本题解析:
本题难度:简单
4、选择题 在一密闭容器中发生反应:2X(g)+Y(g) aZ(g) ΔH=Q kJ・mol-1,开始按体积比2∶1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图象,下列有关说法正确的是( )
aZ(g) ΔH=Q kJ・mol-1,开始按体积比2∶1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图象,下列有关说法正确的是( )
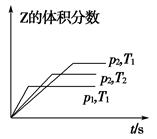
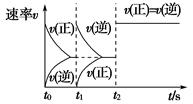
甲 乙
A.图甲,p1>p2,a<3
B.图甲,T1<T2,Q>0
C.图乙,t1时表示恒温、恒压条件下,向平衡体系中充入一定量的Z气体
D.图乙,如果a=3,t2时表示向体系中加入了催化剂或增大压强