| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《化学平衡》试题强化练习(2017年最新版)(六)
CO(g)+H2O(g)  CO2(g)+H2(g),得到如下数据: CO2(g)+H2(g),得到如下数据:
(3)把水煤气中的混合气体经过处理后获得的较纯H2用于工业合成氨。已知: N2(g)+3H2(g)  2NH3(g) ΔH=-92.4kJ?mol-1 2NH3(g) ΔH=-92.4kJ?mol-12N2(g)+6H2O(l)  4NH3(g)+3O2(g) ΔH=" +1530.0kJ" /mol 4NH3(g)+3O2(g) ΔH=" +1530.0kJ" /mol①氢气的燃烧热ΔH=_______________。 ②实验Ⅲ比实验Ⅰ的温度要高,其它条件相同,请在下图中画出实验Ⅰ和实验Ⅲ中NH3浓度随时间变化的示意图,并作必要的标注。  参考答案:(1)AD 本题解析:(1)该反应吸热,升高温度平衡正向移动,水的转化率增大;碳为固体,增加碳的用量平衡不移动,水的转化率不变;加入催化剂,平衡不移动,水的转化率不变;减小CO的浓度,平衡正向移动,用CO吸收剂除去CO可使平衡正向移动,水的转化率增大;(2)利用三段式: 本题难度:困难 2、选择题 在某容积一定的密闭容器中,有下列可逆反应2A(g) + B(g) | |||||||||||||||||
参考答案:C
本题解析:A.根据图II可知,在温度相同时,压强不同,Y的含量不同,说明该反应是反应前后气体体积不等的反应,所以x不等于2,错误;B.根据图I可判断T1>T2和△H<0,p1<p2,正反应为放热反应,错误;C.增大压强,C增大,说明增大压强,平衡正向移动,正反应方向为气体体积减小的反应,所以x<3。对于此可逆反应,p越大,B的转化率越大,T越高,B的转化率越小,正确;D.在恒容的容器内进行的气体发生反应,气体密度始终不变,错误。
考点:考查可逆反应的化学平衡移动、反应热及物质的转化率的计算的知识。
本题难度:困难
3、选择题 相同温度下体积固定的密闭容器中,发生如下可逆反应: A2(g) + 3B2(g) 2AB3(g),下列情况一定能说明该可逆反应已经达到化学平衡状态的是
2AB3(g),下列情况一定能说明该可逆反应已经达到化学平衡状态的是
①反应中各组分的物质的量不随时间而变化了②混合气体的总物质的量不随时间而变化了③容器内的压强不随时间而变化了⒁④容器内气体的平均相对分子质量不随时间而变化了⑤容器内气体的密度不随时间而变化了⑥V(A2) 正/v(B2) 正="1/3" ⑦V(A2) 正/v(B2) 逆="1/3" ⑧c(A2):c(B2):c(AB3)=1:3:2⑨ c(A2)=c(B2)=c(AB3)
参考答案:C
本题解析:可逆反应已经达到化学平衡状态的标志:(1)正、逆反应速率相等;(2)体系中各组分的浓度保持不变;
① 平衡,体积固定的密闭容器中,当各组分的物质的量不随时间而变化,即浓度不变;
②平衡,该反应为非等体积反应,混合气体的总物质的量不随时间而变化,即各组分的浓度不变的状态;
③平衡,容器内的压强不随时间而变化,即体系内气体的总物质的量不变,由于反应为非等体积反应,即各组分的浓度不变;
④平衡,相同温度下体积固定的密闭容器中,容器内气体的平均相对分子质量不随时间而变化,即气体的总物质的量不变的状态,在非等体积反应中,即达平衡;
⑤不一定平衡,体积固定的密闭容器,且反应物和生成物均为气体的状态下,无论平衡与否,容器内气体的密度均不会发生改变;
⑥不一定平衡,速率之比遵循化学计量数之比,不一定说明平衡了,可能平衡也可能未平衡;
⑦平衡,
⑧不一定平衡,浓度之比=化学计量数之比也不一定说明。
⑨不一定平衡,浓度相等也不一定。
本题难度:一般
4、填空题 化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。
请回答下列问题: (1)工业上采取CO和H2为原料合成乙醇,其化学反应方程式为:2CO(g)+4H2(g)
(1)工业上采取CO和H2为原料合成乙醇,其化学反应方程式为:2CO(g)+4H2(g)
参考答案:
本题解析:
本题难度:困难
5、选择题 一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)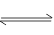 3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后,A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是
3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后,A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是
A.2 mol C B.2 mol A、1 mol B和1 mol He(不参加反应)
C.1 mol B和1 mol C D.2 mol A、3 mol B和3 mol C
参考答案:AB
本题解析:根据方程式可知,该反应是体积不变的可逆反应,所以只要满足最初A和B的物质的量浓度满足1:1即可满足平衡是等效的。根据选项可知A中相当于是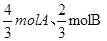 ,这说明选项A中平衡后A的体积分数大于a%。选项B中A的物质的量大于B的,则平衡后A的体积分数大于a%。选项C中相当于是
,这说明选项A中平衡后A的体积分数大于a%。选项B中A的物质的量大于B的,则平衡后A的体积分数大于a%。选项C中相当于是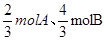 ,因此A的转化率增大,平衡后A的体积分数小于a%;选项D中相当于是4molA和4molB,和最初的平衡是等效的,答案选AB。
,因此A的转化率增大,平衡后A的体积分数小于a%;选项D中相当于是4molA和4molB,和最初的平衡是等效的,答案选AB。
考点:考查等效平衡的有关判断
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生的逻辑推理能力和抽象思维能力,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是明确等效平衡的含义和判断依据,并能灵活运用即可。
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点讲解《阿伏伽德罗.. | |