��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (10��)��֪A(g)+B(g) C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
|�¶�/ ��
| 700
| 900
| 830
| 1000
| 1200
|
ƽ�ⳣ��
| 1.7
| 1.1
| 1.0
| 0.6
| 0.4
|
�ش��������⣺
(1).�÷�Ӧ��ƽ�ⳣ������ʽK=?��
(2).830��ʱ����һ��5 L���ܱ������г���0.20mol��A��0.80mol��B���練Ӧ��ʼ6s��A��ƽ����Ӧ����v(A)=0��003 mol��L-1��s-1������6sʱc(A)=??mol��L-1������Ӧ��һ��ʱ��ﵽƽ��ʱA��ת����Ϊ?�������ʱ����ܱ��������ٳ���1 mol�����ƽ��ʱA��ת����Ϊ?��
(3).1200��ʱ��ӦC(g)+D(g)  A(g)+B(g)��ƽ�ⳣ����ֵΪ?��
A(g)+B(g)��ƽ�ⳣ����ֵΪ?��
�ο��𰸣�(1) ��(2)0.022����80%����80%? (3)2.5
��(2)0.022����80%����80%? (3)2.5
��������������������1���÷�Ӧƽ�ⳣ������ʽΪ ��
��
��2��v(A)=��c(A)/t��AŨ�ȱ仯Ϊ0.003��6=0.018mol/L������6sʱA�����ʵ���Ũ��Ϊ(0.04��0.018)mol/L=0.022mol/L����ﵽƽ��ʱת����A�����ʵ���Ũ��Ϊxmol/L��
A(g)? +? B(g) C(g)+D(g)
C(g)+D(g)
ʼ(mol/L)0.04? 0.16
ƽ(mol/L)0.04��x? 0.16��x? x? x
830��ʱK=1��(0.04��x)(0.16��x) =x��x���x=0.032��
����A��ת����Ϊ0.032/0.04��100%=80%��������Һ���ٳ�������������Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���A��ת������Ϊ80%��
��3��C(g)+D(g)  A(g)+B(g)��A(g)+B(g)
A(g)+B(g)��A(g)+B(g) C(g)+D(g)ƽ�ⳣ����Ϊ������1200��ʱ��ӦC(g)+D(g)
C(g)+D(g)ƽ�ⳣ����Ϊ������1200��ʱ��ӦC(g)+D(g)  A(g)+B(g)��ƽ�ⳣ��K=1/0.4=2.5��
A(g)+B(g)��ƽ�ⳣ��K=1/0.4=2.5��
��������Ӧ������ﻥΪ�ߵ���ƽ�ⳣ����Ϊ������
�����Ѷȣ�һ��
2��ѡ���� �ظ������Һ�д�������ƽ�⣺Cr2O72-(�Ⱥ�ɫ)+H2O  2H++2CrO42-(��ɫ)����K2Cr2O7��Һ�м������������Լ�����Һ��ɫ��ӻ�ɫ��Ϊ�Ⱥ�ɫ
2H++2CrO42-(��ɫ)����K2Cr2O7��Һ�м������������Լ�����Һ��ɫ��ӻ�ɫ��Ϊ�Ⱥ�ɫ
A��NaHSO4
B��NaHCO3
C��Na2CO3
D��CH3COONa
�ο��𰸣�A
�����������Һ�ӻ�ɫ��Ϊ�Ⱥ�ɫ����Ӧ������С�A��HSO4�C�Ƕ�Ԫǿ���������ˮ��Һ��ˮ�������ϴ�HSO4-=H++SO42-��ʹ��Һ��H+Ũ������Cr2O72-(�Ⱥ�ɫ)+H2O  2H++2CrO42-(��ɫ)���淴Ӧ������У�����Һ��Ϊ�Ⱥ�ɫ��B��HCO3-����Һ�в���ˮ��HCO3-+H2O
2H++2CrO42-(��ɫ)���淴Ӧ������У�����Һ��Ϊ�Ⱥ�ɫ��B��HCO3-����Һ�в���ˮ��HCO3-+H2O H2CO3+OH-,H2O
H2CO3+OH-,H2O H++OH-��C��CO32-��ˮ��Һ�в���ˮ�⣬��Һ��CO32-+H2O
H++OH-��C��CO32-��ˮ��Һ�в���ˮ�⣬��Һ��CO32-+H2O  HCO3?+OH-,H++OH-?
HCO3?+OH-,H++OH-? H2O����Ӧ������У�D��CH3COO-+H+
H2O����Ӧ������У�D��CH3COO-+H+ CH3COOH����Ӧ������С�
CH3COOH����Ӧ������С�
�����Ѷȣ�һ��
3��ѡ���� һ���¶Ⱥ�һ������������·�Ӧ��A2(s)+2B2(g) 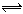 2AB2(g) �ﵽƽ��״̬�ı�־��? (? )
2AB2(g) �ﵽƽ��״̬�ı�־��? (? )
A��V����B2��==V�棨AB2��
B�������ڵ���ѹǿ����ʱ����仯
C����λʱ��������1molAB2��ͬʱ������1mol��B2
D�������ܶȲ�����ʱ��仯���仯
�ο��𰸣�AD
������������淴Ӧ�ﵽƽ��ı�־�������淴Ӧ������ȣ�A��ȷ����A2�ǹ��壬��Ӧǰ���������ʵ������䣬����������ƽ��״̬���Ƿ�ƽ��״̬���¶ȡ����һ��ʱ�����ڵ�ѹǿ�����䣬B��������AB2������B2��ָ����Ӧ�����淴Ӧ��C������A2�ǹ��壬�����������غ㣬����������̶����䣬���������ܶȲ��ٱ仯��ƽ��״̬��D��ȷ��
��������ѧƽ��״̬�ı�־�������淴Ӧ������ȡ�����ְٷֺ������ֲ��䡣ͬʱҪע�������ļ�ӱ�־��
�����Ѷȣ���
4��ѡ���� �ں��º��������У���������Щ���������ٷ����仯ʱ������A(g) + 2B(g)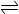 C(g) + D(g)�Ѵ�ƽ��״̬��
C(g) + D(g)�Ѵ�ƽ��״̬��
�ٻ�Ϧ������ѹǿ�ڻ��������ܶȢ�B�����ʵ���Ũ�Ȣܻ������������ʵ����ݻ�������ƽ����Է��������ަ�(C)���(D)�ı�ֵ����������������������������
A���٢ۢܢ�?B���٢ڢۢܢݢ�
C���٢ۢܢݢ�?D���٢ڢۢܢݢޢߢ�
�ο��𰸣�A
����������ٸ÷�Ӧ��һ����Ӧǰ����������仯�Ļ�ѧ��Ӧ����Ӧֻ�дﵽƽ��״̬ʱ�������������ѹǿ�ű��ֲ��䣬������֤���ﵽ��ƽ��״̬������ȷ���ڢߢ���������غ㶨��֪����Ӧǰ�����������ʼ�ղ��䣬������������䣬����������������ܶ�ʼ�ղ��䣬���Բ���֤���ﵽƽ��״̬���ʴ��ܷۢ�Ӧ����ƽ��״̬ʱ��ƽ��ʱ�����ʵ�Ũ�Ȳ��䣬�����������ʵ������䣬������֤���ﵽƽ��״̬������ȷ���ݷ�Ӧ��һ����Ӧǰ����������仯�Ļ�ѧ��Ӧ��ֻ�дﵽƽ��״̬ʱ������������ʵ����Ų��䣬��Ӧǰ�����������ʼ�ղ��䣬��ʱ��������ƽ����Է���������Ҳ�Ͳ��䣬������֤���ﵽƽ��״̬������ȷ���ަ�(C)���(D)�ı�ֵ��ʼ���Dz���ģ����Բ���֤���ﵽƽ��״̬���ʴ��ʴ�A��ȷ
�����Ѷȣ�һ��
5������� ��Ӧm A��n B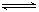 p C��ij�¶��´ﵽƽ�⡣
p C��ij�¶��´ﵽƽ�⡣
����A��B��C�������壬��ѹ������Ӧ����С���淴Ӧ���ʣ���m��n��p�Ĺ�ϵ��________________?��
����CΪ���壬��m?+ n = p���ڼ�ѹʱ��ѧƽ�ⷢ���ƶ�����ƽ��ض���______�����ƶ���
���������ϵ�����ӻ����B������ƽ����������ƶ�����B�϶�����Ϊ_____̬��
�ο��𰸣���m+n > P ����?����
�����������
�����Ѷȣ�һ��