微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 水的电离过程为H2O H++OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14,?KW(35℃)=2.1×10-14。则下列叙述正确的是
H++OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14,?KW(35℃)=2.1×10-14。则下列叙述正确的是
A.c(H+)随温度的升高而降低
B.35℃时,c(H+)>c(OH-)
C.溶液:pH(35℃)>pH(25℃)
D.水的电离是吸热的过程
参考答案:D
本题解析:
水在电离的过程中温度升高,有利于水的电离,它是一个吸热过程。纯水中c(H+)和c(OH-)都增大,电离常数K及水的离子积都增大,但纯水中c(H+)=c(OH-),故选D。
本题难度:简单
2、选择题 某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH( pOH=-lgc(OH-) )与pH的变化关系如图所示,则
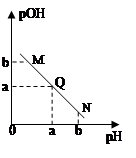
A.N点所示溶液中c(H+) < c(OH-)
B.M点所示溶液导电能力强于Q点
C.M点水的电离程度大于N点
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
参考答案:A
本题解析:向醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液的氢离子浓度逐渐减小,pOH减小。所以Q点溶液呈中性,M点溶液呈酸性,N点呈碱性。所以,A正确;B、Q点溶液强电解质溶液,M点溶液为弱酸,N点碱过量,所以导电能力N>Q>M;C、M点c(H+) = N点c(OH-),水的电离程度相同;D、Q点溶液呈中性,酸稍过量。
本题难度:一般
3、选择题 室温下pH、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
A.加水稀释2倍后,两溶液的pH均减小
B.使温度都升高20℃后,两溶液的pH均不变
C.加等量的水稀释后,醋酸溶液的pH较盐酸小
D.加足量的锌充分反应后,醋酸产生的氢气比盐酸多
参考答案:CD
本题解析:醋酸是一元弱酸,存在电离平衡,稀释促进电离。盐酸是一元强酸,A不正确,加水稀释2倍后,两溶液的pH均增大;升高温度促进醋酸的电离,其水的离子积常数也是增大,B不正确;C正确,再pH相等的条件下,醋酸的浓度大于盐酸的,所以醋酸生成的氢气多,D正确,答案选CD。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强强,在注重对学生基础知识的巩固和训练的同时,侧重对学生能力的培养和方法的指导与训练,有利于培养学生的逻辑推理能力和抽象思维能力。
本题难度:简单
4、选择题 常温下,测得柠檬水溶液的pH是3,其中的c(OH-)是(?)mol/L:
A.1x10-3
B.0.1
C.1x10-7
D.1x10-11
参考答案:D
本题解析:考查pH和水的离子积的有关计算。氢离子浓度的负对数称为pH,pH=3,则c(H+)=0.001mol・L-1,由水的离子积常数可得出c(OH-)=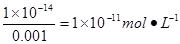 ,故答案选D。
,故答案选D。
本题难度:简单
5、选择题 常温常压下,充分燃烧一定量的甲烷放出热量222.575KJ,经测定完全吸收生成的二氧化碳需消耗1mol/L的NaOH溶液250mL,恰好生成正盐。则此条件下甲烷的燃烧热热化学方程式 ( )
A.CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H="-890.3" kJ/mol
B.1/2CH4(g)+O2(g)=1/2CO2(g)+H2O(l);△H="-222.575" kJ/mol
C.1/2CH4(g)+O2(g)=1/2CO2(g)+H2O(g);△H="-445.15" kJ/mol
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H="-890.3" kJ/mol
参考答案:D
本题解析:由NaOH的物质的量可以算出CO2的量,再由CO2的量算出甲烷的量,计算出1mol CH4充分燃烧放出的热量为890.3 kJ,则甲烷的燃烧热热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H="-890.3" kJ/mol。
本题难度:一般