微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质溶于水,不与CO2反应的是?(?)
A.AlCl3
B.NaAlO2
C.Na2SiO3
D.Na2CO3
参考答案:A
本题解析:略
本题难度:一般
2、选择题 关于 Al、Fe、Cu三种金属,下列说法正确的是
A.三者的单质均为银白色固体
B.三者都能与盐酸、稀硫酸反应
C.AlCl3、FeCl3、CuCl2均可作净水剂
D.制备Al 用电解法,制备Fe、Cu可用还原法
参考答案:D
本题解析:略
本题难度:简单
3、填空题 经精选后的铝土矿A(主要成份为Al2O3,含有一定量的Fe2O3、SiO2杂质),可用A来制备电解铝原料――氧化铝,某课外小组同学模拟该过程,设计了如下方案:
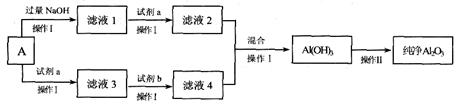
请回答:
(1)A中Al2O3与过量氢氧化钠溶液反应的化学方程式是________________
(2)操作I的名称是________________。
(3)下列说法中正确的是________(填选项)。
a 操作Ⅱ是灼烧? b. 滤液3所含阳离子是Fe3+、Al3+
c. 试剂b可用氢氧化钠? d. 为保证转化完全,所加试剂a和试剂b均应过量
(4)写出滤液2、4混合后生成Al(OH)3的离子方程式是______________________ __
参考答案:(7分)(1)Al2O3+2NaOH=2NaAlO2+H2O(2分)(2)过滤(1分)
(3)acd(2分)?(4)3AlO2-+Al3++6H2O=4 Al(OH)3↓?(2分)
本题解析:(1)氧化铝是两性氧化物,所以Al2O3与过量氢氧化钠溶液反应的化学方程式是Al2O3+2NaOH=2NaAlO2+H2O。
(2)由于氧化铁和氢氧化钠溶液不反应,所以所以从溶液中分离固体的实验操作名称是过滤。
(3)氢氧化铝灼烧即生成氧化铝,a正确;由于二氧化硅不能和盐酸反应,所以试剂a可以是盐酸,则滤液3中Fe3+、Al3+和氢离子,b不正确。将Fe3+、Al3+分离开的试剂可以是氢氧化钠溶液,c正确;为保证转化完全,所加试剂a和试剂b均应过量,d正确,答案选acd。
(4)滤液2中含有AlO2-,能和Al3+反应生成白色沉淀氢氧化铝,则滤液2、4混合后生成Al(OH)3的离子方程式是3AlO2-+Al3++6H2O=4 Al(OH)3↓。
点评:本题以流程图来呈现实验过程的探究性考题,是高考中的常见题型之一。读懂实验流程图,明确实验步骤和原理,是正确解答此类问题的前提,有利于激发学生的学习兴趣和学习积极性。
本题难度:一般
4、选择题 下列说法错误的是
[? ]
A.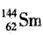 与
与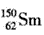 是同一种核素
是同一种核素
B.Al、Al2O3、Al(OH)3都可溶于NaOH溶液和盐酸中
C.甲烷燃烧放热,表明反应物的总能量大于生成物的总能量
D.向豆浆中加入硫酸钙制豆腐,是利用了胶体聚沉的性质
参考答案:A
本题解析:
本题难度:一般
5、选择题 镁和铝比较,下列说法不正确的是
[? ]
A.镁和铝都是银白色的轻金属
B.因为在反应中,铝原子失去三个电子,镁原子失去两个电子,所以铝的化学性质比镁的活泼
C.铝的硬度比镁的大,熔沸点比镁的高
D.常温下,镁和铝的表面都能生成一层致密而坚固的氧化膜,从而失去金属光泽并且有耐腐蚀性
参考答案:B
本题解析:
本题难度:简单