微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 烧过菜的来源:91 考试网铁锅未及时洗去含有NaCl的残液,过一段时间便出现红棕色的铁锈斑点,已知该锈斑为
Fe(OH)3失水的产物。
(1)请你表示此时Fe被腐蚀正极的电极反应式:__________________________
(2)Fe2+和NaOH溶液反应生成Fe(OH)2的离子方程式:________________________
(3)Fe(OH)2在潮湿的空气中转化为Fe(OH)3的化学方程式:________________________。
参考答案:(1)2H2O+O2+4e-=4OH-
(2)Fe2++2OH-=Fe(OH)2↓
(3)4Fe(OH)2+2H2O+O2=4Fe(OH)3
本题解析:
本题难度:一般
2、填空题 (3分) 对于反应2A(g)+B(g) 2C(g)+Q (Q>0),下列图象正确的是??
2C(g)+Q (Q>0),下列图象正确的是??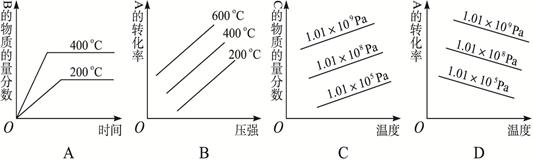
参考答案:AD
本题解析:略
本题难度:一般
3、选择题 以葡萄糖为燃料可以形成微生物燃料电池(酸性电解质体系中)。关于该电池的叙述正确的是
[?]
A.该电池能够在高温下工作
B.电池的负极反应为:?C6H12O6+6H2O?-?24e-=?6CO2↑+24H+?
C.放电过程中,H+从正极区向负极区迁移
D.在电池反应中,每消耗1mol氧气,理论上生成标准状况下CO2气体(22.4/6)L
参考答案:B
本题解析:
本题难度:一般
4、选择题 下列事实不能用原电池原理解释的是( )
A.将镁粉、铁粉和食盐一块加到水中迅速反应放热
B.铁被钝化处理后不易腐蚀
C.纯锌与稀硫酸反应时,滴入少量CuSO4溶液后反应速率加快
D.镀层破损后,镀锌铁比镀锡铁更耐用
参考答案:A、将镁粉、铁粉和食盐一块加到水中,构成原电池装置,金属镁是负极,镁和水的反应是放热反应,形成原电池可以加快化学反应速率,能用原电池原理解释,故A错误;
B、铁被钝化后,在金属表面上会形成一层致密的金属氧化膜,保护内部金属不被腐蚀,不能用原电池原理解释,故B正确;
C、纯锌与稀硫酸反应时,滴入少量CuSO4溶液后,金属锌可以和硫酸铜反应置换出铜,Zn、Cu、硫酸会形成原电此装置,Zn为负极,使得Zn和硫酸的反应速率加快,能用原电池原理解释,故C错误;
D、镀层破损后,镀锌铁和潮湿空气形成的原电池中,金属Zn为负极,Fe为正极,Fe被保护,镀锡铁和潮湿空气形成的原电池中,金属Fe为负极,Sn为正极,Fe被腐蚀速率加快,镀锌铁比镀锡铁更耐用,能用原电池原理解释,故D错误.
故选B.
本题解析:
本题难度:简单
5、选择题 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图。下列有关氢氧燃料电池的说法正确的是
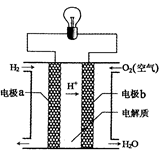
A.该电池的总反应:2H2+O2=2H2O
B.该电池中电极b是负极
C.外电路中电子由电极b通过导线流向电极a
D.该电池工作时电能转化为化学能