| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《热化学方程式》高频试题强化练习(2017年最新版)(八)
参考答案:C 本题解析:反应热就是断裂反应物中的化学键所吸收的能量与形成生成物化学键时所释放的能量的差。2H2(g)+O2(g)=2H2O(g) ΔH=-484 kJ/mol。且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H―O键形成时放出热量463 kJ,则氢气中1 mol H―H键断裂时吸收热量是2×H―H+496 kJ/mol-4×463 kJ/mol=-484 kJ/mol,解得H-H为436 kJ、mol,因此选项是C。 本题难度:一般 4、选择题 相同温度下,容积均恒为2L的甲、乙、丙3个密闭容器中发生反应: |
参考答案:D
本题解析:综合考虑甲乙丙三个容器均容积恒定,则可达等效平衡,Ar不影响平衡状态,而甲从正反应开始,乙和丙同时从正逆反应方向开始,所以放出的热量Q1>Q2>Q3=78.8kJ;结合乙容器中放出的热量,计算得反应的SO2为0.8mol, 2SO2(g) + O2(g)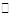 2SO3(g)
2SO3(g)
起始量(mol) 1.8 0.9 0.2
变化量(mol) 0.8 0.4 1.0
平衡量(mol) 1.0 0.5 1.0
由化学平衡常数的表达式:K=c2(SO3)/c(O2)×c2(SO2)=4,B项错误;达平衡时甲中SO2的转化率为50%,因为反应放热,当升高温度时,平衡向逆反应方向移动,其转化率减小。
考点:化学平衡状态、平衡常数、转化率、等效平衡。
本题难度:困难
5、选择题 已知甲烷燃烧生成二氧化碳和液态水放出的热量为55.625kJ・g-1。下列热化学方程式中不正确的是
[? ]
A.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H =-890kJ/mol
B.1/2 CH4(g)+O2(g)=1/2CO2(g)+H2O(l);△H =-445kJ/mol
C.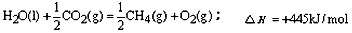
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-55.625kJ/mol
参考答案:D
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《化学与工农.. | |