��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪��CH3CH2CH2CH3(g)��6.5 O2(g)===4CO2(g)��5H2O(l)����H����2 878 kJ/mol (CH3)2CHCH3(g)��6.5
O2(g)===4CO2(g)��5H2O(l)����H����2 869 kJ/mol ����˵����ȷ����
[? ]
A����������Ӵ�������������춡�����
B����������ȶ��Դ����춡��
C���춡��ת��Ϊ������Ĺ�����һ�����ȹ���
D���춡������е�̼�����������Ķ�
2������� ��6�֣�����������N2H4Ϊȼ��,NO2Ϊ������,���߷�Ӧ����N2��ˮ����, ��֪
N2(g)+2O2(g)=2NO2(g)
3������� X��Y��Z��W��Ԫ�����ڱ���ǰ�����ڵij���Ԫ�أ��������Ϣ���±���
Ԫ��
| �����Ϣ
|
X
| X�Ļ�̬ԭ�Ӻ���3���ܼ����е��ӣ���ÿ���ܼ��ϵĵ��������
|
Y
| ˫ԭ�ӷ��ӵ����ڱ�״�����ܶ�Ϊ1.429g/L
|
Z
| ���ʼ��仯�������ɫ��ӦΪ��ɫ
|
W
| WԪ�ػ�̬ԭ�ӵ�M��ȫ������N��ֻ��һ������
|
��1��Xλ��Ԫ�����ڱ�λ��Ϊ�ڵ�__________���ڵ�_________�塣X��һ�ֵ����۵�ܸߣ�Ӳ�Ⱥܴ������ֵ��ʵľ������� ���塣
��2��X��Y�е縺�Խ�ǿ����(��Ԫ�ط��ţ� ��XY2�ĵ���ʽ�� �������д��� ��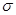 ����
����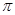 ���ĸ������� ��
���ĸ������� ��
��3��Z2Y2�к��еĻ�ѧ�������� ��W�Ļ�̬ԭ�Ӻ�������Ų�ʽ�� ��
��4���Ͼ�ӡˢ��·������W�ĵ���A����H2O2��H2SO4�Ļ����Һ���ܳ�ӡˢ��·���ϵ�A����֪��
��A(s)+H2SO4(aq) ="=" ASO4 (aq) + H2(g) ��H=+64.4kJ��mol-1
��2H2O2(l) ="=" 2H2O(l) + O2(g) ��H= -196.4kJ��mol-1
��H2(g)+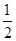 O2(g) ="=" H2O(l) ��H= -285.8kJ��mol-1
O2(g) ="=" H2O(l) ��H= -285.8kJ��mol-1
��д��A��H2SO4��H2O2��Ӧ����ASO4(aq)��H2O(l)���Ȼ�ѧ����ʽ(A�û�ѧʽ��ʾ)�� ��
4������� CH4?��һ����ࡢ��Ч�����������Ļ������ܵ�ȼ�ϣ���ȼ����Ϊ890.3KJ?mol-1����������Ϊȼ�ϵ�ص�ȼ�ϣ�
��1��д������ȼ�յ��Ȼ�ѧ����ʽ��______��
��2����֪H2��g����C��s����ȼ���ȷֱ���285.8KJ?mol-1��393.5KJ?mol-1����ӦC��s��+2H2��g��=CH4��g���ķ�Ӧ�ȡ�H=______��
��3���Լ��顢����������������ҺΪԭ�ϣ����Ե缫Ϊ�缫���Թ���ȼ�ϵ�أ��õ�صĸ�����ӦʽΪ��______��
��4���ã�3���е�ȼ�ϵ��Ϊ��Դ����ʯīΪ�缫���500ml���з�̪��NaCl��Һ��װ����ͼ��ʾ��
����д�������������������۲쵽������______��
�ڵ�ȼ�ϵ������2.8L?O2����״���£�ʱ�������ʱNaCl��Һ��pH=______��������Һ��������䣬����ȫ������Һ���ݳ�������Y��ͨ���ĵ��ӵ����ʵ���Ϊ��______��
�۵��֮��Ҫʹ��Һ�ָ�ԭ״��Ӧ������Һ�м�������______�������ƣ�����Һ��Cl-����______�����X����Y������
5������� ��Ҫ��д�Ȼ�ѧ����ʽ��
��1����֪ϡ��Һ�У�1mol?H2SO4��NaOH��Һǡ����ȫ��Ӧʱ���ų�114.6kJ������д����ʾH2SO4��NaOH��Ӧ���к��Ȼ�ѧ����ʽ______��
��2��25�桢101kPa�����³��ȼ��һ�����Ķ�������ų�����ΪQ?kJ�����ⶨ�������ɵ�CO2ͨ����������ʯ��ˮ�в���25g��ɫ������д����ʾ����ȼ���Ȼ�ѧ����ʽ______��
��3����֪�����Ȼ�ѧ����ʽ��
��CH3COOH��l��+2O2��g���T2CO2��g��+2H2O��l����H1=-870.3kJ/mol
��C��s��+O2��g���TCO2��g����H2=-393.5kJ/mol
��H2��g��+
O2��g���TH2O��l����H3=-285.8kJ/mol
д����C��s����H2��g����O2��g����������CH3COOH��l�����Ȼ�ѧ����ʽ______��