微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。制取铁酸钠的化学方程式如下:
(1)□Fe(NO3)3+□NaOH+□Cl2===□Na2FeO4+□NaNO3+□NaCl+□H2O
(2)在上述反应中 元素被氧化,当3molCl2参与反应时,转移电子的总数为 ;
(3)铁酸钠之所以能净水,除了能氧化杀菌外,另一个原因是 。
参考答案:(9分)
⑴(3分)2、16、3、2、6、6、8 (2)(4分)Fe(或铁)、 3.612×1024
(3)(2分)还原产物Fe3+与水反应生成Fe(OH)3胶体,能吸附杂质。
本题解析:(1)根据电子守恒配平铁从正三价升高到正六价转移3个电子,氯气从0价到负一转移2个电子,最小公倍数是6,即可配平。(2)中铁元素化合价升高失电子被氧化。3mol氯气到氯离子转移6mol电子既是3.612×1024 (3) 还原产物Fe3+与水反应生成Fe(OH)3胶体,胶体的比表面积比较大能吸附杂质。
考点:氧化还原反应的配平及相关概念。
本题难度:一般
2、选择题 金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以金红石为原料制取Ti的反应为:
aTiO2+bCl2+cC aTiCl4+cCO……反应①
aTiCl4+cCO……反应①
TiCl4+2Mg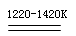 Ti+2MgCl2……反应②
Ti+2MgCl2……反应②
关于反应①②的分析不正确的是(? )
A.TiCl4在反应①中是还原产物,在反应②中是氧化剂
B.C、Mg在反应中均为还原剂,被氧化
C.每生成0.4 mol Ti,反应①②中共转移3.2 mol e-
D.反应①②都是置换反应
参考答案:D
本题解析:选项A,在反应①中TiCl4为还原产物,Cl2为氧化剂,在反应②中,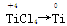 ,故TiCl4是氧化剂。选项B,还原剂被氧化。选项C,每生成0.4 mol Ti,反应①②中转移电子均为1.6 mol,共3.2 mol e-。选项D,反应①不是置换反应。
,故TiCl4是氧化剂。选项B,还原剂被氧化。选项C,每生成0.4 mol Ti,反应①②中转移电子均为1.6 mol,共3.2 mol e-。选项D,反应①不是置换反应。
本题难度:一般
3、填空题 (14分)Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
第一电离能
| 离子半径
| 熔点
| 酸性
|
Si S
| O2- Na+
| NaCl Si
| H2SO4 HClO4
|
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 mol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目 。
参考答案:
(1)第三周期,第ⅠA族 2,1s22s22p63s23p2
(2)<,>,<,<,
(3)4CuCl(s)+O2(g)=2CuCl2(2)+2CuO(s) △H=-177.6kJ/mol
(4)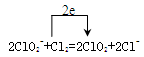
本题解析:(1)S的最外层有6个电子,为3s23p4,3p能级三个轨道、四个电子,依据泡利原理和洪特规则,先每个轨道排1个,方向相同,排满后再排,方向相反,故有两个孤对电子;硅,核电核数为14,根据构造原理可以排出。
(2)第一电离能同周期从左往右逐渐增大趋势,但有几个反常,故有Si<S;具有相同的电子层结构,核电荷越多半径越小,故有O2-<Na+;一般熔沸点原子晶体大于离子晶体;同周期从左到右非金属性逐渐增强,非金属性越强其最高价氧化物对应水化物的酸性越强。
(3)该反应为氧化还原反应,Cu从+1到+2价,O2做氧化剂,从0价到-2价。
(4)氯气做氧化剂从0价到-1价,亚氯酸根从+3到+4价。
考点:物质结构、元素及化合物性质、氧化还原反应、热化学反应方程式等
本题难度:一般
4、选择题 高氯酸铵(NH4ClO4)加热至483 K时,可完全分解成N2、Cl2、O2和H2O,则反应中氧化产物与还原产物的物质的量之比是
A.1∶1
B.1∶3
C.2∶1
D.3∶1
参考答案:D
本题解析:由题可知,高氯酸按分解的化学方程式配平2NH4ClO4 = N2+Cl2+ 2O2+ 4H2O?从而可知氧化产物与还原产物的物质的量之比(1+2)∶1?所以选D。
本题难度:一般
5、选择题 在一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则与1molCr3+反应所需PbO2的物质的量为……(?)
A.3.0mol
B.1.5mol
C.1.0mol
D.0.75mol
参考答案:B
本题解析:利用电子守恒,当1molCr3+被氧化为Cr2O72-(0.5mol)时,所失去的电子为3mol,这些电子被PbO2得到,而1molPbO2被还原只能得到2mol电子,因此所需PbO2的物质的量为1.5mol.
本题难度:一般