��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �ڸ�����ʴ�����У��������ֱ仯���ܷ������ǣ�������
��Fe��+2��תΪ+3��?
��O2����ԭ��
�۲���H2��
��Fe��OH��3ʧˮ�γ�Fe2O3-xH2O��
������̼��������
A���٢ڢۢ�
B��ֻ�ڢۢ�
C��ֻ�٢�
D���٢ڢۢܢ�
�ο��𰸣���������Ĺ����ǽ�����������������ʴ���������ⸯʴ����ԭ���ԭ������Ϊ����������ʧ���ӵ�������Ӧ��Fe-2e-=Fe2+���������������õ��ӷ�����ԭ��Ӧ��2H2O+O2+4e-=4OH-��O2����ԭ�����������Ի����£������ӵõ��ӵĹ��̣�����������������������ױ���������Ϊ����������4Fe��OH��2+O2+2H2O=4Fe��OH��3��Fe��+2��תΪ+3�ۣ����Fe��OH��3ʧˮ�γ�Fe2O3?xH2O����Ϊ����ijɷ֣�
��ѡA��
���������
�����Ѷȣ�һ��
2������� ��12�֣��о������ĸ�ʴ��������зdz���Ҫ�����塣
��1�����ĵ绯ѧ��ʴ�������֣������ָ�ʴ�ĸ�����Ӧ��Ϊ?����������Ӧ���������ˮĤ����Ծ�������ˮĤ��Ƚϸ�ʱ��������ӦʽΪ?�����ָ�ʴ��Ϊ?��ʴ����ˮĤ���Բ�ǿʱ��������ӦʽΪ?�����ָ�ʴ��Ϊ?��ʴ��
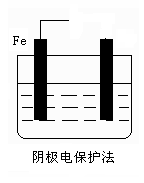
��2����ֹ������ʴ�ĵ绯ѧ���������֣���ͼ��Һ��Ϊ��ˮ������ͼ�����ӱ�Ҫ�ĵ��ߡ���Դ��ע����һ�缫�ĵ缫�������ƣ�ʹ�����ͼ����ע�ı���������
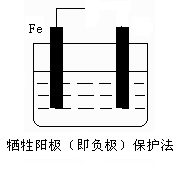 ?
?
�ο��𰸣���1�����缫��Ӧʽÿ��2�֣�����ÿ��1�֣�
Fe -2e�C =Fe2+?2H++ 2e�C = H2��?����?O2+2H2O+ 4e�C =4OH�C?����
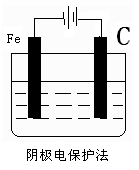
��2������ͼ2�֣�
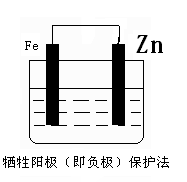 ?
?
�����������������ĸ�ʴ�����
��1�����������绯ѧ��ʴ����������ʧȥ���ӣ�����������Ӧʽ��Fe -2e�C =Fe2+ ����ˮĤ��Ƚϸ�ʱ���������ⸯʴ��������ӦʽΪ2H++ 2e�C = H2������ˮĤ���Բ�ǿʱ������������ʴ��������ӦʽΪO2+2H2O+ 4e�C =4OH�C��
��2���绯ѧ��ֹ������ʴ�ķ��������֣��ֱ���������������������������ӵ����������������������ͼ����Ҫһ�ֽ�����ǿ�����ģ�����п������ͼ����Ӧ�����������͵�Դ�ĸ���������������ȷ��ͼʾ�� ?
?
�����Ѷȣ�һ��
3��ѡ���� ��ѧ���������ճ�������������Ҫ��Ӧ�á�����˵������ȷ����

A�������ĸ�ʴ���̾���������ǵ绯ѧ��ʴ

B���ں������������п�飬�ɼ�������ĸ�ʴ����

C�����CuCl2������Һ�����ɽ���ͭ������

D�����MgCl2������Һ�����Ƶý���þ
�ο��𰸣�D
���������������ʴ�����ڵ绯ѧ��ʴ��A��ȷ��B����������������������������ȷ�����CuCl2������Һ�����������ӷŵ���������������ͭ���ӷŵ�����ͭ��C��ȷ��þ���ڻ����Խ�������ˮ��Һ��þ���Ӳ��ܷŵ磬ֻ�е������MgCl2�ſ��Ƶý���þ����D��
�����Ѷȣ�һ��
4��ʵ���� Zn��MnO2�ɵ��Ӧ�ù㷺����������Һ��ZnCl2��NH4Cl�����Һ��
(1)�õ�صĸ���������?����ع���ʱ����������?�������������������
(2)��ZnCl2��NH4Cl�����Һ�к�������Cu2���������ij�缫�ĸ�ʴ������Ҫԭ����?
?������ȥCu2+�����ѡ�������Լ��е�?������ţ���
a��NaOH? b��Zn? c��Fe? d��NH3��H2O
(3)MnO2����������֮һ����ʯīΪ�缫������ữ��MnSO4��Һ�������ĵ缫��Ӧʽ��?��������·��ͨ��2mol���ӣ�MnO2�����۲���Ϊ?�ˡ�
�ο��𰸣���1����450 ��ʱ��2molSO2�����1molO2������ȫ��Ӧ����2molSO3����ʱ�ų�������Ϊ190kJ��ûд����450��ʱ����1�֣�ûд�¶�ͨ����ָ��25�桱������2�֣�
��ʱ��2molSO2�����1molO2������ȫ��Ӧ����2molSO3����ʱ�ų�������Ϊ190kJ��ûд����450��ʱ����1�֣�ûд�¶�ͨ����ָ��25�桱������2�֣�
(2)2CO (g) + SO2 (g)="S" (s) +2CO2 (g) ?��H=-270kJ/mol��3�֣������κ�һ�����÷֣�
�����������
�����Ѷȣ���
5������� ��8�֣�[��ѧ����ѧ�뼼��]
��ͭ�к���������п������������Ƚ����������������ʣ������Ӧ������ʵ����������������ͭ��ҺΪ���Һ���õ��ķ����Դ�ͭ�ᴿ������������͵��Һ�н������л��պͺ����ⶨ���ش��������⣻
��1������һ����⾫�ƣ��������У�����ͭ��Ũ�Ȼ�?��ѡ�����䡢��С����
������������ɺԵ��Һ���д�����
��2����������ۺ����ã�
ϡ���ᴦ��������õ�������ϡ��Һ����д���ò���Ӧ�����ӷ���ʽ��?��
�������м������Ļƽ���λ��ս����Dz������й����ϣ��˽��һЩ�йؽ��֪ʶ�����������ǻ�ȡ��һЩ��Ϣ��
���
| ��Ӧ
| ƽ�ⳣ��
|
1
| Au + 6HNO3��Ũ��= Au(NO3)3 + 3NO2��+ 3H2O
| << 1
|
2
| Au3+ + 4Cl�� =? AuCl4��
| >>1
|
���п�֪������������ᷴӦ����ȴ��������ˮ��Ũ���������ᰴ�����l��3�Ļ����������Ҫ���ͽ��ܹ�������ˮ��ԭ��?��
��3�����Һ�����IJⶨ����ͼ�Ǹ�С��̽�����Һ��һ��ʵ�����̣�
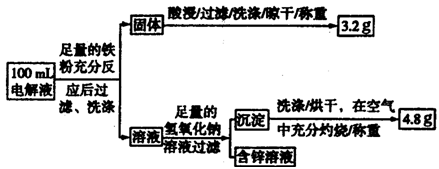
��100mL��Һ��Cu2+��Ũ��Ϊ?mol��L��1��Fe2+��Ũ��Ϊ?mol��L��1
�ο��𰸣�31����8�֣���1����С��1�֣���2��3Ag+4H++NO-3==3Ag++NO ��+2H2O��1�֣�
��3��Ũ�����к�����Cl-��Au3+��Cl-1�γ��ȶ�AuCl-4��ʹ��Ӧ2ƽ�������ƶ�����ʹ��Ӧ1���ҽ��У����������ˮ��2�֣�
��4��0.5 mol��L) 2�֣�0.6mol��L��2�֣�
���������
����������һ�����ݵ�⾫��ͭʱ�������������������ķ�Ӧ���ش�
���������1�����������Ժ�ϡ���ᷴӦ������������һ��������ˮ�����ݻ�ѧƽ���ƶ�ԭ�����������ܹ�������ˮ��ԭ��
��2�����ݻ�ѧ��Ӧԭ��������ش�
��𣺽⣺����һ���ڵ�⾫��ͭʱ��������Ӧ�ǽ���п������������ʧ���ӣ�����ʱ��������ͭ�����Ѿ��õ��ӣ���ͭ�����Ѿ���С�˶���δ�������ϲ���ͭ���ӣ��ʴ�Ϊ����С��
���������1�����������Ժ�ϡ���ᷴӦ������������һ��������ˮ����3Ag+4H++NO3-=3Ag++NO��+2H2O�����ݱ��е���Ϣ��Au+6HNO3��Ũ��=Au��NO3��3+3NO2��+3H2O������Au3++4Cl-=AuCl4-������ˮ�У�����Ũ�����Ũ���ᣬŨ���Ậ�д��������ӣ�Au3+�������������γ��ȶ���AuCl4-���ӣ�ʹ��Ӧ2ƽ�������ƶ������������ˮ�У�
�ʴ�Ϊ��3Ag+4H++NO3-=3Ag++NO��+2H2O��Ũ���Ậ�д��������ӣ�Au3+�������������γ��ȶ���AuCl4-���ӣ�ʹ��Ӧ2ƽ�������ƶ������������ˮ�У�
��2��100mL����Һ�к����������ӡ�ͭ���ӡ�п���ӣ������������Ľ���Fe�ԺὫ����ͭȫ���û��������������ɵ�3.2g������Cu������ͭ���ӵ�Ũ��c=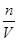 =
=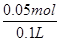 ="0.5" mol/L���������Ӻ��������Ʒ�Ӧ�����������������ڿ����и��ױ�����Ϊ�������������ȷֽ����ɵ���������������4.8g������ԭ���غ㣬�������ӵ����ʵ����ǣ�
="0.5" mol/L���������Ӻ��������Ʒ�Ӧ�����������������ڿ����и��ױ�����Ϊ�������������ȷֽ����ɵ���������������4.8g������ԭ���غ㣬�������ӵ����ʵ����ǣ�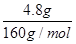 ��2
��2
=0.06mol�������������ӵ�Ũ��c=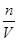 =
=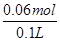 =0.6mol/L���ʴ�Ϊ��0.5��0.6��
=0.6mol/L���ʴ�Ϊ��0.5��0.6��
�����������漰�йص�⾫��ͭ����ѧƽ���ƶ�ԭ���Լ����ʵĺ����IJⶨ���ۺ�֪ʶ������Ƕȹ㣬�ѶȽϴ�
�����Ѷȣ�һ��