微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在容积固定的容器中发生反应:CO(g)+2H2(g) CH3OH(g)?△H<0,各物质的浓度如下表
CH3OH(g)?△H<0,各物质的浓度如下表

下列说法不正确的是(? )
A.2min-4min内用氢气表示的速率为0.3mol/(L?min)
B.达平衡时,CO的转化率为62.5%
C.反应在第2min时改变了条件,可能是加入了催化刺
D.反应在第2min时改变了条件,可能增加了H2的浓度
2、简答题 [15分]甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
反应过程
| 化学方程式
| 焓变△H
(kJ/mol)
| 活化能Ea
(kJ/mol)
|
甲烷氧化
| CH4(g)+2O2(g) CO2(g)+2H2O(g) CO2(g)+2H2O(g)
| -802.6
| 125.6
|
CH4(g)+O2(g) CO2(g)+2H2(g) CO2(g)+2H2(g)
| -322.0
| 172.5
|
蒸汽重整
| CH4(g)+H2O(g) CO(g)+3H2(g) CO(g)+3H2(g)
| 206.2
| 240.1
|
CH4(g)+2H2O(g) CO2(g)+4H2(g) CO2(g)+4H2(g)
| 165.0
| 243.9
|
回答下列问题:
(1)反应CO(g)+H2O(g) CO2(g)+H2(g)的△H=?kJ/mol。
CO2(g)+H2(g)的△H=?kJ/mol。
(2)在初始阶段,甲烷蒸汽重整的反应速率?甲烷氧化的反应速率(填大于、小于或等于)。
(3)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可以平衡常数(记作KP),则反应CH4(g)+H2O(g) CO(g)+3H2(g)的KP=?;
CO(g)+3H2(g)的KP=?;
随着温度的升高,该平衡常数?(填“增大”、“减小”或“不变”)。
(4)从能量阶段分析,甲烷自热重整方法的先进之处在于?。
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如下图:
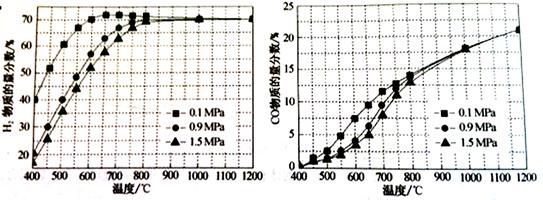
①若要达到H2物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是?。
A.600℃,0.9Mpa? B.700℃,0.9MPa? C.800℃,1.5Mpa? D.1000℃,1.5MPa
②画出600℃,0.1Mpa条件下,系统中H2物质的量分数随反应时间(从常温进料开始即时)
的变化趋势示意图:
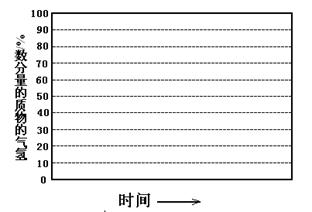
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是?。
3、选择题 恒温恒容的条件下,在密闭容器中按不同方式投入反应物,均达到平衡,测得平衡时的有关数据如下(已知:N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ/mol)
2NH3(g)△H=-92.4kJ/mol)

下列说法一定正确的是
[? ]
?①c1=c2?②c3=2c2?③Q1=?Q2?④Q1+Q2=92.4?⑤P1=P2?⑥a2>a3?
A.①④⑤⑥?
B.①③⑤⑥?
C.①②③⑥?
D.②③⑤⑥
4、选择题 下列四个数据是在不同条件下测出的合成氨反应的速率,其中最快的是
[? ]
A.v(H2)==0.1 mol/(L・min)
B.v(N2)==0.1mol/(L・min)
C.v(NH3)==0.15mol/(L・min)
D.v(N2)==0.002mol/(L・s)
5、填空题 (10分)在一定条件下的下列可逆反应达到平衡时,试填出:xA+yB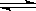 zC
zC
(1)若A、B、C都是气体,增大压强,平衡向正反应方向移动,则x+y与z关系是_____?__;
(2)若A、C是气体,且x+y=z,在加压时化学平衡可发生移动,则平衡必定是向?方向移动;
(3)若B、C是气体,A是固体,增大A的浓度,平衡?(填“正向移动”、“逆向移动”或“不移动”);
(4)若升高温度后,C的百分含量减小,则正反应是?(填“吸热”或“放热”)反应。
(5)若该可逆反应达到平衡时加入催化剂,平衡?(填“正向移动”、“逆向移动”或“不移动”);