��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
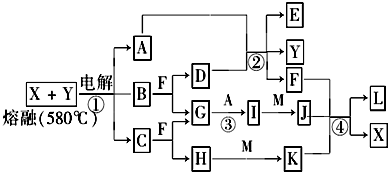
1������� ��ͼ��ʾ������֮���ת����ϵ������A��B��C��GΪ���ʣ���Ϊ��ҵ�����г�����Ӧ��E��һ�־���Ư�����õ��Σ�Y�׳��⣬M��һ�����Ի����L��һ�ְ�ɫ������
����������й����⣺
��1��M�Ļ�ѧʽΪ______��Y��ʵ�����е���;��______���о�һ�У�
��2��X���۵�Ϊ801�棬ʵ�ʹ�ҵұ���г�������һ������Y���ۣ����빤ҵ����������Ŀ�ģ�______����ҵ�����У����������Ե缫���X��F�Ļ����÷�Ӧ�������缫��ӦʽΪ______��
��3����Ӧ�ڵĻ�ѧ����ʽ��______��
��4����Ӧ�ܵ����ӷ���ʽ��______��
�ο��𰸣���ͼ�б�ʾ������֮���ת����ϵ��A��B��C��GΪ���ʣ�����A��GΪ���壬FΪҺ�壮��Ϊ��ҵ�����г�����Ӧ��E��һ�־���Ư�����õ��Σ��ƶ�ΪCa��ClO��2��Y�׳��⣬��������������ƶ�ΪCaCl2�����ת����ϵ��֪��FΪH2O��AΪCl2��DΪCa��OH��2��B+F��H2O��=D��Ca��OH��2��+G���ƶ�BΪCa��GΪH2��IΪHCl��M��һ�����Ի����L��һ�ְ�ɫ��״�������ж�LΪAl��OH��3��MΪAl2O3��JΪAlCl3���������������ƶ�KΪƫ�����Σ�HΪ�CΪNa��HΪNaOH�����������õ�����Ca��Na��Cl2��˵��X��YΪNaCl��CaCl2��
��1��������������֪MΪAl2O3��YΪCaCl2��������ˮ�ԣ���������������ʴ�Ϊ��Al2O3���������
��2��X���۵�Ϊ801�棬ʵ�ʹ�ҵұ���г�������һ������Y���ۣ���ҵ����������Ŀ���ǣ�����X��Y�ۻ�ʱ���¶ȣ���Լ��Դ�� �������õ��X��F�Ļ����Ϊ����ʳ��ˮ����ȡCl2��H2��NaOH�������缫��ӦʽΪ2Cl--2e-=Cl2�����ʴ�Ϊ������X��Y�ۻ�ʱ���¶ȣ���Լ��Դ��2Cl--2e-=Cl2����
��3�������жϷ�Ӧ���ǹ�ҵ��Ư�۵ķ�Ӧ����Ӧ�Ļ�ѧ����ʽ�ǣ�2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��
�ʴ�Ϊ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��
��4����Ӧ�������κ�ƫ��������ˮ��Һ�е�˫ˮ�ⷴӦ��������������������Ӧ�����ӷ�Ӧ����ʽ�ǣ�Al3++3AlO2-+6H2O=4Al��OH��3����
�ʴ�Ϊ��Al3++3AlO2-+6H2O=4Al��OH��3����
���������
�����Ѷȣ�һ��
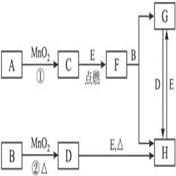
2���ƶ��� ��ͼ���漰�����ʾ�Ϊ��ѧ��ѧ�еij������ʣ�����CΪO2��DΪCl2��EΪFe���ʣ�����Ϊ��������Ǵ�������ת����ϵ����Ӧ�����ɵ�ˮ����Ҫ���������ȥ��
��1��д���й����ʵ����ƻ�ѧʽ��
B_______________��F__________________��H____________________��
��2��ָ��MnO2����ط�Ӧ�е����ã���Ӧ������_________������Ӧ������__________����
��3������Ӧ�����ڼ��������½��У���A��_____________������Ӧ�����ڳ��������½��У���A��_____________��
��4��д��B��MnO2���Ȼ��D�Ļ�ѧ����ʽ��__________________________________��
�ο��𰸣�(1)ŨHCl? Fe3O4? FeCl3? (2)��?����? (3)KClO3? H2O2?
(4) 4HCl+MnO2 MnCl2+H2O+Cl2
MnCl2+H2O+Cl2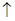
���������AΪH2O2��BΪŨ���CΪO2��DΪCl2��EΪFe��FΪFe3O4��GΪFeCl2��HΪFeCl3��
��2����Ӧ��Ϊ��������ֽ���������MnO2��Ϊ�������ӿ췴Ӧ�Ľ��С���Ӧ���У�MnO2��Ϊ����������Ũ���ᷴӦ�Ʊ�������
��3��CΪO2��ʵ�����Ʊ������ķ���ʽ���漰��MnO2���м���KClO3�ֽ���������H2O2�ֽ���������
��4����ѧ����ʽΪ 4HCl+MnO2 MnCl2+H2O+Cl2
MnCl2+H2O+Cl2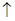
���������ƶ���������ۺϿ������������Ʊ��Լ��������Ʊ��������е��⡣���ƶ���Ľ��Ӧע��Ѱ��ͻ�ƿڡ�
�����Ѷȣ�һ��
3��ʵ���� ij����ұ�����Ĺܵ������к���̿�ڼ�����ͭ��п�����ۺ�ʵ���С���ͬѧ����˴ӹܵ������л��ս���ͭ�����÷����еĶ��������Ʊ������ʵ�鷽����ʵ�������ͼ��ʾ��
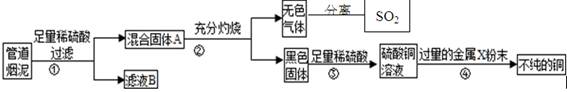
��ش�
��1��������У����˲���ʹ���˲���������������?�����ȷ�������Ѿ�����?��
��2��������У�������Ľ���X��Zn�Ļ��˳����Zn��X������X���й㷺��;��X��?���йط�Ӧ�Ļ�ѧ����ʽ?��
��3����ȥ����ͭ�е����ʽ���X����ѡ�õ��Լ�����Ʒ��?�����ţ���
a������? b��ϡ����? c������ˮ? d���Ȼ�ͭ��Һ��
��4�����������SO2ͨ�����е�ѭ�����չ��̼�����H2SO4,������ȡH2�����������£�
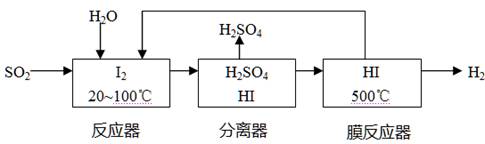
��д����Ӧ����Ĥ��Ӧ���еĻ�ѧ��Ӧ����ʽ?��??��
�ο��𰸣���10�֣����� ��ȡ��ҺB����п���������ݲ�����˵������������𰸺�������
Fe �� Fe+CuSO4==FeSO4+Cu ��2�֣���? a b d
SO2+2H2O+I==H2SO4+2HI ��2�֣���? 2HI==H2��+I2��2�֣�
�����������1���ڹ��˲����в����������������ã��Է�ֹҺ��ɽ�������п�Ļ������ǰ��ͭ�Ļ�����������ͭп�������ϡ���ᷴӦʱ��ͭ���ܲ��뷴Ӧ��̼Ҳ���ܷ�Ӧ����п��ϡ���ᷴӦ����������п�����Թ���ʱ��Һ������п������A��ͭ��̿�ڵĻ���
��2�����������̼�������ɶ�����̼��ͭ������������ͭ������ͭ�������ת��������ͭ����Һ������ͭ�ӹ�����xͭ˵��x�Ļ�Ա�ͭǿ������������X��Zn�Ļ��˳����Zn��X������X���й㷺��;֪X�ǽ���������Ӧ����������ͭ�����û���Ӧ������ʽΪ��CuSO4+Fe�TCu+FeSO4��
��3���������Ϲ������õIJ�����ͭ��ͭ��δ��Ӧ�����ۣ�ͭ���������ı��棬�ô��������ͼ��Ȼ�ͭʱ��ԭ�����У���ʵ�ʲ���������ɣ�����ϡ����ʱͭ���ܷ�Ӧ�����ܣ�����ܷ������ߣ�����������ˮ���ܷ������ߡ�
������������һ���������Դ�����⣬����ķ����Ƕ���Ʒ������漰�Ļ�ѧ��ӦҪ����ȷ���������Է�Ӧ�������������жϣ������������Ի���ʵ���⡣
�����Ѷȣ�һ��
4���ƶ��� ��Ϣʱ�������Ĵ������������Ի��������˼������в��ij�����Ϊ����ѧ��̽��С�齫һ����������·��������õ��ĺ�ɫ����M�ͽ���E�������¿�ͼ��ʾת������ø�Ч��ˮ��K2EO4.(����ʱ����ѧʽ����ѧ����ʽ�е�M��E��������Ӧ��Ԫ�ط��ű�ʾ)��

��1��д��M����ϡH2SO4��H2O2���Һ�����ӷ���ʽ??��
��2������X�������ӵķ�����������?��
��3��ijͬѧȡX����Һ�ڿ����з��ú��ữ������KI�͵�����Һ����Һ��Ϊ��ɫ���������ӷ���ʽ��ʾ��Һ��Ϊ��ɫ��ԭ��?��
��4����MSO4����ɫ��Һ��һϵ�в������Ի����ɫ���壬��Щ�������õ���ʵ���������˾ƾ��ơ��ձ�����������©��������̨�⣬����Ҫ�õ��Ĺ�����������?(��д��������)��
��5��ijͬѧ����H2��ԭMO���ⶨM�����ԭ����������ͼ�Dzⶨװ��ʾ��ͼ��A���Լ������ᡣ

��װ��D������?��
�����Ӻ�װ�ò�����װ�õ������Ժ�Ӧ���ȡ����ȷ�Ӧ��E�����ǡ���Aƿ����μ���Һ�塱? ?��������֮�仹Ӧ���еIJ�����??��
�۸�ʵ������Ƿ��в���֮����������ָ�����Ľ�����û�б��ʿɲ���
��6����˵��K2EO4��������Ч��ˮ����ԭ��?��
�ο��𰸣���17�֣���1��Cu��H2O2��2H����Cu2����2H2O ��2�֣�
��2��ȡX��Һ�������Թ��У����뼸��KSCN��Һ����Һ���Ժ�ɫ�������Թ��м��뼸��������ˮ����Һ�Ժ�ɫ����2�֣�
��3��2Fe3+ + 2I-��2Fe2+ + I2?��2�֣���4��������2�֣�
��5��������ˮ����������H2��2�֣�?�ڴ�Aƿ����μ���Һ�壨1�֣�?����H2�Ĵ��ȣ�1�֣�
���в��㣨1�֣���δ����β�����������þƾ��ƽ�δ��Ӧ������ȼ�յ�����2�֣�
��6��������ؾ���ǿ�����ԣ�ɱ������������ԭΪFe3+��Fe3+ˮ������ɵ��������������־��н�ǿ�������ԣ����������ؿ�������Ч��ˮ����
�����������1��M�Ǻ�ɫ��������M��ͭ��˫��ˮ����ǿ�����ԣ���ϡ������Һ���ܰ�ͭ������������ͭ����˫��ˮ�Ļ�ԭ������ˮ����Ӧ�����ӷ���ʽ��Cu��H2O2��2H����Cu2����2H2O��
��2��Y�ܺ�KSCN��Һ��Ӧ����Һ�Ժ�ɫ������Y�к��������ӣ����E�ǽ���������������ͭ��Ӧ����ͭ��������������X�������������������Ӿ��л�ԭ�ԣ��ݴ˿��Լ��飬������X�������ӵķ�����������ȡX��Һ�������Թ��У����뼸��KSCN��Һ����Һ���Ժ�ɫ�������Թ��м��뼸��������ˮ����Һ�Ժ�ɫ��
��3���������Ӿ��л�ԭ�ԣ��ڿ������ױ��������������ӣ������Ӿ��������ԣ��ܰѵ⻯���������ɵ��ʵ⣬������������ɫ����Ӧ�����ӷ���ʽ��2Fe3+ + 2I-��2Fe2+ + I2��
��4��������ͭ��Һ�еõ�����ͭ����IJ��������������˾ƾ��ơ��ձ�����������©��������̨�⣬����Ҫ�õ��Ĺ���������������
��5����Bװ�����Ʊ������ģ����������ӷ����������ɵ������к����Ȼ����ˮ���������Cװ����ʢ�б���ʳ��ˮ�������Ȼ��⣬Dװ����ʢ��Ũ���ᣬ����ˮ����������������
������װ���л����п�����ʵ��ǰ��Ҫ���������ž��������������ȴ�Aƿ����μ���Һ�塣����Ϊ�����ǿ�ȼ�����壬��ȼǰ��Ҫ���������Ĵ��ȣ�������������֮�仹Ӧ���еIJ����Ǽ��������Ĵ��ȡ�
�����������ǿ�ȼ�����壬���������ŷŵ������У����Ը�װ�ô��ڲ��㣬�Ľ��ķ������þƾ��ƽ�δ��Ӧ������ȼ�յ����ɡ�
��6�����ڸ�����ؾ���ǿ�����ԣ�ɱ������������ԭΪFe3+��Fe3+ˮ������ɵ��������������־��н�ǿ�������ԣ����������ؿ�������Ч��ˮ����
�����Ѷȣ�����
5���ƶ��� ���п�ͼ�漰������������Ԫ���У���һ��Ԫ���⣬�����Ϊ1��18��Ԫ�ء���֪��A��FΪ��ɫ���嵥�ʣ�BΪ���д̼�����ζ�����壬CΪ��ɫ�����EΪ��ɫ�������ʣ����ַ�Ӧ�IJ���δ��ȫ����
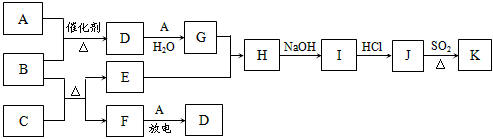
��ش���������
��1��B�ĵ���ʽΪ_________________��
��2��J��K��ͬ�ֽ������Ȼ����KΪ��ɫ������д��SO2��ԭJ����K�����ӷ���ʽ_________________________________��
��3������β���г�����D��B�ڼ��Ⱥʹ������ڵ�������������D����Ⱦ����֪��
��4NH3(g)��5O2(g) 4NO(g)��6H2O(g) ��H����905 kJ��mol-1
4NO(g)��6H2O(g) ��H����905 kJ��mol-1
��4NH3(g)��3O2(g) 2N2(g)��6H2O(g) ��H����1268 kJ��mol-1
2N2(g)��6H2O(g) ��H����1268 kJ��mol-1
��B��D��Ӧ���Ȼ�ѧ����ʽΪ________________________��
��4��������Ϊ�������滯ѧ���о��ɹ���ʹB��D�ķ�Ӧ�ڴ����������ʱ��Ч�ʴ����ߣ��Ӷ�ʹ��Ⱦ��D��ת���ʴ����ߡ�����Ӧ�û�ѧ�������۶Դ˹۵�������ۣ�___________________________
�ο��𰸣���1��
��2��2Cu2++2Cl-+SO2+2H2O==2CuCl��+4H++SO42-
��3��6NO��g��+4NH3��g��==5N2��g��+6H2O��g�� ��H=-1812.5 kJ��mol-1
��4�����о�ֻ�����ѧ��Ӧ���ʣ�����ʹ��ѧƽ�ⷢ���ƶ�
���������
�����Ѷȣ�һ��