微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 (12分)有A、B两种常见化合物组成混合物,其焰色反应均为黄色,其相互转化关系如图(其他物质均略去)。
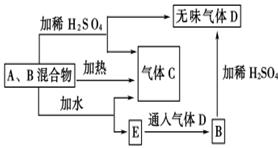
根据以上关系,回答下列问题:
(1)写出A、B、C、D的化学式:A_______, B__________,C________,D________。
(2)写出混合物中加水反应的化学方程式:?
_________________________________________________________________。
参考答案:(每空2分)
(1)Na2O2 NaHCO3 O2 CO2
(2)2Na2O2+2H2O===4NaOH+O2↑?NaOH+NaHCO3===Na2CO3+H2O
本题解析:略
本题难度:一般
2、填空题 已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:
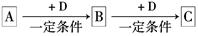
(1)若A能使湿润的红色石蕊试纸变蓝;C为红棕色气体。则A转化为B反应的化学方程式为?。
(2)若D是金属,C溶液在贮存时应加入少量D,其理由是(用必要的文字和离子方程式说明)?。
(3)若D是一种常见的温室气体,A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子,固体C受热分解可得固体B,该反应的化学方程式是?。
(4)若D为氯碱工业的主要产品,B具有两性,则B转化为C的离子方程式为?。
(5)若A、B、C均为氧化物,D是一种黑色固态非金属单质,则元素D在周期表中的位
置是?,B分子的结构式为?。
参考答案:(1)4NH3 + 5O2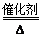 4NO + 6H2O(2)防止Fe2+被氧化,2F3+ + Fe = 3Fe2+(3)2NaHCO3
4NO + 6H2O(2)防止Fe2+被氧化,2F3+ + Fe = 3Fe2+(3)2NaHCO3 Na2CO3 + H2O +CO2↑(4)Al(OH)3 + OH- = AlO2- + 2H2O(5)第2周期、第ⅣA族,O=C=O
Na2CO3 + H2O +CO2↑(4)Al(OH)3 + OH- = AlO2- + 2H2O(5)第2周期、第ⅣA族,O=C=O
本题解析:A和D反应生成B,B和D反应生成C,则B和C中含有的某种共同元素是变价元素。
(1)若A能使湿润的红色石蕊试纸变蓝,则A是NH3,C为红棕色气体NO2,NH3和D能反应生成B,则B是NO,D是O2,A转化为B的反应方程式为4NH3+5O2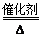 4NO+6H2O(2)D是金属,C溶液在贮存时应加入少量D,说明C易被氧化而变质,则A为Cl2,B为FeCl3,C为FeCl2,D为Fe,在亚铁离子溶液中加入的理由防止Fe2+被氧化,离子方程式2F3+ + Fe = 3Fe2+(3)若D是一种常见的温室气体,则D是二氧化碳,A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子,则A是NaOH,则B为Na2CO3,C为NaHCO3,B转化为C的离子方程式为CO2+CO32-+H2O=2HCO3-(4)D为氯碱工业的主要产品为NaOH,B具有两性推断为Al(OH)3;则C溶液是Al(OH)3和NaOH反应生成NaAlO2,离子方程式Al(OH)3 + OH- = AlO2- + 2H2O(5)若A、B、C均为氧化物,D是一种黑色固态非金属单质,推断为D为C,B为CO2,C为CO,则元素D在周期表中的位置是第2周期、第IVA族,B分子的结构式为O=C=O。
4NO+6H2O(2)D是金属,C溶液在贮存时应加入少量D,说明C易被氧化而变质,则A为Cl2,B为FeCl3,C为FeCl2,D为Fe,在亚铁离子溶液中加入的理由防止Fe2+被氧化,离子方程式2F3+ + Fe = 3Fe2+(3)若D是一种常见的温室气体,则D是二氧化碳,A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子,则A是NaOH,则B为Na2CO3,C为NaHCO3,B转化为C的离子方程式为CO2+CO32-+H2O=2HCO3-(4)D为氯碱工业的主要产品为NaOH,B具有两性推断为Al(OH)3;则C溶液是Al(OH)3和NaOH反应生成NaAlO2,离子方程式Al(OH)3 + OH- = AlO2- + 2H2O(5)若A、B、C均为氧化物,D是一种黑色固态非金属单质,推断为D为C,B为CO2,C为CO,则元素D在周期表中的位置是第2周期、第IVA族,B分子的结构式为O=C=O。
本题难度:一般
3、简答题 用右图所示装置进行实验,将A逐滴加入B中;
(1)若A为浓硫酸,B为第三周期金属元素的片状单质,其在常温下难与水反应;C为品红溶液,实验中观察到溶液褪色,则B是______(写化学式),B与浓H2SO4反应的化学方程式为______;反应后往烧杯中加入沸水,又可观察到试管C中的现象为______.
(2)若B为Na2CO3,C为C6H5ONa溶液,实验中观察到小试管内溶液变浑浊,则酸A应具有的性质是______.然后往烧杯中加入沸水,可观察到试管C中的现象是______.
(3)若B是生石灰,实验中观察到C溶液先形成沉淀,然后沉淀溶解,当溶液恰好澄清时,关闭E,然后往烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,则A是______(写名称),C是______(写化学式)与葡萄糖的混合液.该反应的离子方程式为______,仪器D在此实验中的作用是______.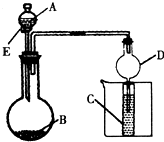
参考答案:(1)由题意可知,B为第三周期金属元素的片状单质,其在常温下难与水反应,B可能为铝活着镁,但浓硫酸常温下会使铝钝化,所以B只能为镁,与浓硫酸发生氧化还原反应,反应的方程式为Mg+2H2SO4(浓)=MgSO4+SO2↑+2H2O,SO2具有漂白性,可使品红褪色,但不稳定,加热又能恢复到原来的颜色,
故答案为:Mg;Mg+2H2SO4(浓)=MgSO4+SO2↑+2H2O;C中溶液变红;
(2)观察到小试管内溶液变浑浊,说明生成二氧化碳,则A的酸性应比碳酸的酸性强,生成苯酚易溶于热水,加热溶液变澄清,
故答案为:酸性比碳酸的酸性强;溶液由浑浊变澄清;
(3)试管壁出现光亮的银镜,说明生成氨气,可用浓氨水或铵盐的浓溶液与生石灰反应制取,C中应为葡萄糖与银氨溶液的反应,则C中应为AgNO3和葡萄糖的混合液,加热时发生:CH2OH(CHOH)4CHO+2[Ag(NH3)2]++2OH-水溶
本题解析:
本题难度:一般
4、填空题 A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件及部分产物未列出)。
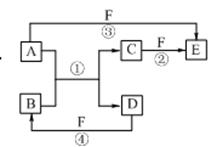
(1)若A是常见金属单质,与B的水溶液反应生成C和D。D、F是气体单质,D在F中燃烧时发出苍白色火焰。则F所对应的元素在周期表位置是?;反应②(在水溶液中进行)的离子方程式为?。
(2)若A、D为短周期元素组成的固体单质,A为金属,D为非金属。且③④两个反应都有红棕色气体生成,则反应①、④的化学方程式分别为
①??;④??。
(3)若A、D、F都是短周期非金属单质,且A、D所含元素同主族,A、F所含元素同周期,C是一种能与血红蛋白结合的有毒气体;则物质B的晶体类型是?,分子E的结构式是?。
参考答案:(1)第3周期第ⅦA族,2Fe2++Cl2=2Fe3++2Cl-
(2)①2Mg+CO2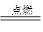 2MgO+C(条件不写得1分)
2MgO+C(条件不写得1分)
④C+4HNO3(浓)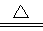 CO2↑+4NO2↑+2H2O(条件不写得1分)
CO2↑+4NO2↑+2H2O(条件不写得1分)
(3)原子晶体?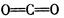
本题解析:(1)若A是常见的金属单质,反应①是置换反应,D、F是气态单质,根据框图可知,A与F生成E,C与F也能生成E,因此A只能为Fe,D为H2,F为Cl2,B为HCl,C为FeCl2,E为FeCl3。
(2)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子核外最外层电子数D是A的2倍,反应①是置换反应,根据框图可知,A为Mg,D为C,B为CO2,C为MgO,又知③和④两个反应中都有红棕色气体生成,F为HNO3。
(3)若A、D、F都是非金属单质,反应①是置换反应,A、D同主族,根据框图可知,A与F生成E,C与F也能生成E,因此只能是SiO2与C反应,则A是C、B是SiO2、C是CO、D是Si,E是CO2、F是O2。
本题难度:一般
5、推断题 物质X、Y、Z有如下转化关系:
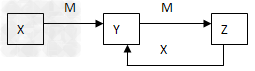
请回答下列问题:
(1)若X、Y、Z中均含有铝元素,则Y的化学式是____________,实验室用明矾制取该物质的离子方程式为___________________。
(2)若M是某元素的最高价氧化物且为气态,此元素的最高价与最低价化合价代数和为0?,X是由电子数均为10的阴阳离子组成,则Y溶液中离子浓度大小的顺序为___________________________。
(3)?若X为黄绿色气体,M是常见金属。完成下列问题:
①?X能与石灰乳反应制取漂白粉,其离子方程式_________________
②含M的一种盐可以作为杀菌消毒、净水剂,其一种制备方法是:以M(OH)3、NaClO和KOH为原料,请写出此反应的离子方程式___________________
③M(OH)3溶液中存在如下的沉淀溶解平衡:M(OH)3(s) M3+?(aq)?+?3OH-(aq)? 常温下,M(OH)3的溶度积Ksp?=?4.0?×?10-38,要使M3+离子浓度降至10-5mol/L,溶液的PH应调至_________。?(lg2=0.3,lg5=0.7)
M3+?(aq)?+?3OH-(aq)? 常温下,M(OH)3的溶度积Ksp?=?4.0?×?10-38,要使M3+离子浓度降至10-5mol/L,溶液的PH应调至_________。?(lg2=0.3,lg5=0.7)
参考答案:(1)Al(OH)3;Al3+?+?3NH3・H2O?=?Al(OH)3↓+?3NH4+
(2)c(Na+)?>?c(CO32-)?>?c(OH-)?>?c(HCO3-)?>?c(H+)
(3)①?Cl2?+?Ca(OH)2?=?Ca2+?+?ClO-?+?Cl-?+?H2O;②?2Fe(OH)3?+?3ClO-?+?4OH-?=?2FeO42-+3Cl-?+?5H2O;③3.2
本题解析:
本题难度:一般