微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 检验SO2中是否混有CO2气体,可采用的方法是
A.通过品红溶液,若品红溶液褪色,则说明混有CO2气体
B.通过澄清石灰水,若变混浊,则说明混有CO2气体
C.先通过足量NaOH溶液,再通过澄清石灰水,若变混浊,则说明混有CO2气体
D.先通过足量KMnO4溶液(具有强氧化性),再通过澄清石灰水,若变混浊,则说明混有CO2气体
参考答案:D
本题解析:A不正确,只能说明含有SO2,因为CO2不能使品红溶液褪色。B不正确,因为SO2也能使澄清的石灰水反应,变混浊。C不正确,因为SO2和CO2都能被氢氧化钠溶液吸收。D正确,SO2首先被氧化,排除其干扰,答案选D。
本题难度:一般
2、选择题 能符合如下图所示的转化关系的元素是?

A.硅
B.硫
C.铜
D.铁
参考答案:B
本题解析:A、硅与氧气反应生成二氧化硅,但二氧化硅与水不反应,不能生成硅酸,错误;B、硫与氧气反应生成二氧化硫,二氧化硫与水反应生成亚硫酸,亚硫酸与氢氧化钠反应生成亚硫酸钠,正确;C、铜与氧气反应生成氧化铜,氧化铜不与水反应,错误;D、铁与氧气反应生成四氧化三铁,四氧化三铁与水不反应,错误,答案选B。
本题难度:一般
3、实验题 (12分)为验证木炭可被浓硫酸氧化成二氧化碳,选用下图中的仪器(含所盛物质)组装成套实验装置,回答下列问题。(KMnO4能吸收SO2)
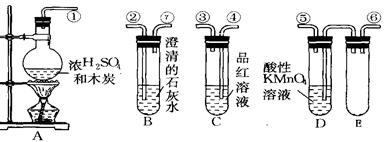
(1)在实验进行中,按气流方向从左到右的顺序,导管口的三处连接应该
是?接?,?接?,?接?。
(2)试管B,C中各有什么现象,才能表示已检验出二氧化碳?
B中?,C中?。
(3)试管D中能否用饱和NaHCO3溶液代替酸性KMnO4溶液??
说明理由:?
(4)试管E的作用是?
(5)写出A中反应的化学方程式:?
参考答案:(1)①接⑥,⑤接④,③接②;(2分)
(2)品红不褪色(2分)?澄石灰水变浑浊(2分)
(3)不能,(1分)若用NaHCO3饱和溶液, NaHCO3会发生反应:2NaHCO3+SO2==Na2SO3+H2O+CO2↑,生成CO2,因此无法确认木炭是否被氧化生成CO2(2分)?(4)防倒吸(或为安全瓶装置)(1分)
(5)C+2H2SO4(浓) CO2↑+2SO2↑+2H2O(2分)
CO2↑+2SO2↑+2H2O(2分)
本题解析:(1)由于SO2也能使澄清的石灰水变混浊,所以首先除去SO2,所以连接顺序是①接⑥,⑤接④,③接②。
(2)C是检验SO2是否被完全除尽的,因此当C中品红不褪色,而B中澄石灰水变浑浊,才能说明反应中产生了CO2。
(3)由于SO2能和碳酸氢钠反应产生CO2,方程式为2NaHCO3+SO2==Na2SO3+H2O+CO2↑,因此无法确认木炭是否被氧化。所以不能用碳酸氢钠来代替顺序高锰酸钾溶液。
(4)CO2在石灰水反应时,溶液有可能倒流,所以E的作用是防倒吸(或为安全瓶装置)。
(5)方程式为C+2H2SO4(浓) CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
本题难度:一般
4、选择题 实验室中洗涤附着在试管内壁上的硫应选择的试剂是
[? ]
A.二硫化碳
B.水
C.盐酸
D.酒精
参考答案:A
本题解析:
本题难度:简单
5、计算题 一定量的锌与一定浓度的H2SO4反应,生成的气体在标准状况下体积为2.24 L,求反应消耗的锌和H2SO4的物质的量。
参考答案:若气体全为H2,耗Zn 0.1 mol,耗H2SO4 0.1 mol
若气体全为SO2,耗Zn 0.1 mol,耗H2SO4 0.2 mol
若气体为SO2和H2,耗Zn 0.1 mol,耗H2SO4(0.1+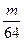 ) mol
) mol
本题解析:与Zn反应的硫酸的浓度未确定,因此需讨论,若为稀H2SO4,则2.24 L为H2;若为浓H2SO4,又有两种可能:一是浓H2SO4量大,则2.24 L全为SO2;若浓H2SO4量少,反应过程中浓度减小,则2.24 L为H2、SO2的混合气体。
若气体全为H2,则有:
Zn? +? H2SO4(稀)====ZnSO4+H2↑
1? 1? 1
0.1 mol? 0.1 mol? ="0.1" mol
="0.1" mol
若气体全为SO2,则有:
Zn? +? 2H2SO4(浓) ZnSO4+SO2↑+2H2O
ZnSO4+SO2↑+2H2O
1? 2? 1
0.1 mol? 0.2 mol? ="0.1" mol
="0.1" mol
若气体为SO2、H2的混合气体,
则n(混)= ="0.1" mol
="0.1" mol
设SO2的质量为m g,n(SO2)=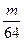 mol,n(H2)=(0.1-
mol,n(H2)=(0.1-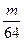 )mol。
)mol。
Zn? +? 2H2SO4(浓) ZnSO4+SO2↑+2H2O
ZnSO4+SO2↑+2H2O
1? 2? 1
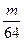 mol?
mol?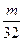 mol?
mol?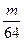 mol
mol
Zn? +? H2SO4(稀)====ZnSO4+H2↑
1? 1? 1
(0.1-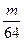 ) mol? (0.1-
) mol? (0.1-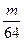 ) mol? (0.1-
) mol? (0.1-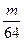 ) mol
) mol
所以n(Zn)=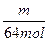 +(0.1-
+(0.1-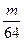 ) mol="0.1" mol
) mol="0.1" mol
n(H2SO4)= 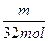 +(0.1-
+(0.1-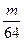 ) mol=(0.1+
) mol=(0.1+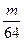 )mol
)mol
本题难度:简单