微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关AgCl沉淀的溶解平衡的说法正确的是
A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.升高温度,AgCl沉淀的溶解度减小
D.向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解程度不变
参考答案:A
本题解析:A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等 ,正确,是动态平衡;
B.AgCl难溶于水,溶液中没有Ag+和Cl-?错误,难容并不是不溶。
C.升高温度,AgCl沉淀的溶解度减小;升高温度,平衡会向吸热方向移动;溶解过程是吸热过程,所以,溶解度会增大;
D.向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解程度不变;会减小,是同离子效应;故选A。
点评:在一定温度下难溶电解质晶体与溶解在溶液中的离子之间存在溶解和结晶的平衡,称作多项离子平衡,也称为沉淀溶解平衡。
以AgCl为例,尽管AgCl在水中溶解度很小,但并不是完全不溶解。
从固体溶解平衡角度认识:AgCl在溶液中存在下属两个过程:
①在水分子作用下,少量Ag+和Cl-脱离AgCl表面溶入水中;
②溶液中的Ag+和Cl-受AgCl表面正负离子的吸引,回到AgCl表面,析出沉淀。
在一定温度下,当沉淀溶解和沉淀生成的速率相等时,得到AgCl的饱和溶液,即建立下列动态平衡:
AgCl(s) Ag+(aq)+ Cl-(aq)
Ag+(aq)+ Cl-(aq)
溶解平衡的特点是动态平衡,即溶解速率等于结晶速率,且不等于零。
其平衡常数Ksp称为溶解平衡常数;它只是温度的函数,即一定温度下Ksp一定。
本题难度:一般
2、选择题 在重铬酸钾(K2Cr2O7)溶液中存在如下平衡: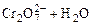

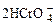

 , 向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
, 向K2Cr2O7溶液中加入AgNO3溶液,发生离子交换反应,生成砖红色沉淀且溶液的pH下降,则生成的砖红色沉淀为
A.Ag2O
B.Ag2CrO4
C.AgHCrO4
D.Ag2Cr2O7
参考答案:B
本题解析:略
本题难度:一般
3、填空题 (9分)工业废水中常含有一定量的Cr2O72―和CrO42―,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为
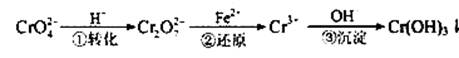
其中第①步存在平衡:2CrO42―(黄色)+2H+ Cr2O72―(橙色)+H2O
Cr2O72―(橙色)+H2O
(1)该反应体系的平衡常数表达式为:
(2)若平衡体系的pH=2,则溶液显 色.
(3)能说明第①步反应达平衡状态的是 。
a.溶液的颜色不变 b.2v (Cr2O72―) ="v" (CrO42―)
c. Cr2O72―和CrO42―的浓度相同
(4)完成第②步反应的离子方程式:
__Cr2O72―+ __Fe2+ +_____="__" Cr3+ + __Fe3+ +__ H2O
(5)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+(aq)+3OH―(aq)
Cr3+(aq)+3OH―(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)・ c3(OH―)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。
方法2:电解法
该法用Fe做电极电解含Cr2O72―的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(6)写出电解过程中的电极反应式:
阳极: 。阴极: 。
(7)溶液中同时生成的沉淀还有 。
参考答案:(共11分)(1)略(2分) (2)橙(1分) (3)a(1分)
(4)Cr2O72―+ 6Fe2+ +14H+ = 2Cr3+ + 6Fe3+ +7 H2O(2分) (5)5(2分)
(6)Fe-2e-=Fe2+(1分), 2H++2e-=H2↑(1分) (7) Fe(OH)3(1分)
本题解析:(1)平衡常数是指:可逆反应达到平衡后生成物浓度幂之积与反应物浓度幂之积的比值:即表示为: ;
;
(2)溶液显酸性,即溶液颜色显橙色;
(3)能说明第①步反应达平衡状态的是c.溶液的颜色不变
(4)根据氧化还原反应过程中元素化合价升高的总价数=化合价降低的总价数配平可得,反应的离子方程式为:Cr2O72―+ 6Fe2+ +14H+ = 2Cr3+ + 6Fe3+ +7 H2O;
(5)要使c(Cr3+)降至10-5mol/L,c(OH-)3 =" Ksp" / c(Cr3+) = 10-32÷ 10-5 = 10-27mol/L,c(OH-) = 10-9mol/L,pOH = 9,pH = 5。
(6)用Fe做电极的原因为:阳极:Fe - 2e- = Fe2+,在阳极附近溶液中会发生:6Fe2+ + Cr2O72- + 14H+ = 6Fe3+ + 2Cr3+ + 7H2O;
在阴极附近溶液pH升高的原因是:2H+ + 2e- = H2↑ ;
(7)阴极附近溶液c(H+)减小,pH升高,产生Cr(OH)3沉淀。溶液中同时产生沉淀还有Fe(OH)3
本题难度:困难
4、填空题 工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下:
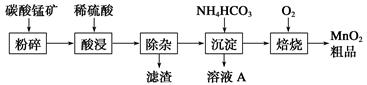
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
氢氧化物
| Al(OH)3
| Fe(OH)3
| Fe(OH)2
| Cu(OH)2
| Pb(OH)2
| Mn(OH)2
|
开始沉淀的pH
| 3.3
| 1.5
| 6.5
| 4.2
| 8.0
| 8.3
|
沉淀完全的pH
| 5.2
| 3.7
| 9.7
| 6.7
| 8.8
| 9.8
|
?
请回答下列问题:
(1)酸浸前将碳酸锰矿粉碎的作用是__________________。
(2)酸浸后的溶液中含有Mn2+、SO42―,另含有少量Fe2+、Fe3+、Al3+、Cu2+、Pb2+等,其除杂过程如下:
①加入MnO2将Fe2+氧化,其离子反应方程式为__________________________。
②加入CaO将溶液的pH调到5.2~6.0,其主要目的是
_____________________________________________________________。
③加入BaS,除去Cu2+、Pb2+后,再加入NaF溶液,除去______________________。
(3)从溶液A中回收的主要物质是________________,该物质常用作化肥。
(4)MnO2粗品中含有少量Mn3O4,可以用稀硫酸处理,将其转化为MnSO4和MnO2,然后再用氧化剂将Mn2+转化为MnO2,制得优质MnO2。写出Mn3O4与稀硫酸反应的化学方程式:______________________________。
参考答案:(1)增大接触面积,加快反应速率(使反应更充分)
(2)①2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O
②除去Fe3+、Al3+ ③Ca2+
(3)(NH4)2SO4
(4)Mn3O4+2H2SO4=2MnSO4+MnO2+2H2O
本题解析:(1)将碳酸锰矿粉碎,可以增大与H2SO4的接触面积,加快化学反应速率。(2)根据沉淀时的pH值,应把Fe2+氧化;加入CaO和H+反应,增大pH到5.2~6.0可使Al3+、Fe3+完全转化为Al(OH)3、Fe(OH)3沉淀,除去Fe3+、Al3+;调节pH值时,加入了CaO,为了除去Ca2+,应加入NaF,使之生成CaF2沉淀。
(3)溶液A中的阴离子为SO42―,所以加NH4HCO3后,生成的主要物质是(NH4)2SO4,作为氮肥用。
(4)Mn3O4+2H2SO4=2MnSO4+MnO2+2H2O (用倒配法配平,Mn3O4中Mn的化合价为+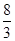 )。
)。
本题难度:困难
5、选择题 有关AgCl的沉淀溶解平衡的说法正确的是
A.AgCl沉淀生成和溶解同时在不断进行,且速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.用等体积的蒸馏水和0.01mol・L-1的盐酸洗涤AgCl沉淀,用水洗涤造成的AgCl的损失小于用稀盐酸洗涤的损失量。
D.向含有AgCl的悬浊液中加入NaBr固体,AgCl沉淀不变化
参考答案:A
本题解析:溶解平衡像化学平衡一样,是一个动态平衡,A正确;由于沉淀溶解平衡的存在,溶解中肯定存在Ag+和Cl-,B不正确;用水洗涤AgCl,AgCl(s) Ag+(aq)+Cl-(aq)平衡右移,AgCl的质量减少,用HCl洗涤AgCl,稀释的同时HCl电离产生的Cl-会使平衡左移,AgCl减少的质量要小些,C错。向含有AgCl的悬浊液中加入NaBr固体,AgCl沉淀会转变为AgBr沉淀,D错。答案选A。
Ag+(aq)+Cl-(aq)平衡右移,AgCl的质量减少,用HCl洗涤AgCl,稀释的同时HCl电离产生的Cl-会使平衡左移,AgCl减少的质量要小些,C错。向含有AgCl的悬浊液中加入NaBr固体,AgCl沉淀会转变为AgBr沉淀,D错。答案选A。
本题难度:一般