��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
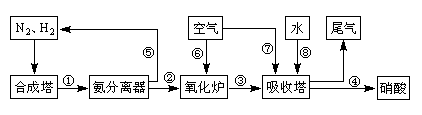
1������� ��16�֣���ҵ�ϳɰ����Ʊ�����һ��������������������£�
��1����ҵ����ʱ����ȡ������һ����ӦΪ��CO(g)+H2O(g) CO2(g)+H2(g)��t��ʱ����10L�ܱ������г���2mol CO��3molˮ��������Ӧ����ƽ�����ϵ��c(H2)=0.12mol��L-1������¶��´˷�Ӧ��ƽ�ⳣ��K= �������������
CO2(g)+H2(g)��t��ʱ����10L�ܱ������г���2mol CO��3molˮ��������Ӧ����ƽ�����ϵ��c(H2)=0.12mol��L-1������¶��´˷�Ӧ��ƽ�ⳣ��K= �������������
��2���ϳ����з�����ӦN2(g)+3H2(g) 2NH3(g) ��H<0���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������T1 300�棨�>������<����=������
2NH3(g) ��H<0���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������T1 300�棨�>������<����=������
T/��
| T1
| 300
| T2
|
K
| 1.00��107
| 2.45��105
| 1.88��103
|
��3�������ڴ�����ȼ������һ�ֵ��ʺ�ˮ����ѧ�����ô�ԭ������Ƴɡ�����-������ȼ�ϵ�أ���ͨ�백���ĵ缫�� ����������������������������£��õ缫������Ӧ�ĵ缫��ӦʽΪ ��
��4���ð������������������ᣬ��β���е�NOx����Ⱦ������Ŀǰ��ѧ��̽������ȼ�������еļ���Ƚ����������ﻹԭΪ������ˮ����Ӧ����Ϊ��
CH4(g)+4NO2(g)��4NO(g)+CO2(g)+2H2O(g) ��H= ��574kJ��mol��1
CH4(g)+4NO(g)��2N2(g)+CO2(g)+2H2O(g) ��H= ��1160kJ��mol��1
�����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ ��
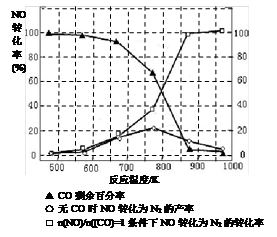
��5��ij�о�С����ʵ�����ԡ�Ag-ZSM-5��Ϊ��������ý�NOת��ΪN2��ת�������¶ȱ仯�����ͼ����ͼ����������ʹ��CO���¶ȳ���775K������NO��ת���ʽ��ͣ�����ܵ�ԭ��Ϊ ����n(NO)/n(CO)=1�������£�Ӧ���Ƶ�����¶��� ���ҡ�
�ο��𰸣���1����2�֣�1 ��2����2�֣���
��3����4�֣����� ��2�֣� 2NH3 �� 6e- + 6OH- =N2 +6H2O ��2�֡���ѧʽ1�֡���ƽ1�֣�
��4����3�֣�CH4(g)+2NO2(g)��CO2(g)��2H2O(g)+N2(g) ��H����867kJ/mol ������ʽ2�֣�
��H��ֵ1�֣�
��5����5�֣��÷�Ӧ�Ƿ��ȷ�Ӧ��1�֣�������775K��Ӧ�ﵽƽ�����������¶ȣ�1�֣���ƽ�����棨�����ƶ���NOת���ʽ��ͣ�1�֣� 870K��2�֡�д860-875K֮��������ֵ�����֣�
�����������1�����ݡ�����ʽ�����м��㣺CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
��ʼŨ�ȣ�mol?L?1�� 0.2 0.3 0 0
ת��Ũ�ȣ�mol?L?1�� 0.12 0.12 0.12 0.12
ƽ��Ũ�ȣ�mol?L?1�� 0.08 0.18 0.12 0.12
ƽ�ⳣ��K=0.12��0.12�£�0.08��0.18��=1��
��2����Ϊ�÷�Ӧ��H<0��Ϊ���ȷ�Ӧ�������¶����ߣ�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С��T1��ƽ�ⳣ������300��ʱƽ�ⳣ��������T1 < 300�档
��3��ȼ�ϵ���У�O2Ϊ������ȼ��Ϊ����������ͨ�백���ĵ缫�Ǹ�����NH3ʧȥ�������ɵĵ���ΪN2�����Ե缫����ʽΪ��2NH3 �� 6e- + 6OH- =N2 +6H2O
��4��NO2����ԭΪN2����CH4������ΪCO2��д����ѧ����ʽ����ƽ��CH4(g)+2NO2(g)��CO2(g)��2H2O(g)+N2(g)�����ݸ�˹��������ʱ䣬��H=1/2��H1+1/2��H2=��867kJ?mol?1���ɵ��Ȼ�ѧ����ʽ��
��5��0~775K��Ϊ��Ӧ������ѧƽ��Ĺ��̣�775Kʱ�ﵽƽ�⣬�¶ȼ������ߣ�NO��ת���ʼ�С��˵������ӦΪ���ȷ�Ӧ���¶����ߣ�ƽ�����淴Ӧ�����ƶ���
���㣺���⿼��ƽ�ⳣ�����жϼ����㡢ȼ�ϵ��ԭ�����Ȼ�ѧ����ʽ����д����ѧƽ���ƶ���
�����Ѷȣ�����
2������� ��ѧ��Ҫ�о���̼Ԫ�ؼ��仯������صĺܶ���⣮
��1����̿��������ȡˮú�������12g̼��ˮ������ȫ��Ӧ����ˮú��ʱ��������131.6kJ�������÷�Ӧ���Ȼ�ѧ����ʽ��______��
��2����ҵ�Ͽ��ý�̿ұ����������0.5mol̼��ȫ�������Ӧ���õ�0.6mol����ͬʱ����2�ֳ������壬��÷�Ӧ�Ļ�ѧ����ʽ��______��
��3��̼��ˮ������ˮú���ķ�Ӧ��һ�����淴Ӧ��������������жϸ÷�Ӧһ���ﵽƽ��״̬����______��ѡ���ţ���
a��v����H2O��=v����H2�� b���������¶Ȳ��ٷ����ı�
c������n mol H2ͬʱ����n mol CO d������������������ʵ�������ʱ��ı�
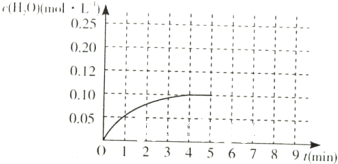
��4���¶�T1ʱ����һ���Ϊ2L���ܱ��ݻ��У�����2.0mol CO��2.0mol��H2����Ӧ��c��H2O���ı仯�����ͼ��ʾ��T1ʱ��Ӧ[C��s��+H2O��g��?CO��g��+H2��g��]��ƽ�ⳣ������ֵΪ______���ڵ�5����ʱ����ϵ���·����ߵ�T2�����ڵ�8����ʱ�ﵽ�µ�ƽ�⣬������ͼ�л�����5���ӵ�9���Ӻ�c��H2O��Ũ�ȱ仯���Ƶ����ߣ�ֻҪ���Ա�ʾ����
�ο��𰸣���1��12g̼�����ʵ���Ϊ1mol����ˮ������ȫ��Ӧ����CO��H2������131.6kJ�������÷�Ӧ���Ȼ�ѧ����ʽC��s��+H2O��g��=CO��g��+H2��g����H=+131.6kJ?mol-1��
�ʴ�Ϊ��C��s��+H2O��g��=CO��g��+H2��g����H=+131.6kJ?mol-1��
��2��0.5mol̼��ȫ�������Ӧ���õ�0.6mol����ͬʱ����2�ֳ������壬����ΪCO2��CO��������CO2��CO�����ʵ����ֱ�Ϊxmol��ymol������Cԭ���غ���x+y=0.5�����ݵ���ת���غ���4x+2y=0.6��3���������x=0.4��y=0.1��CO2��CO��ϵ��Ϊ4��1���ʸ÷�Ӧ�ķ���ʽΪ5C+3Fe2O3����.4CO2��+CO��+6Fe��
�ʴ�Ϊ��5C+3Fe2O3����.4CO2��+CO��+6Fe��
��3��C��s��+H2O��g��=CO��g��+H2��g����H=+131.6kJ?mol-1��
a��v����H2O��=v����H2�������ݷ�Ӧ��֪��ʼ����v����H2O��=v����H2��������˵����Ӧ����ƽ�⣬��a����
b����Ӧ�����ȷ�Ӧ���������¶Ȳ��䣬˵����Ӧ�ﵽƽ�⣬��b��ȷ��
c�����ݷ�Ӧ��֪������n mol H2ͬʱ����n mol CO����Ӧ������в���˵����Ӧ����ƽ�⣬��C����
d����Ӧǰ����������ʵ��������仯���淴Ӧ������������ʵ������ӣ�����������������ʵ�������ʱ��ı䣬˵����Ӧ����ƽ�⣬��d��ȷ��
��ѡ��bd��
��4���¶�T1ʱ����һ���Ϊ2L���ܱ��ݻ��У�����2.0mol CO��2.0mol��H2����Ӧ��c��H2O���ı仯�����ͼ��ʾ��
C��s��+H2O��g��?CO��g��+H2��g��
��ʼ����mol/L�� 0 0 1 1
�仯����mol/L�� 0.1 0.1 0.1
ƽ������mol/L�� 0.1 0.9 0.9
T1ʱ��ӦC��s��+H2O��g��?CO��g��+H2��g����ƽ�ⳣ��=0.9��0.90.1=8.1��
�ڵ�5����ʱ����ϵ���·����ߵ�T2�����ڵ�8����ʱ�ﵽ�µ�ƽ�⣬�ڷ�Ӧ�����ȷ�Ӧ����ƽ��������У�ˮ��Ũ�ȼ�С����ͼ�л�����5���ӵ�9���Ӻ�c��H2O��Ũ�ȱ仯���Ƶ�����Ϊ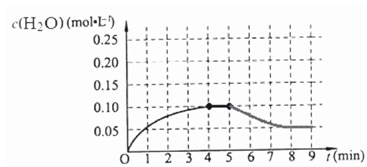 ��
��
�ʴ�Ϊ��8.1�� ��
��
���������
�����Ѷȣ�һ��
3��ѡ���� ��֪��298Kʱ���й����ݣ�C(s)��1/2O2(g)===CO(g)����H1����110.5kJ��mol��1��
C(s)��O2(g)===CO2(g)����H2����393.5kJ��mol��1����C(s)��CO2(g)===2CO(g)�Ħ�HΪ(����)
A��+283.5kJ��mol��1
B��+172.5kJ��mol��1
C����172.5kJ��mol��1
D����504kJ��mol��1