微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在相同的温度下,100 mL 0.01 mol・L-1醋酸溶液与10 mL 0.1 mol・L-1醋酸溶液相比较,下列数值中前者大于后者的是
A.中和时所需氢氧化钠的物质的量
B.H+的物质的量浓度
C.电离平衡常数K
D.H+的物质的量
参考答案:D
本题解析:A、100 mL 0.01 mol・L-1醋酸溶液与10 mL 0.1 mol・L-1醋酸溶液中醋酸的物质的量相等,因此中和时所需氢氧化钠的物质的量相等,A不正确;B、醋酸的浓度越大,溶液的酸性越强,氢离子的浓度就越大。所以H+的物质的量浓度是前者小于后者,B不正确;C、电离平衡常数K只与温度有关系,所以两种醋酸溶液中电离平衡常数K相等,C不正确;D、醋酸是弱酸,存在电离平衡。稀释促进电离,所以将10 mL 0.1 mol・L-1醋酸溶液稀释到100 mL 0.01 mol・L-1醋酸溶液,溶液中氢离子的物质的量增加,D正确,答案选D。
本题难度:一般
2、选择题 物质的量浓度相同的氨水.氢氧化钠和氢氧化钡溶液,分别用蒸馏水稀释到原来的X倍、Y倍、Z倍,稀释后三种溶液的pH同,则X、Y、Z的关系是
[? ]
A.X=Y=Z
B.X>Y=Z
C.X<Y<Z
D.X=Y<Z
参考答案:C
本题解析:
本题难度:简单
3、选择题 相同条件下,向100mL,pH=1的硫酸、醋酸、盐酸溶液中分别加入0.46gNa,产生氢气的体积分别为V1、V2、V3,则下列关系中,正确的 91Exam.org是( )
A.V3<V2<V1
B.V3=V2=V1
C.V1=V3>V2
D.V1=V3<V2
参考答案:B
本题解析:
本题难度:一般
4、选择题 常温下,取pH=2的两种二元酸H2A与H2B各1 mL,分别加水稀释,测得pH变化与加水稀释倍数有如图所示变化,则下列有关叙述不正确的是
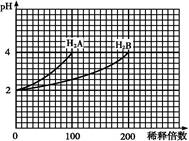
A.H2A为二元强酸
B.pH=4的NaHA水溶液中离子浓度大小为:c(Na+)>c(HA-)>c(A2-)>c(H2A)>c(OH-)
C.含NaHA、NaHB的混合溶液中,离子浓度大小为:c(Na+)=c(A2-)+c(HB-)+c(B2-)+c(H2B)
D.Na2B的水溶液中,离子浓度大小为:c(Na+)>c(B2-)>c(OH-)>c(H+)
参考答案:B
本题解析:A、从图分析,H2A稀释100倍,pH改变了2,说明是强酸,正确,不选A;B、H2A为二元强酸,所以NaHA水溶液中没有HA-和H2A,所以选B;C、H2B稀释100倍,pH变化小,说明是弱酸,所以HB-能电离也能水解,在含NaHA、NaHB的混合溶液中存在物料守恒,c(Na+)=c(A2-)+c(HB-)+c(B2-)+c(H2B),正确,不选C;D、Na2B的水溶液中B2-水解使溶液显碱性,所以正确,不选D。
 考点:盐类的水解,溶液的离子浓度的比较,强弱电解质的判断
考点:盐类的水解,溶液的离子浓度的比较,强弱电解质的判断
本题难度:困难
5、选择题 25℃ 时,水的离子积为Kw,该温度下将 a mol ・L-1一元酸 HA 与b mol・L-1一元强碱BOH 等体积混合,若恰好完全反应,下列结论中不正确的是
A. 混合液中:c(H+ ) ≤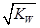 ?B. 混合液中:c(HA)+c(A-)=a mol・L-1?
?B. 混合液中:c(HA)+c(A-)=a mol・L-1?
C.? a = b?D. 混合液中:c(H+)+c(B+)= c(OH-)+c(A-)
参考答案:B
本题解析: HA 与BOH 等体积混合,恰好完全反应:HA+BOH==BA+H2O,酸和碱的物质的量相同,故C正确;根据电荷守恒,D正确;若HA为强酸,反应后的盐溶液为中性,c(H+)=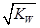 ;若HA为若酸,反应后的盐溶液为碱性,c(H+)<
;若HA为若酸,反应后的盐溶液为碱性,c(H+)<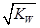 ,A正确;若HA为强酸,反应后的盐溶液为中性,c(A-)=1/2a mol・L-1;若HA为若酸,反应后的盐溶液为碱性,c(HA)+c(A-)=1/2a mol・L-1,B不正确;
,A正确;若HA为强酸,反应后的盐溶液为中性,c(A-)=1/2a mol・L-1;若HA为若酸,反应后的盐溶液为碱性,c(HA)+c(A-)=1/2a mol・L-1,B不正确;
本题难度:一般