微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列变化需要加入适当的氧化剂才能完成的是
A.CuO→Cu
B.Fe→FeCl3
C.H2SO4→H2
D.HNO3→N2
参考答案:B
本题解析:氧化剂在反应中得到电子,元素的化合价降低,因此如果变化需要加入适当的氧化剂才能完成,这说明选项中物质是还原剂,有关元素的化合价升高。A、转化CuO→Cu中铜元素的化合价降低,需要加入还原剂,A不正确;B、转化Fe→FeCl3中铁元素的化合价升高,需要加入氧化剂,B正确;C、转化H2SO4→H2中氢元素的化合价降低,需要加入还原剂,C不正确;D.转化HNO3→N2中氮元素的化合价降低,需要加入还原剂,D不正确,答案选B。
本题难度:一般
2、选择题 判断下列有关化学基本概念的依据正确的是
A.胶体:分散质的微粒直径是否在1 nm~100 nm之间
B.化学变化:是否有热效应、颜色变化、气体或沉淀生成等四种实验现象
C.离子反应:反应物是否全部以离子的形式存在
D.氧化还原反应:反应前后元素的化合价是否变化
参考答案:AD
本题解析:略
本题难度:简单
3、选择题 在5ml0.05mol/L的某金属氯化物的溶液中,滴加
0.1mol/LAgNO3溶液,生成沉淀的质量与加入AgNO3溶液的体积关系如图所示,则该氯化物中金属元素的化合价为
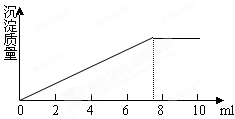
A.+1
B.+2
C.+3
D.+4
参考答案:C
本题解析:
分析:根据氯离子和银离子之间反应生成氯化银沉淀的实质以及氯化物的化学式进行计算.
解答:解:氯化物种的Cl-和Ag+1:1反应,因此消耗掉的硝酸银的物质的量为这些溶液中Cl-离子的物质的量,n(Cl-)=n(Ag+)=7.5×10-3L×0.1mol/L=7.5×10-4mol.
设该金属的化合价为X其化学式为A(Cl)x,n(Ax+)=5×10-3L×0.05mol/L=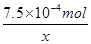 ,解得x=3.
,解得x=3.
故选C.
点评:本题考查学生分析和解决问题的能力,是一道有关离子反应的计算题,难度不大.
本题难度:简单
4、填空题 实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4二主要流程如下:
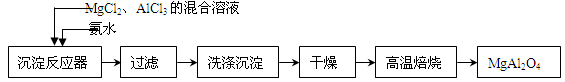
⑴制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式 。
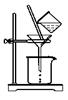
⑵如图所示,过滤操作中的一处错误是 。判断流程中沉淀是否洗净所用的试剂是 。高温焙烧时,用于盛放固体的仪器名称是 。
⑶在25℃下,向浓度均为0.01 mol?L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成_______沉淀(填化学式),生成该沉淀的离子方程式_______ ______________
(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10 -34。)
⑷无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
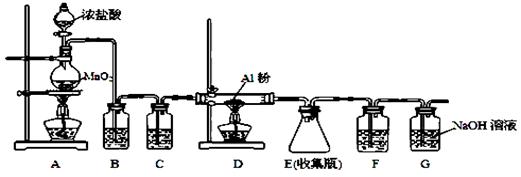
装置B中盛放饱和NaCl溶液,该装置的主要作用是 ; F中试剂的作用是 ;用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为 。
⑸将Mg、Cu组成的3.92g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体1.792L(标准状况),向反应后的溶液中加入4mol/L的NaOH溶液80mL时金属离子恰好完全沉淀。则形成沉淀的质量为 g。
参考答案:(1) 2 Al(OH)3+Mg (OH)2 MgAl2O4 + 4H2O
MgAl2O4 + 4H2O
(2)漏斗下端尖嘴未紧贴烧杯内壁 AgNO3溶液(或硝酸酸化的AgNO3溶液);坩埚
(3)Al(OH)3 Al3++ 3NH3・H2O=Al(OH)3↓+ 3NH4+
(4)除去HCl;吸收水蒸气;碱石灰(或NaOH与CaO混合物)
(5)8.00
本题解析:
试题分析:(1)向MgCl2、AlCl3的混合溶液中加入过量的氨水,发生反应:MgCl2+ 2NH3・H2O=Mg(OH)2↓+ 2NH4Cl;AlCl3+ 3NH3・H2O=Al(OH)3↓+ 3NH4Cl;然后把Al(OH)3、Mg (OH)2沉淀过滤出来,并洗涤干净、干燥,最后高温灼烧发生反应2Al(OH)3+Mg (OH)2 MgAl2O4 + 4H2O。即得到要制备MgAl2O4。⑵在如图所示的过滤操作中的错误是漏斗下端尖嘴未紧贴烧杯内壁。由于沉淀是从金属氯化物中过滤出来的,所以要判断流程中沉淀是否洗净的方法就是用硝酸酸化的AgNO3溶液来检验是否含有Cl-即可。高温焙烧时,要用坩埚来盛放固体物质。⑶Mg2+形成沉淀需要的
MgAl2O4 + 4H2O。即得到要制备MgAl2O4。⑵在如图所示的过滤操作中的错误是漏斗下端尖嘴未紧贴烧杯内壁。由于沉淀是从金属氯化物中过滤出来的,所以要判断流程中沉淀是否洗净的方法就是用硝酸酸化的AgNO3溶液来检验是否含有Cl-即可。高温焙烧时,要用坩埚来盛放固体物质。⑶Mg2+形成沉淀需要的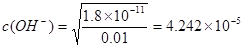 ;而Al3+形成沉淀需要的
;而Al3+形成沉淀需要的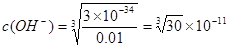 <4.242×10-5。需要的OH-的浓度越小,越容易形成沉淀。因此首先形成的是Al(OH)3沉淀。(4)装置B中盛放饱和NaCl溶液,该装置的主要作用是除去氯气中杂质气体HCl,同时减小氯气的溶解。由于无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,所以在F中试剂的作用是吸收水蒸气,防止无水AlCl3水解。用干燥管装填碱石灰也可起到F和G的作用。⑸Mg、Cu与硝酸发生反应变为Mg2+、Al3+时失去的电子的物质的量与HNO3得到电子的物质的量相等。而当向反应后的溶液中加入NaOH溶液金属离子恰好完全沉淀时增加的质量就是OH-的质量,其物质的量就等于Mg2+、Al3+时失去的电子的物质的量。根据等量关系可得。n(NO)= 1.792L÷22.4L/mol=0.08mol.所以n(e-)="0.08mol×3=0.24mol." 故形成沉淀的质量为3.92g+0.24mol×17g/mol=8.00g。考点:考查物质的制备、混合物的分离、仪器的选择与使用、气体的制取、杂质的除去、沉淀形成的先后顺序、守恒法在化学计算中的应用的知识。
<4.242×10-5。需要的OH-的浓度越小,越容易形成沉淀。因此首先形成的是Al(OH)3沉淀。(4)装置B中盛放饱和NaCl溶液,该装置的主要作用是除去氯气中杂质气体HCl,同时减小氯气的溶解。由于无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,所以在F中试剂的作用是吸收水蒸气,防止无水AlCl3水解。用干燥管装填碱石灰也可起到F和G的作用。⑸Mg、Cu与硝酸发生反应变为Mg2+、Al3+时失去的电子的物质的量与HNO3得到电子的物质的量相等。而当向反应后的溶液中加入NaOH溶液金属离子恰好完全沉淀时增加的质量就是OH-的质量,其物质的量就等于Mg2+、Al3+时失去的电子的物质的量。根据等量关系可得。n(NO)= 1.792L÷22.4L/mol=0.08mol.所以n(e-)="0.08mol×3=0.24mol." 故形成沉淀的质量为3.92g+0.24mol×17g/mol=8.00g。考点:考查物质的制备、混合物的分离、仪器的选择与使用、气体的制取、杂质的除去、沉淀形成的先后顺序、守恒法在化学计算中的应用的知识。
本题难度:困难
5、选择题 在过量的稀硫酸溶液中加入5.6g铁粉,待反应完全后,再加入50 mL 0.5mol・L-1 KNO3溶液,恰好反应完全。该反应的方程式为:__FeSO4+__KNO3+__H2SO4===__K2SO4+__Fe2(SO4)3+__NxOy+__H2O,则对该反应的下列说法正确的是( )。
A.反应中还原产物是NO
B.化学方程式中按物质顺序的计量数是:8、2、5、1、4、1、5
C.反应过程中转移的电子数为8e-
D.氧化产物和还原产物的物质的量之比为1∶4