| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《影响化学反应速率的因素》在线测试(2017年最新版)(四)
参考答案:A 本题解析:增大压强、升高温度、增大接触面积、增大反应物的量均可使反应速率加快,由于碳为固体,增大碳粉的用量对反应速率没有影响。 本题难度:一般 2、实验题 (14分)某课外兴趣小组对双氧水(H2O2水溶液)做了如下实验探究。
②实验结果说明催化剂作用的大小与 有关。 (2)取三份含有等量H2O2,但质量分数不同的双氧水,分别向其中加入1克MnO2粉末。测定结果如下:
①反应完成所需的时间不同的原因 。 ②反应后液体温度不同的原因 。 ③收集到气体体积不同的原因 。 (3)向含有酚酞的NaOH稀溶液中,逐滴滴入10%的双氧水,红色褪去。 ①已知双氧水显弱酸性,试写出H2O2的电离方程式: 。 ②小组讨论红色褪去的原因时,甲同学认为是双氧水显酸性所致;乙同学认为是双氧水有较强氧化性所致。请你设计一个简单实验来说明是甲对还是乙对。(简要文字说明) 参考答案:(每空2分,共14分) 本题解析:(1)①双氧水在催化剂的作用下,分解生成氧气,反应的方程式是2H2O2 本题难度:困难 3、选择题 下列说法中正确的是( ) |
参考答案:C
本题解析:催化剂能改变反应速率,但不能引发反应,故A项错;催化剂在反应前后质量和化学性质都不变,故B项错;C项对;D项中加入NaOH增加了水的导电能力,NaOH不是催化剂,故D项错。
考点:影响化学反应速率的因素
本题难度:一般
4、计算题 已知:将KI、盐酸、试剂X和淀粉四种溶液混合,无反应发生。若再加入双氧水,将发生反应:H2O2+2H++2I―→2H2O+I2,且生成的I2立即与试剂X反应而被消耗。一段时间后,试剂X将被反应生成的I2完全消耗。由于溶液中的I―继续被H2O2氧化,生成的I2与淀粉作用,溶液立即变蓝。因此,根据试剂X的量、滴入双氧水至溶液变蓝所需的时间,即可推算反应H2O2+2H++2I―→2H2O+I2的反应速率。
下表为某同学依据上述原理设计的实验及实验记录(各实验均在室温条件下进行):
| 编号 | 往烧杯中加入的试剂及其用量(mL) | 催化剂 | 开始变蓝时间(min) | ||||
| 0.1 mol・Lˉ1 KI溶液 | H2O | 0.01 mol・Lˉ1 X溶液 | 0.1 mol・Lˉ1 双氧水 | 1?mol・Lˉ1 稀盐酸 | |||
| 1 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 无 | 1.4 |
| 2 | 20.0 | m | 10.0 | 10.0 | n | 无 | 2.8 |
| 3 | 10.0 | 20.0 | 10.0 | 20.0 | 20.0 | 无 | 2.8 |
| 4 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 5滴Fe2(SO4)3 | 0.6 |
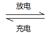 2AlI3(s)。含I―传导有机晶体合成物作为电解质,该电池负极的电极反应为:______________________________,充电时Al连接电源的___________极。
2AlI3(s)。含I―传导有机晶体合成物作为电解质,该电池负极的电极反应为:______________________________,充电时Al连接电源的___________极。参考答案:(16分)?
(1)20.0,20.0?(各2分,共4分)
(2)0.5mL(2分)
(3)画图(共4分,标注2分)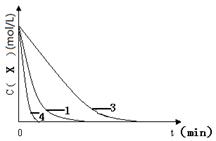
(4)降低(2分)?
(5)Al―3e― +3I― =" Al" I3?负极 (各2分,共4分)
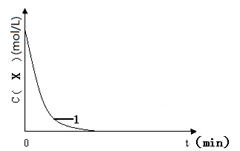
本题解析:(1)根据对比实验的目的可知,只改变双氧水浓度,其它条件相同,则盐酸的浓度不变,所以其体积保持不变,则n=20.0;由于实验1所用溶液总体积为(20.0+10.0+10.0+20.0+20.0)mL,实验2所用溶液的总体积为(20.0+m+10.0+10.0+n),由于实验1、2所用溶液的总体积相同,n=20.0,则m=20.0;(2)由于n=c?V,则n(X)= 0.01 mol・Lˉ1×10.0×10ˉ3L =10ˉ4mol;由于I2与X反应时,两者物质的量之比为1∶2,则n(I2)=0.5×10ˉ4mol,为了确保看到蓝色,n(I2)一定大于0.5×10ˉ4mol;由于n(I―)= 0.1 mol・Lˉ1×10.0×10ˉ3L =10ˉ3mol,则碘离子一定过量,过氧化氢完全反应,H2O2+2H++2I―→2H2O+I2中过氧化氢与I2的系数之比等于物质的量之比,为了确保看到蓝色,n(H2O2)一定大于0.5×10ˉ4mol;由于V=n/c,则V(H2O2)>0.5×10ˉ4mol÷0.1 mol・Lˉ1,即V(H2O2)>0.5mL;(3)画图要点:由于KI、双氧水、盐酸均过量,则X将反应完全,实验1、3、4中X的起始浓度相同,反应停止时X的浓度也都为0;实验1→实验3,仅减小碘化钾溶液的浓度,反应速率减小,X的浓度由起始浓度减小到0的时间增大,实验3和实验1的起点和终点值相同,中间过程的曲线在实验1曲线的右边,反应的时间比实验1长;实验1→实验4,其他条件相同,仅使用了催化剂,反应速率加快,X的浓度由起始浓度减小到0的时间缩短,实验4和实验1的起点和终点值相同,中间过程的曲线在实验1曲线的左边,反应的时间比实验1少;(4)硫酸铁溶液是该反应的催化剂,能加快反应速率,原因是催化剂能降低反应的活化能;(5)原电池的负极反应氧化反应,正极发生还原反应,电池总反应中铝元素由0升为+3价,发生氧化反应,说明负极的主要反应物和产物是Al、AlI3,根据电解质中定向移动离子及电子、电荷、原子守恒原理,负极反应式为Al―3e― +3I― =" Al" I3;放电时铝电极发生氧化反应,充电时该电极上发生还原反应,铝元素由+3降为0,由于电解池中阴极发生还原反应,则充电时铝电极作阴极,应该与直流电源的负极相连。
本题难度:困难
5、选择题 在一密闭容器中充入1molH2和1molI2,压强为p(Pa),并在一定温度下使其发生反应H2(g)+I2(g)=2HI(g)下列说法正确的是( )
A.保持容器容积不变,向其中加入1molH2,化学反应速率不变
B.保持容器容积不变,向其中加入1molAr,化学反应速率增大
C.保持容器内气体压强不变,向其中加入1molAr,化学反应速率不变
D.保持容器内气体压强不变,向其中加入1molH2(g)和1molI2(g),新平衡时化学反应速率不变
参考答案:A.保持容器容积不变,向其中加入1molH2,反应物浓度增大,反应速率增大,故A错误;
B.保持容器容积不变,向其中加入1molAr,参加反应的物质的浓度不变,则反应速率不变,故B错误;
C.保持容器内气体压强不变,向其中加入1molAr,体积增大,反应物的浓度减小,则反应速率减小,故C错误;
D.保持容器内气体压强不变,向其中加入1 mol H2(g)和1molI2(g),因体积增大为2倍,物质的量增大为2倍,则浓度不变,反应速率不变,故D正确.
故选D.
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《氧化钠与过.. | |