微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下面是常见的电化学装置图,①③④中均为惰性电极,下列说法正确的是
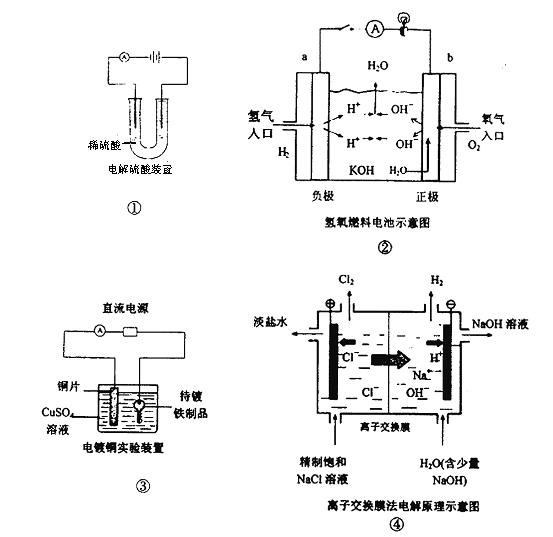
A.装置①中电解一段时间后,溶液的PH不变。
B.装置②中b极为正极,该极的电极反应方程式为O2+4H++ 4e-=2H2O
C.装置③中铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol
电子转移,此时铜片和铁制品的质量差为128g
D.装置④中阳离子交换膜上每透过1mol Na+时,则阴极上产生11.2L H2
参考答案:C
本题解析:A项,电解稀硫酸实质是电解水,电解过程中,硫酸的物质的量不变,溶液的体积减少,H+的浓度增大,溶液的PH减少;B项,该电池的电解质溶液为KOH溶液,故该极的电极反应式应为O2+2H2O+4e-=4OH-;C项,阴极反应式:Cu2++2e-="Cu" ,即2mol电子转移时铜片质量增加64克,阳极反应式:Cu-2e-= Cu2+,当2mol电子转移时,铜片质量减少64克,故铜片和铁制品的质量差为128g。D项,阳离子交换膜上每透过1mol Na+时,电子转移1mol,据阴极反应式:2H+ + 2e-+ =H2 ↑,若在标准状况下,产生11.2L H2,但题意中无此条件,故D项错。
本题难度:一般
2、选择题 某学生欲完成反应Cu+H2SO4===CuSO4+H2↑而设计了下列四个实验,你认为可行的是
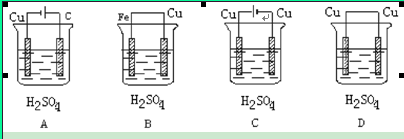
参考答案:C
本题解析:
试题解析:A、该装置为电解装置,铜作阴极,被保护,其实质是电解水,错误;B、该装置是原电池装置,铁作负极,发生氧化反应其方程式为Fe+H2SO4===FeSO4+H2↑,错误;C、为电解装置,阳极铜失电子进入溶液,阴极氢离子得电子生成氢气,正确;D、两极材料相同,不能形成原电池,错误,答案选C。
本题难度:简单
3、填空题 下表列出了3种燃煤烟气脱硫方法的原理。

(1)方法I中氨水吸收燃煤烟气中SO2的化学反应为:
2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO4+SO2+H2O=2NH4HSO3
能提高燃煤烟气中SO2去除率的措施有________(填字母)。
A.增大氨水浓度 B.升高反应温度 C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
采用方法I脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是__________(用离子方程式表示)
?(2)方法Ⅱ主要发生了下列反应:
2CO(g) +SO2(g)=S(g)+2CO2(g) △H=8.0kJ/mol
2H2(g)+SO2(g)=S(g)+2H2O(g) △H=90.4 kJ/mol
2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ/mol
2H2(g)+O2(g)=2H2O(g) △H=-483. 6 kJ/mol
S(g)与O2(g)反应生成SO2(g)的热化学方程式为____________________
(3)方法Ⅲ中用惰性电极电解NaHSO3溶液的装置如下图所示。阳极区放出气体的成分为____________ (填化学式)。
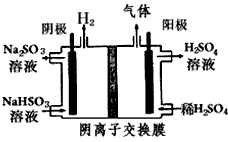
参考答案:(1)AC;HCO3-+SO2=CO2+HSO3-
(2)S(g)+O2(g)=SO2(g) △H=-574.0 kJ/mol
(3)O2、SO2
本题解析:
本题难度:一般
4、填空题 (10分)氢氧燃料电池的实验装置如图所示,回答下列有关该实验的问题。
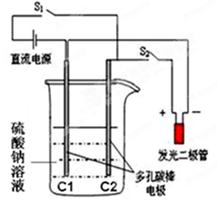
(1)要使发光二极管发亮,实验时的操作顺序是:先_______,电解一段时间后,__________;
(2)在实验的全过程中能量的主要转化形式是 ;
(3)写出下列两种操作时的电极反应式,并注明电极名称:
①按下开关S1,断开开关S2,一段时间后: C1为 极,电极反应: ;
②断开开关S1,迅速按下开关S2:(提示:此时C1附近溶液显碱性,C2附近溶液显酸性)C2为______极, 电极反应: 。
参考答案:(1)关闭S1(1分);打开S1,关闭S2(1分)
(2)电能→化学能→电能 (或电能→化学能→电能→光能) (2分)
(3)①阴极(1分) 2H++2e-=H2↑(其他合理形式也可给分)(2分)
②正极(1分) O2+ 4H+ + 4e-=2H2O(2分)
本题解析:(1)要使发光二极管发亮,则需要电源。由于要形成原电池,根据装置图可知需要燃料氢气和氧化剂氧气,所以实验时的操作顺序是先关闭S1,电解碳酸钠溶液生成氢气和氧气,电解一段时间后,打开S1,关闭S2从而构成原电池对外供电;
(2)根据(1)中的分析可知,在实验的全过程先是电解池,然后是原电池,所以能量的主要转化形式是电能→化学能→电能;
(3)①按下开关S1,断开开关S2,则构成电解池,C1与电源的负极相连为阴极,溶液中的氢离子放电,因此电极反应为2H++2e-=H2↑;
②断开开关S1,迅速按下开关S2,则此时构成原电池,C2电极上氧气得到电子为正极,电极反应O2+ 4H+ + 4e-=2H2O。
考点:考查电化学原理的应用
本题难度:一般
5、选择题 以惰性电极电解一定量的CuSO4溶液,若阳极上产生气体的物质的量为0.01mol,则阴极上析出Cu的质量可能为( )
A.1.00?g
B.1.92?g
C.2.56?g
D.5.12g
参考答案:解;以惰性电极电解CuSO4溶液,在阳极上氢氧根离子放电生成氧气物质的量为0.01mol,阴极上铜离子得到电子析出金属铜,
阳极电极反应:4OH--4e-=2H2O+O2↑;阴极电极反应:2Cu2++4e-=2Cu;
根据电子守恒,若电子转移全部在氧气和铜之间存在,得到:O2~2Cu~4e-
? ?0.01mol 0.02mol
阴极析出铜的质量=0.02mol×64g/mol=1.28g;
若阴极上铜离子得到电子后,溶液中的氢离子得到电子放氢气,则阴极上析出Cu的质量可能为1.00g;
故选A.
本题解析:
本题难度:简单