微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中不正确的是
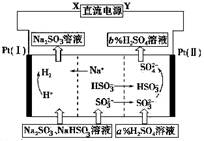
A.X为直流电源的负极,Y为直流电源的正极
B.阳极区pH增大
C.图中的b>a
D.该过程中的产品主要为H2SO4和H2
参考答案:B
本题解析:A、氢气在Pt极上生成,说明Pt为为阴极,则X为负极,Y为正极,正确;B、阳极区的SO32-、HSO3-在阳极被氧化为SO42-、H2SO4,酸性增强,pH减小,错误;C、由于阴、阳离子交换膜的存在,使加进阳极区的硫酸的浓度小于阳极再生的硫酸的浓度,即b>a,正确;D、阳极产品为硫酸,阴极产品有氢气和亚硫酸钠,正确,答案选B。
本题难度:一般
2、填空题 (9分)
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。
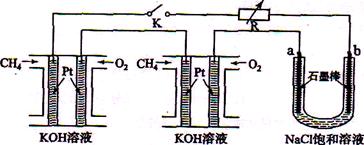
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为 、 。
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是 ,电解氯化钠溶液的总反应方程式为 ;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为
(法拉第常数F=9.65×l04C.mol-1,列式计算),最多能产生的氯气体积为 L(标准状况)。
参考答案::(1)O2+2H2O +4e―=4OH―,CH4+10OH--8e―=CO32-+ 7H2O;(2)H2;2NaCl+2H2O 2NaOH+ H2↑+ Cl2↑;(3)(1L/22.4L.mol-1)×8×9.65× 104C.mol-1 =3.45×104C;4。
2NaOH+ H2↑+ Cl2↑;(3)(1L/22.4L.mol-1)×8×9.65× 104C.mol-1 =3.45×104C;4。
本题解析::(1)燃料电池的总反应就是燃料燃烧的反应即:CH4+2O2+2OH- = CO32-+ 3H2O,故其正极反应式为:O2+ 2H2O +4e―= 4OH―,我们用总反应式减正极反应式可得负极反应式:CH4+10OH--8e―=CO32-+ 7H2O;(2分析图中三池可看出1、2两池是串联的燃料电池,通入甲烷的一极是负极,故此电解池中与其相连的b电极为阴极,生成的气体为氢气;电解的总反应式为:2NaCl+2H2O 2NaOH+ H2↑+ Cl2↑;(3)根据(1)中的负极反应式,可知通入1mol甲烷时失电子8mol,总电量为8×96500C,由于图中的两个电池是串联,故可知线路上转移的电子与一个燃料电池时相同,结合甲烷的量,其1L为1/22.4mol,可求电为:(1L/22.4L.mol-1)×8×9.65× 104C.mol-1 =3.45×104C;电解时得到氢气为4L。
2NaOH+ H2↑+ Cl2↑;(3)根据(1)中的负极反应式,可知通入1mol甲烷时失电子8mol,总电量为8×96500C,由于图中的两个电池是串联,故可知线路上转移的电子与一个燃料电池时相同,结合甲烷的量,其1L为1/22.4mol,可求电为:(1L/22.4L.mol-1)×8×9.65× 104C.mol-1 =3.45×104C;电解时得到氢气为4L。
【考点定位】此题以燃料电池的使用为载体,考查了原电池的电极反应式书写、电极的判断和电解知识。
本题难度:一般
3、选择题 如下图所示:pH=a的某电解质溶液,通直流电一段时间后,溶液的pH<a,则该电解质可能是
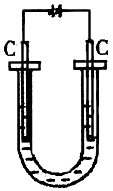
[? ]
A.NaCl
B.CuSO4
C.NaOH
D.K2SO4
参考答案:B
本题解析:
本题难度:一般
4、选择题 在水中加入等物质的量的Ag+、Ba2+、SO42-、NO3-、Cl-、Na+,用惰性材料作电极进行电解,通电片刻后停止,下列说法不正确的是(?)
A.电解的实质是:阳极:2Cl--2e-====Cl2↑;阴极:Ag+e-====Ag
B.电解的实质是:阳极:4OH--4e-====2H2O+O2↑;阴极:2H++2e-====H2↑
C.要恢复成电解前的溶液可以加水
D.电解产物中氧化产物和还原产物的物质的量之比为1∶2
参考答案:A
本题解析:由原溶液中Ag+与Cl-、Ba2+与SO42-均全部沉淀,故溶液其实是NaNO3溶液,根据放电顺序可知:阳极:4OH--4e-==2H2O+O2↑;阴极:2H++2e-==H2↑,氧化产物氧气和还原产物氢气的物质的量之比为1∶2;相当于电解水,恢复成电解前的溶液可以加水即可;
故答案为A
本题难度:一般
5、选择题 下列叙述正确的是
A.在电解池的阴极和原电池的负极上都发生氧化反应
B.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
C.用惰性电极电解KOH溶液,阴、阳两极产物的物质的量之比为1:2
D.用惰性电极电解饱和NaCl溶液,若有lmol电子转移,则生成l molNaOH
参考答案:D
本题解析:A、电解池阴极发生还原反应,A错误;B、Fe比Sn活泼,故镀层破损后镀锡铁腐蚀更快,而Zn比铁活泼,镀锌铁镀层破损后首先是Zn被腐蚀,起到保护铁的作用,B错误;C、电解KOH溶液,阴极为H+放电,阳极OH-放电生成O2,产物物质的量比值为2:1,C错误;D、正确。
本题难度:一般