微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)臭氧是一种强氧化剂,常用于消毒、灭菌等。
(1)O3可将KI氧化,生成的两种单质化学式为 、 。
(2)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如下表所示:
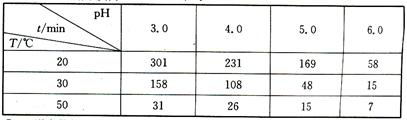
根据表中数据分析,pH升高,O3分解速率 ;温度升高,O3分解速率 (选填“加快”或“减慢”)。
(3)臭氧是理想的烟气脱硝试剂,其脱硝反应为:2NO2(g)+O3(g)  N2O5(g)+O2(g)。若反应在恒容密闭容器中进行,下列相关图像正确的是 (填字母)。
N2O5(g)+O2(g)。若反应在恒容密闭容器中进行,下列相关图像正确的是 (填字母)。
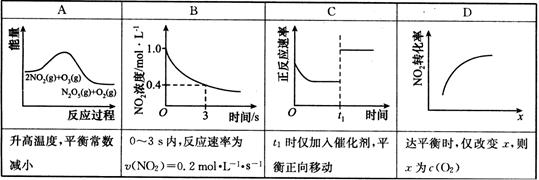
参考答案:18.(12分)(1)O2 I2 (2)①加快 加快 (3)AB(4分)
本题解析:(1)O3氧化KI,I-转化为I2的同时本身被还原生成O2。(2)根据表中数据分析,pH升高,O3分解速率加快;温度升高,O3分解速率加快;(3)A、该反应为放热反应,升高问题平衡朝逆向移动,平衡常数减小,正确;B、V(NO2)=0.2mol/(L?S),正确;C、催化剂不影响平衡移动,错误;D、通入氧气,平衡逆向移动,转化率减小,错误,选AB。
考点:考查臭氧的化学性质、外界条件对反应速率的影响。
本题难度:困难
2、填空题 如何降低大气中CO2的含量及有效地开发利用碳资源的研究显得尤为紧迫。
在催化剂作用下,CO2和H2可以制取甲醇和乙醇。如:2CO2(g)+6H2(g)  ?CH3CH2OH(g)+3H2O(g) 。
?CH3CH2OH(g)+3H2O(g) 。
(Ⅰ) 在一定压强下,利用CO2反应制取乙醇,测得反应的实验数据如下表。分析表中数据回答下列问题:
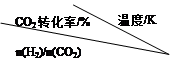
| 500
| 600
| 700
| 800
|
1.5
| 45
| 33
| 20
| 12
|
2.0
| 60
| 43
| 28
| 15
|
3.0
| 83
| 62
| 37
| 22
|
温度升高,平衡常数K值将?(填“增大”、“减小”、或“不变”)。提高氢碳比[n(H2)/n(CO2)], 平衡常数K值将?(填“增大”、“减小”、或“不变”)。
在600K时反应达到平衡,要使该平衡向右移动,其它条件不变时,可以采取的措施有
?(填序号)。
A.缩小反应器体积?B.通入CO2?C.升高温度到800K? D.使用合适的催化剂
(Ⅱ)某温度下,在体积为l L的密闭容器中充入lmol CO2和4mol H2,测得CO2和CH3OH(g)的浓度随时间变化如图所示。
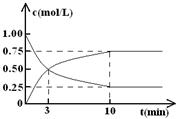
从反应开始到平衡,甲醇的平均反应速率v(CH3OH)=?;
氢气的平衡浓度为?mol/L。
参考答案:减小 , 不变 ;? AB; 0.075 mol/(L.min); 1.75
本题解析:(Ⅰ)根据表中数据可知,随着温度的升高,CO2的转化率减小,这说明升高温度平衡向逆反应方向移动,则正反应是放热反应,由此升高温度平衡常数减小。平衡常数只与温度有关系,由此提高氢碳比[n(H2)/n(CO2)], 平衡常数K值不变。根据方程式可知,正反应是体积减小的可逆反应,则缩小容器的体积,增大压强,平衡向正反应方向进行;通入CO2,增大反应物的浓度,平衡向正反应方向进行;升高温度,平衡向逆反应方向进行,催化剂不能改变平衡状态,所以答案选AB。
(Ⅱ)根据图像可知,反应进行到10min时物质的浓度不再发生变化,说明反应达到平衡状态。此时生成甲醇的浓度是0.75mol/L,则从反应开始到平衡,甲醇的平均反应速率v(CH3OH)=0.75mol/L÷10min=0.075 mol/(L・min)。根据方程式CO2(g)+3H2(g) ?CH3OH(g)+H2O(g)可知,消耗氢气的浓度是0.75mol/L×3=2.25mol/L,则剩余氢气的浓度是4mol/L-2.25mol/L=1.75mol/L。
?CH3OH(g)+H2O(g)可知,消耗氢气的浓度是0.75mol/L×3=2.25mol/L,则剩余氢气的浓度是4mol/L-2.25mol/L=1.75mol/L。
点评:该题是高考中的常见考点和题型,属于中等难度试题的考查,试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力,提升学生的学科素养。
本题难度:一般
3、填空题 在10 L的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下表:
t/℃
| 700
| 800
| 830
| 1 000
| 1 200
|
K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
|
请回答:
(1)该反应为 (填“吸热”或“放热”)反应。
(2)该反应的化学平衡常数表达式为K = 。
(3)能说明该反应达到化学平衡状态的是 (填字母)。
a.υ正(CO2)=υ正(H2) b.υ逆(CO)=υ逆(H2O)
c.υ逆(H2)=υ逆(H2O) d.υ正(H2)=υ逆(H2)
(4)某温度下,将CO2和H2各0.10 mol充入该容器中,达到平衡后,测得 c(CO)="0.0080" mol・L-1,则CO2的转化率为 。
(5)某温度下,平衡浓度符合下式:c(CO2)・c(H2)=c(CO)・c(H2O),试判断此时的温度为 ℃。
参考答案:(1)吸热 (1分)
(2)
(3)d(2分)
(4)80%(2分)
(5)830(2分)
本题解析:
试题解析:(1)升高温度,K值增大,说明升温平衡正向移动,所以正向为吸热反应。
(2)根据平衡常数的定义可得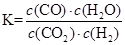
(3)当反应达到化学平衡状态时υ正=υ逆,a、b、c均代表同向的反应速率,错误,答案选d。
(4)CO2(g)+H2(g)?CO(g)+H2O(g)平衡后c(CO) =" 0.0080" mol・L-1,可计算出转化的c(CO2)=" 0.0080" mol・L-1,初始浓度c(CO2)="0.1mol/10L=0.01" mol・L-1,所以CO2的转化率为0.0080 mol・L-1/0.01 mol・L-1×100%=80%。
(5)根据c(CO2)・c(H2)=c(CO)・c(H2O)可知K=1.0,所以此时的温度为830℃。
考点:考查化学平衡常数的定义、化学平衡的特征判断、条件对平衡影响的运用、简单计算
本题难度:一般
4、选择题 一定温度时于密封容器中发生反应:mA(g)+nB(g) pC(g),达平衡后,若将气体体积压缩到原来的1/2。当再达平衡时C的浓度是原来的1.9倍,则下列叙述正确的是
pC(g),达平衡后,若将气体体积压缩到原来的1/2。当再达平衡时C的浓度是原来的1.9倍,则下列叙述正确的是
[? ]
A.平衡向正反应方向移动
B.C气体的质量分数增大
C.气体A的转化率降低
D.m+n>p
参考答案:C
本题解析:
本题难度:一般
5、计算题 一氧化碳变换反应 CO(g)+ H2O(g)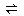 ?H2(g)+ CO2(g),在773K时,平衡常数Kc =" 9" ,如反应开始时CO和H2O的浓度都是0.020 mol/L ,计算在次条件下,CO的最大转化率是多少?
?H2(g)+ CO2(g),在773K时,平衡常数Kc =" 9" ,如反应开始时CO和H2O的浓度都是0.020 mol/L ,计算在次条件下,CO的最大转化率是多少?
参考答案:一氧化碳最大的转化率是75% 。
本题解析:CO(g) +? H2O(g)?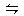 ?CO2(g)? +? H2(g)
?CO2(g)? +? H2(g)
初始浓度/mol・L-1:0.020? 0.020? 0? 0
转化浓度/mol・L-1: x? x? x? x
平衡浓度/mol・L-1:0.020―x? 0.020―x? x? x?
依题意,可得:?
K? = ? ?="?" 9
?="?" 9
解之,得:x =" 0.015" mol・L-1?
故一氧化碳最大的转化率为:
α(CO)= ? ×100% = 75%
×100% = 75%
本题难度:一般