|
|
|
高考化学知识点总结《化学平衡》高频试题特训(2017年最新版)(一)
2017-09-25 18:36:22
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
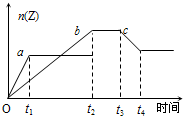
1、选择题 某密闭容器中,加入一定量的X和Y,发生如下反应:2X+Y?2Z.不同温度时,产物Z的生成情况如右图所示,a为T1℃时的情况,b为T2℃时的情况,c为T2℃时从时间t3开始加压的情况,下列叙述正确的是( ? )
A.反应“2X+Y?2Z”的△H<0
B.Z一定为气体,X一定为非气体
C.升高温度,化学平衡向正反应方向移动
D.若t2~t3段平衡常数为K1,t4后平衡常数为K2,则K1>K2
| 
2、选择题 下列事实不能用勒夏特列原理解释的是
A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率
B.合成氨工厂通常采用20 MPa-50 MPa压强,以提高原料的利用率
C.实验室用排饱和食盐水的方法收集氯气
D.经粉碎的黄铁矿在沸腾炉中燃烧得较快、较完全
|
3、填空题 以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如下:

回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为___。在(NH4)2SO4溶液中,存在NH4+ +H2O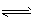 NH3・H2O+H+,该反应的平衡常数表达式为K=___ 。
NH3・H2O+H+,该反应的平衡常数表达式为K=___ 。
(2)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为___。
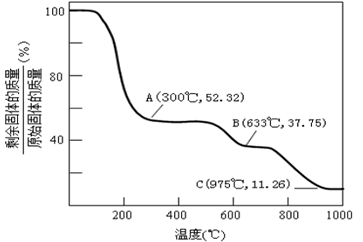
(3)固体NH4Al(SO4)2.12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体成分的化学式为___ 。
(4)综上分析,流程图中M的主要成分的化学式为___,M可用一种物质吸收以实现循环利用,该物质的名称是___。
4、填空题 硫酸工业中接触氧化是最重要的一个反应:2SO2(g) + O2(g)  2SO3(g) △H= -197kJ/mol。为了研究这一反应,在体积为2L的密闭容积中,投入2mol SO2,1molO2,然后控制反应温度,在反应进行至20min时加入一定的催化剂,测定并记录一定时间内容器内SO3的物质的量,得到下表:
2SO3(g) △H= -197kJ/mol。为了研究这一反应,在体积为2L的密闭容积中,投入2mol SO2,1molO2,然后控制反应温度,在反应进行至20min时加入一定的催化剂,测定并记录一定时间内容器内SO3的物质的量,得到下表:
时间/min
| 10
| 20
| 30
| 40
| 50
|
N(SO3)/mol
| 0.4
|
0.6
| 1.2
| 1.6
| 1.6
|
(1)反应前10 min,用O2表示该反应的反应速率v(O2)=
。
(2)该温度下,该反应的平衡常数为
。
(3)在反应进行至50min时,再向容器中充入2molSO2和1molO2,达到新平衡后,SO2的转化率将
。(填“增大”、“减小”或“不变”)
(4)保持温度不变,若在该容器中只投入2mol SO3,达到平衡时,反应吸收的热量为
kJ。
5、选择题 下图是关于反应A2(g)+3B2(g) 2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是
2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是
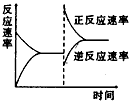
[? ]
A.升高温度,同时加压
B.降低温度,同时减压
C.增大反应物浓度,同时减小生成物浓度
D.增大反应物浓度,同时使用催化剂


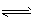 NH3・H2O+H+,该反应的平衡常数表达式为K=___ 。
NH3・H2O+H+,该反应的平衡常数表达式为K=___ 。
 2SO3(g) △H= -197kJ/mol。为了研究这一反应,在体积为2L的密闭容积中,投入2mol SO2,1molO2,然后控制反应温度,在反应进行至20min时加入一定的催化剂,测定并记录一定时间内容器内SO3的物质的量,得到下表:
2SO3(g) △H= -197kJ/mol。为了研究这一反应,在体积为2L的密闭容积中,投入2mol SO2,1molO2,然后控制反应温度,在反应进行至20min时加入一定的催化剂,测定并记录一定时间内容器内SO3的物质的量,得到下表: 2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是
2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是