微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 氟和氟盐是化工原料。由于氟气性质活泼,很晚才制取出来。
(1)不能通过电解纯净的液态HF获得F2,其原因是__________?;但电解液态KHF2时,两极分别得到F2和H2,写出阳极上HF2-?放电产生气体的电极反应式__________。
(2)利用K2MnF6和SbF5在一定条件下发生反应也能制取氟,同时生成KSbF6?和MnF3,化学方程式为____________,其中还原产物是___________。
(3)已知氟化氢气体中存在下列平衡?:H3F3 3HF?△H?>0,?H2F2?
3HF?△H?>0,?H2F2? 2HF?△H?>0。
2HF?△H?>0。
①若在定温定容条件下再充入H3F3,则H3F3与HF的浓度(mol/L)比值_________(填“增大”“减小”或“不变”,下同);
②若在定温定容条件下再充入HF,则H3F3与HF的浓度(mol/L)比值__________。
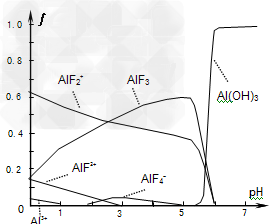
(4)一定浓度的HF和Al2(SO4)3混合液中,铝的?各种微粒含量随pH的分布曲线如图示。用NaOH使混合液的pH从5调整到7,写出有关反应的离子方程式为___________?。
参考答案:(1)氟化氢是共价化合物,纯液态时不电离,因而不导电?; HF2-?-2e-?=F2↑+H+?
(2)2K2MnF6?+4SbF5?=4KSbF6?+?2MnF3?+F2↑;?MnF3
(3)增大?;?增大
(4)AlF2++3OH-=Al(OH)3↓+2F-,AlF3+3OH-=Al(OH)3↓+3F-
本题解析:
本题难度:一般
2、选择题 在固定容积的密闭容器中,氮气和氢气合成氨的反应达到了平衡,此时容器中含有0.1molN2、0.3mol
H2、0.2molNH3。若维持原来的条件,向该容器中再同时加入0.1molN2、0.3molH2、0.2molNH3,则
[? ]
A.正、逆反应速率同时增大,化学平衡不移动
B.正、逆反应速率同时增大,平衡混合气中NH3的体积分数增大
C.正、逆反应速率同时增大,化学平衡向逆反应方向移动
D.正逆反应速率不变,化学平衡不移动
参考答案:B
本题解析:
本题难度:一般
3、选择题 mA(g)+nB(g)?pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
①体系的压强不再改变?
②绝热体系的温度不再改变?
③各组分的浓度不再改变
④各组分的质量分数不再改变?
⑤反应速率vA:vB:vC:vD=m:n:p:q
⑥单位时间内m?mol?A断键反应,同时p?mol?C也断键反应.
A.③④⑤⑥
B.②③④⑥
C.①③④⑤
D.①③④⑥
参考答案:①若反应前后气体的体积发生不变,体系的压强不再改变说明到达平衡,若反应前后气体的物质的量不变,体系的压强自始至终不变,体系的压强不再改变不能说明到达平衡,故①错误;
②随反应进行体系的温度发生变化,绝热体系的温度不再改变说明到达平衡,故②正确;?
③随反应进行各组分的浓度发生不变,各组分的浓度不再改变说明到达平衡,故③正确;
④随反应进行各组分的质量分数发生不变,各组分的质量分数不再改变说明到达平衡,故④正确;
⑤反应速率自始至终都按vA:vB:vC:vD=m:n:p:q,不能说明到达平衡,故⑤错误;
⑥A断键表示正反应速率,C断键表示逆反应速率,单位时间内m?molA断键反应,同时生成pmolC,C的断键与成键相等,说明到达平衡,故⑥正确.
故选B.
本题解析:
本题难度:简单
4、填空题 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示___________________,K值大小与温度的关系是:温度升高,K值______________ (填一定增大、一定减小、或可能增大也可能减小)。
(2)在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g) 2SO3(g) (△H< 0)
2SO3(g) (△H< 0)
①写出该反应的化学平衡常数表达式K=_____________________
②降低温度,该反应K值______________ ,二氧化硫转化率_________,化学反应速度_____________(以上均填增大、减小或不变)
③600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是__________________________。
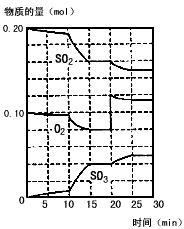
④据图判断,反应进行至20min时,曲线发生变化的原因是_____________________________________(用文字表达)
⑤10min到15min的曲线变化的原因可能是 __________________(填写编号)。
a.加了催化剂 b.缩小容器体积 c.降低温度 d.增加SO3的物质的量
参考答案:(1)可逆反应的进行程度越大;可能增大也可能减小
(2)①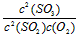 ;②增大;增大;减小;③15-20min和25-30min;④增加了O2的浓度;⑤ab
;②增大;增大;减小;③15-20min和25-30min;④增加了O2的浓度;⑤ab
本题解析:
本题难度:一般
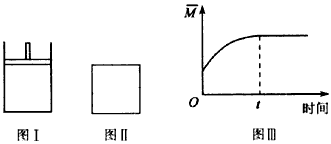
5、选择题 如图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器。 当其他条件相同时,在Ⅰ、Ⅱ 中分别加入
2 mol X和2 mol Y,开始时容器的体积均为VL,发生如下反应并达到平衡状态:2X(?)+Y(?)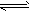 aZ(g)(提示:物质X、Y的状态均未知,物质Z的状态为气态)。此时I中X、Y、Z的物质的量之比为1:3:2。下列判断正确的是
aZ(g)(提示:物质X、Y的状态均未知,物质Z的状态为气态)。此时I中X、Y、Z的物质的量之比为1:3:2。下列判断正确的是
[? ]
A.物质Z的化学汁量数a=2
B.若Ⅱ中混合气体的平均相对分子质量(M)如图Ⅲ所示,则X、Y两种物质可能均为气态
C.若X、Y均为气态,则在平衡时X的转化率:Ⅰ<Ⅱ
D.若X为固态、Y为气态,则Ⅰ、Ⅱ中从开始到平衡所需的时间:Ⅰ>Ⅱ
参考答案:B
本题解析:
本题难度:一般