1��ѡ���� ��þ��������ƽ�в���ʢ��һ��Ũ�ȵ�NaOH��Һ���ձ��У��õ��ߺ͵��������ӳ�ԭ��أ�װ����ͼ��ʾ���˵�ع���ʱ������������ȷ����(? )

A��Mg��Al���ã�Mgʧȥ���ӱ�������Mg2+
B������������������Ĥ�����ɲ��ش���
C���õ�ص������·�У����������ɵ��Ӷ����ƶ��γɵ�
D��Al�ǵ�ظ�������ʼ����ʱ��Һ�л������а�ɫ��������
2��ѡ���� ��ѧ����������һ������ʽ��ﮡ�������أ�����ʱ���տ����е������ڶ���Ƴɵ����������Ϸ�Ӧ���ܷ�Ӧ�ɱ�ʾΪ2Li��O2 Li2O2�������й�˵����ȷ���ǣ�������
Li2O2�������й�˵����ȷ���ǣ�������
A�����ʱ������Ƴɵĵ缫��ӵ�Դ����
B���ŵ�ʱ�����տ�����22.4 L��O2������2 mol e���ӵ�ظ�������
C���ŵ�ʱ��Li���Ӹ����������ƶ�
D���õ�ؿ�ʹ�ú�Li����ˮ��Һ���������Һ
3��ѡ���� ��ͼ��ijѧ����Ƶ�һ��ԭ��أ���Ҫװ���е����Ʒ���ƫת��
��M��N��������ɲ�����

A��Zn��Zn
B��Zn��Cu
C��Cu��Cu
D��ʯī��ʯī
4������� (10��)�״��ϳɷ�ӦΪ��CO(g)+2H2(g) 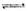 ?CH3OH(g)
?CH3OH(g)
��ҵ������Ȼ��Ϊԭ�ϣ���Ϊ�����Ʊ��״���
(1)�Ʊ��ϳ�����CH4+H2O��g��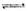 CO+3H2��Ϊ����ϳ�����H2������CO��������⣬ԭ������������CO2��CO3+H2=CO+H2O��Ϊ��ʹ�ϳ��������ѣ�������ԭ�����м����������̼�����Ϊ____________________________________��
CO+3H2��Ϊ����ϳ�����H2������CO��������⣬ԭ������������CO2��CO3+H2=CO+H2O��Ϊ��ʹ�ϳ��������ѣ�������ԭ�����м����������̼�����Ϊ____________________________________��
(2)�ϳɼ״����ٷ�Ӧ���� �����������仯����ͼ��ʾ��д���ϳɼ״����Ȼ�ѧ����ʽ__________________��
�����������仯����ͼ��ʾ��д���ϳɼ״����Ȼ�ѧ����ʽ__________________��

ʵ������1L�ܱ������н���ģ��ϳ�ʵ�顣��lmolCO��2molH2ͨ�������У��ֱ������300���500�淴Ӧ��ÿ��һ��ʱ���������м״���Ũ�����£�
(�������ݵ�λ��mol��L��1)
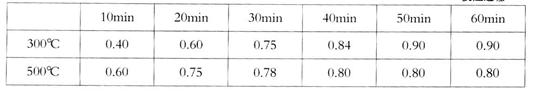 ��300��ʱ��Ӧ��ʼ10�����ڣ�H2��ƽ����Ӧ����Ϊ__________��
��300��ʱ��Ӧ��ʼ10�����ڣ�H2��ƽ����Ӧ����Ϊ__________��
��500��ʱƽ�ⳣ��K����ֵΪ___________��
��300��ʱ�����������ݻ�ѹ����ԭ����1��2���������������������£���ƽ����ϵ?������Ӱ����__________(����ĸ)��
a.c(H2)��С? b������Ӧ���ʼӿ죬�淴Ӧ���ʼ���
c.CH3OH�����ʵ�������? d������ƽ��ʱc(H2)��c(CH3OH)��С
5��ѡ���� �~���ؿ�����Ϊ���������ṩ��Դ�����ط�Ӧ�ɼ�Ϊ��2Li + I2?= 2LiI�������й�˵����ȷ����
A��I2����������Ӧ
B����缫Ϊ�õ�ص�����
C��������ӦΪ��Li �C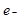 = Li+
= Li+
D���õ�طŵ�ʱ��ѧ��ת��Ϊ����