1��ѡ���� ����������ȷ����? (����)
A��һ����Ϊ��������Ũ��С��10��4 mol/Lʱ������Ϊ�Ѿ�������ȫ
B����ӦAgCl��NaBr=AgBr��NaCl����ˮ��Һ�н��У�����ΪAgBr��AgCl��������ˮ
C��Al(OH)3(s) Al3��(aq)��3OH��(aq)��ʾ�����ܽ�ƽ�⣬Al(OH)3
Al3��(aq)��3OH��(aq)��ʾ�����ܽ�ƽ�⣬Al(OH)3 Al3����3OH����ʾˮ��ƽ��
Al3����3OH����ʾˮ��ƽ��
D��ֻ�з�Ӧ���ʺܸߵĻ�ѧ��Ӧ����Ӧ���ڹ�ҵ����
�ο��𰸣�B
�����������������Ũ��С��10��5 mol/Lʱ������Ϊ�ѳ�����ȫ��A�����Al (OH)3 Al3����3OH����ʾAl(OH)3�ĵ���ƽ�⣬C�����ѧ��Ӧ�ܷ�Ӧ���ڹ�ҵ�����뷴Ӧ�����ޱ�Ȼ��ϵ��
Al3����3OH����ʾAl(OH)3�ĵ���ƽ�⣬C�����ѧ��Ӧ�ܷ�Ӧ���ڹ�ҵ�����뷴Ӧ�����ޱ�Ȼ��ϵ��
�����Ѷȣ�һ��
2��ѡ���� ���л�ѧʵ����ʵ������Ͷ���ȷ����
[? ]
A�����ˮ�еμ�CCl4�����ú�ֲ㣬CCl4����Ϻ�ɫ��˵������CCl4�ӵ�ˮ����ȡ��
B����SO2ˮ��Һ�еμ������ữ��BaCl2��Һ���а�ɫ�������ɣ�˵��BaSO3����������
C����0.1mol��L-1 FeSO4��Һ�еμ���������KMnO4��Һ��KMnO4��Һ��ɫ��˵��Fe2+����������
D����2.0mLŨ�Ⱦ�Ϊ0.1mol��L-1��KCl��KI�����Һ�еμ�1~2��0.01mol��L-1 AgNO3��Һ���������ʻ�ɫ��˵��AgCl��Ksp��AgI��Ksp
�ο��𰸣�AD
���������
�����Ѷȣ�һ��
3��ѡ���� ��֪25��ʱ��Mg(OH)2���ܶȻ�����Ksp �� 5.6��10-12��MgF2���ܶȻ�����Ksp �� 7.4��10-11������˵����ȷ����
A��25��ʱ����Mg(OH)2������Һ�м���������NH4Cl���壬c(Mg2+)����
B��25��ʱ������Mg(OH)2��Һ�뱥��MgF2��Һ��ȣ�ǰ��c(Mg2+)��
C��25��ʱ��Mg(OH)2������ͬ���ͬŨ�ȵİ�ˮ��NH4Cl��Һ�е�Ksp��Ƚϣ�ǰ��С
D��25��ʱ����Mg(OH)2������Һ�м��뱥��NaF��Һ��Mg(OH)2������ת����MgF2
�ο��𰸣�A
���������
��ȷ�𰸣�A
A ����������NH4Cl���壬NH4�� ��OH�D��ϣ��ٽ��ܽ�Mg(OH)2ƽ�������ƶ���c(Mg2+)����
B����ȷ��Mg(OH)2���ܶȻ�����С��c(Mg2+)С
C����ȷ���ܶȻ�����ֻ���¶��йأ�
D������ȷ��Mg(OH)2��2F�D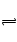 MgF2��2OH�D���Ǹ�������̣�ƽ��������ƶ���һ�������£�Ҳ���������ƶ���
MgF2��2OH�D���Ǹ�������̣�ƽ��������ƶ���һ�������£�Ҳ���������ƶ���
�����Ѷȣ���
4������� ��п�������Ĺ�ҵ��������п�������˺�Zn�⣬������Fe��Al��Cd��SiO2�����ʣ�������п����ȡ������ZnSO4��7H2O�ͽ����ӣ�Cd����һ������ij��ԣ����������£�
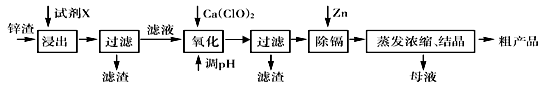
��֪��Fe3+��Al3+��Zn2+��Cd2+��Fe2+������������ȫ����ʱ��pH�ֱ�Ϊ��3.2��4.7��6.5��9.4��9.7���Իش��������⣺
��1������ʱ�õ����Լ�XΪ �� д���ܽ�����мӿ�������ʺ���߽����ʵ������ʩ��_______________________________��______________________________��
��2��д������Ca(ClO)2��Ӧ�����ӷ���ʽ ��
��3������pH���̿���ѡ�� ���ZnO����NaOH�����������̵�pH����һ�����5����Ŀ���� ��
��4��д�����˺���������п�۷�Ӧ�����ӷ���ʽ ��
��5��������Ũ������ʱ��Ҫ��ȡʵ���ʩ�ǣ� ��
�ο��𰸣���1��H2SO4��Һ �ʵ����¡���ֽ��衢�ӳ��ܽ�ʱ��ȣ������𰸺���Ҳ���֣�
��2��2H++ClO��+2Fe2+ =Cl��+2Fe3++H2O����ƽ����1�֣�
��3��ZnO ����ȥFe3+��Al3+����ֹZn2+��������
��4��Zn+Cd2+=Zn2++Cd ��5������һ������ȣ������������Ҳ���֣�
�����������1���������Ʊ�����п����ĵĹ������̣�п���к������ܵĶ����������ʣ�ѡ�����ܳ�ȥ�������裬���Ǿ������������ʣ�Ӧѡ������������ӵ�������Һ�����ܽ⡣��Ҫ�ӿ�������ʺ���߽����ʣ������ʵ������¶Ȼ������Һ���ʵ��ӳ�ʱ��ȡ�
��2���������������Һ�к�������Fe3+��Al3+��Zn2+��Cd2+��Fe2+ �����ӣ�������Щ���ӷֱ������pHֵ��Ӧ�ð�Fe2+ ����ΪFe3+ �ڳ�����ȥ�����Լ���������Ca(ClO)2 �����ķ�Ӧ��ʽΪ��2H++ClO��+2Fe2+ =Cl��+2Fe3++H2O��
��3���������������Ʊ���������п���壬�����ڵ���pHʱҪע�ⲻ���������ʣ�����Ӧ��ѡ��ZnO���ڣ�������pHֵ��5����Ŀ����ʹ���׳�����Fe3+��Al3+ �ȳ�����ȥ����ֹpH���߰����ɵ�Al(OH)3�ܽ⡢��Zn2+ ������
��4�����ϲ�������pH����Һ�л�������������Cd2+ ������Cd2+ ������pHֵ��Zn2+ ������pHֵ��������Բ����ó�������ȥ������Ҫ���뵥��Zn��Cd�û���������˷��������ӷ���ʽΪ��Zn+Cd2+=Zn2++Cd��
��5������п������Ũ��ʱ������ˮ�⣬����Ϊ�˼���ˮ��������ʣ�Ӧ�ñ�����Һһ������ȡ�
���㣺���⿼����ǻ�ѧ���������⣬���⿼�ıȽϻ������������ͽ϶ࡣ
�����Ѷȣ�����
5��ѡ���� ����ʱ��CaCO3��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪CaCO3���ܶȻ������£�Ϊ2.8��10-9������˵���в���ȷ����

A��x����ֵΪ2��10-5
B��c��ʱ��CaCO3����
C����������ˮ��ʹ��Һ��d���� a��
D��b����d���Ӧ���ܶȻ����
�ο��𰸣�C
�����������
�����Ѷȣ�һ��