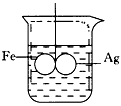
1、选择题 如图所示,在铁圈和银圈的焊接处,用一根棉线将其悬在盛水的烧杯中,使之平衡;小心地向烧杯中央 滴入CuSO4溶液,片刻后可观察到的现象是
[? ]
A.铁圈和银圈左右摇摆不定
B.保持平衡状态
C.铁圈向下倾斜
D.银圈向下倾斜
参考答案:D
本题解析:
本题难度:一般
2、填空题 (12分)(1)由氢气和氧气反应生成1 mol水蒸气放热241.8kJ,写出该反应的热化学方程式: 。若1g水蒸气转化成液态水放热2.5kJ,则氢气的燃烧热为△H= kJ/mol。
(2)近年来已经研制出甲烷(CH4)燃料电池,该电池的电解质溶液为H2SO4溶液,
写出该电池负极的电极反应式:_____________________________。
该电池总反应式:_____________________________。
(3)用惰性电极电解AgNO3溶液,写出该电解反应的化学方程式 ;若在阳极收集到 0.32 g O2,中和电解生成的酸需0.4 mol・L-1NaOH溶液 mL
参考答案:(1)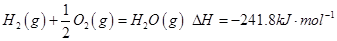 ;―286.8;
;―286.8;
(2)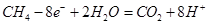 ;
; ;
;
(3)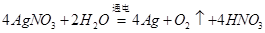 ;100
;100
本题解析:根据热化学方程式书写原则,该反应的热化学方程式为 ;18g水蒸气转化成液态水放热2.5kJ×18,由氢气和氧气反应生成1 mol液态水放热241.8kJ+2.5kJ×18,所以氢气的燃烧热为△H=―286.8kJ/mol;(2)甲烷燃料电池,电解质溶液为H2SO4溶液,总反应即甲烷燃烧的方程式
;18g水蒸气转化成液态水放热2.5kJ×18,由氢气和氧气反应生成1 mol液态水放热241.8kJ+2.5kJ×18,所以氢气的燃烧热为△H=―286.8kJ/mol;(2)甲烷燃料电池,电解质溶液为H2SO4溶液,总反应即甲烷燃烧的方程式 ,负极反应为甲烷失电子,发生氧化反应,反应式为
,负极反应为甲烷失电子,发生氧化反应,反应式为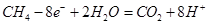 。(3)电解AgNO3溶液,阳极OH―发生氧化反应生成氧气,阴极Ag+的电子发生还原反应生成银单质,所以总反应为
。(3)电解AgNO3溶液,阳极OH―发生氧化反应生成氧气,阴极Ag+的电子发生还原反应生成银单质,所以总反应为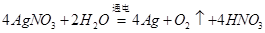 ;得到0.01mol gO2,生成硝酸0.04mol,所以消耗氢氧化钠0.04mol,根据
;得到0.01mol gO2,生成硝酸0.04mol,所以消耗氢氧化钠0.04mol,根据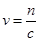 ,消耗氢氧化钠溶液100mL
,消耗氢氧化钠溶液100mL
考点:本题考查热化学方程式、燃料电池、电解原理。
本题难度:一般
3、选择题 银锌蓄电池的反应方程式为 Zn(OH)2 + 2Ag Zn+ Ag2O+H2O,此电池放电时,负极上发生反应的物质为
Zn+ Ag2O+H2O,此电池放电时,负极上发生反应的物质为
[? ]
A.Ag
B.Zn(OH)2
C.Ag2O
D.Zn
参考答案:D
本题解析:
本题难度:一般
4、选择题 世博会中国馆、主题馆等建筑使用光伏并网发电,总功率达4兆瓦,是历届世博会之最,通过并网,使用半导体照明(LED)。已知发出白光的LED 是由GaN芯片和钇铝石榴石(YAG,化学式:Y3Al5O12)芯片封装在一起做成的。下列有关叙述正确的是
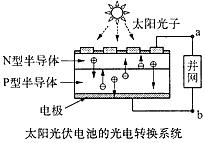
[? ]
A.光伏电池是将太阳能直接转变为电能
B.图中N型半导体为正极,P 型半导体为负极
C.电流从a 流向b
D.LED中的Ga和Y都显+3价
参考答案:AD
本题解析:
本题难度:一般
5、选择题 下图各装置中,不能构成原电池的是
[? ]
A.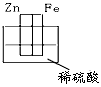
B.
C.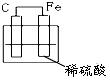
D.
参考答案:D
本题解析:
本题难度:简单