1、选择题 某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量)
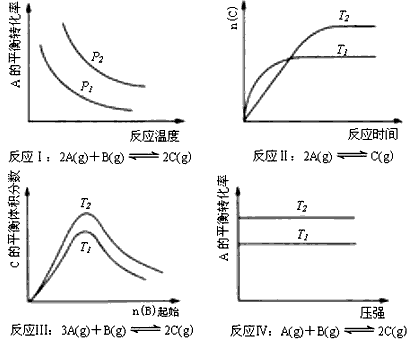
根据以上规律判断,上列结论正确的是
[? ]
A.反应Ⅰ:△H>0, P2>P1
B.反应Ⅱ:△H<0, T1>T2
C.反应Ⅲ:△H>0, T2>T1; 或△H<0, T2<T1
D.反应Ⅳ:△H<0, T2> T1
参考答案:BC
本题解析:
本题难度:一般
2、填空题
氢气在化学工业中有广泛用途。
(1)实验室用锌和稀硫酸制取氢气,反应过程中,溶液中水的电离平衡______移动(填“向左”、“向右”或“不”);若加入少量的_________(填编号),产生氢气速率加快。
A.NaNO3 B.CuSO4 C.CH3COONa D.NaHSO3
工业合成氨的反应原理为N2(g)+3H2(g) 2NH3(g)。实验室模拟化工生产,控制起始浓度均为
2NH3(g)。实验室模拟化工生产,控制起始浓度均为
c(N2)= 1.50 mol/L、c(H2)=2.50 mol/L,分别在三种不同实验条件下反应,N2浓度随时间变化如下图。

请回答下列问题:
(2)平衡时反应物的转化率:实验Ⅲ比实验I______(填“大”、“小”或“相同”)。
(3)与实验I比较,实验Ⅱ改变的条件为__________, 判断依据是______________________。
(4)实验Ⅲ的平衡常数K=_________;恒温恒容条件下,向实验Ⅲ达到平衡的容器中通入N2和NH3,使N2 和NH3浓度均变为原平衡的2倍,平衡__________(填编号)。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动 D.无法判断是否移动
参考答案:(1)向右;B
(2)小
(3)加入催化剂;实验Ⅱ和实验I的平衡状态相同,而实验Ⅱ达到平衡所需时间短
(4)1.00;B
本题解析:
本题难度:一般
3、填空题 向某密闭容器中加入4 mol A、1.2 mol C和一定量的B三种气体,一定条件下发生反应,各物质的浓度随时间变化如甲图所示[已知t0~t1阶段保持恒温、恒容,且c(B)未画出]。乙图为t2时刻后改变反应条件,反应速率随时间的变化情况,已知在t2、t3、t4、t5时刻各改变一种不同的条件,其中t3时刻为使用催化剂。
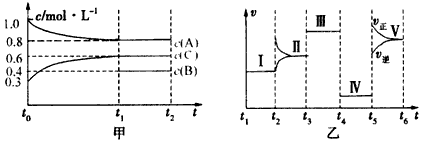
(1)若t1=15s,则t0~t1阶段的反应速率为v(C)=__________。
(2)t4时刻改变的条件为___________,B的起始物质的量为___________。
(3)t5时刻改变的条件为___________,该反应的逆反应为____________ (填“吸热反应”或“放热反应”)。
(4)已知t0~t1阶段该反应放出或吸收的热量为Q kJ(Q 为正值),试写出该反应的热化学方程式:___________________。
(5)图乙中共有I~V五处平衡,其平衡常数最大的是___________。
参考答案:(1)0.02 mol・L-1・s-1
(2)减小压强;2 mol
(3)升高温度;放热反应
(4)2A(g)+B(g)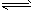 3C(g) △H=+2. 50 kJ/mol
3C(g) △H=+2. 50 kJ/mol
(5)V
本题解析:
本题难度:一般
4、选择题 COCl2(g)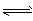 CO(g)+Cl2(g) ;△H>0量当反应达到平衡时,下列措施能提高COCl2转化率的是
CO(g)+Cl2(g) ;△H>0量当反应达到平衡时,下列措施能提高COCl2转化率的是
[? ]
①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,
A.①②④
B.①④⑥
C.②③⑥
D.③⑤⑥
参考答案:B
本题解析:
本题难度:一般
5、选择题 下图所示为800°C时A、B、C三种气体在密闭容器中反应时浓度的变化只从图上分析不能得出的结论是

[? ]
A.A是反应物
B.前2min A的分解速率为0.1mol・L-1・min-1
C.达平衡后,若升高温度,平衡向正反应方向移动
D.达平衡后,若增大压强,平衡向逆反应方向移动
参考答案:C
本题解析:
本题难度:一般